Clear Sky Science · zh
肝细胞癌血管的分形分析显示与血管侵袭无关的区域性差异
通过血管观察癌症
临床医生知道,癌症会生长出自身混乱的血管网络,而这些血管的排列方式会影响治疗效果。在肝癌中,针对血供的药物已成为标准疗法的一部分,但目前的实验室指标主要统计血管数量,而不是它们的布局。本研究提出了一个简单但有力的问题:我们能否用少数几个数值捕捉肿瘤血管的“模式”,这些模式在肿瘤、邻近组织及肝脏其他部位是否存在差异?
枝状网络中隐藏的模式
研究者将焦点放在肝细胞癌——最常见的原发性肝癌。他们检查了29例患者的组织样本,这些肝脏标本经过染色,使血管内皮在显微镜下呈现棕色。研究不再只是计数血管,而是分析血管如何在空间中共同填充,采用常用于海岸线或树枝等复杂自然形状的数学工具。使用了两个关键测度:一个描述血管网络的“错综复杂”程度,另一个描述血管间空隙的分布方式。将这些数值合并后,可以把血管网络的视觉复杂性浓缩为便于在肝脏不同区域间比较的形式。
将显微图像转成可测量的图谱
为此,团队首先需要在大型数字切片上可靠地区分血管和背景组织。他们建立了一个自动图像处理流程,识别出棕色染色的血管,去除噪声并填充血管内部,从而生成清晰的黑白血管网络图。这些自动分割结果经肝脏病理学专家核对,发现总体上吻合良好,尤其是在影响全局血管组织测度的方面。随后将切片切分为许多较小的图块,每块归入三类区域之一:肿瘤、肿瘤周围组织(肿周)或远端非肿瘤肝组织。包含坏死组织或主要伪影的图块被仔细排除,因为它们可能模拟出密集且不真实的血管模式。
肿瘤区域与其他区域的差异
在数千个图块中,研究发现三类肝组织在血管模式上存在明显且统计学显著的差异。非肿瘤肝组织表现出最高的复杂性,在较大尺度上几乎像一种填充空间的网状结构。肿周组织位于中间,而肿瘤区域的复杂性持续较低。另一项关于血管间空隙如何排列的相关测度也从非肿瘤到肿周再到肿瘤逐步增加,表明肿瘤相关血管更为聚集且空间相关性更强。关键的是,肿瘤是否开始侵入附近血管——这是一个重要的临床警示信号——并未显著改变这些总体模式。血管网络的结构主要受肿瘤存在本身的影响,而非这一侵袭步骤。
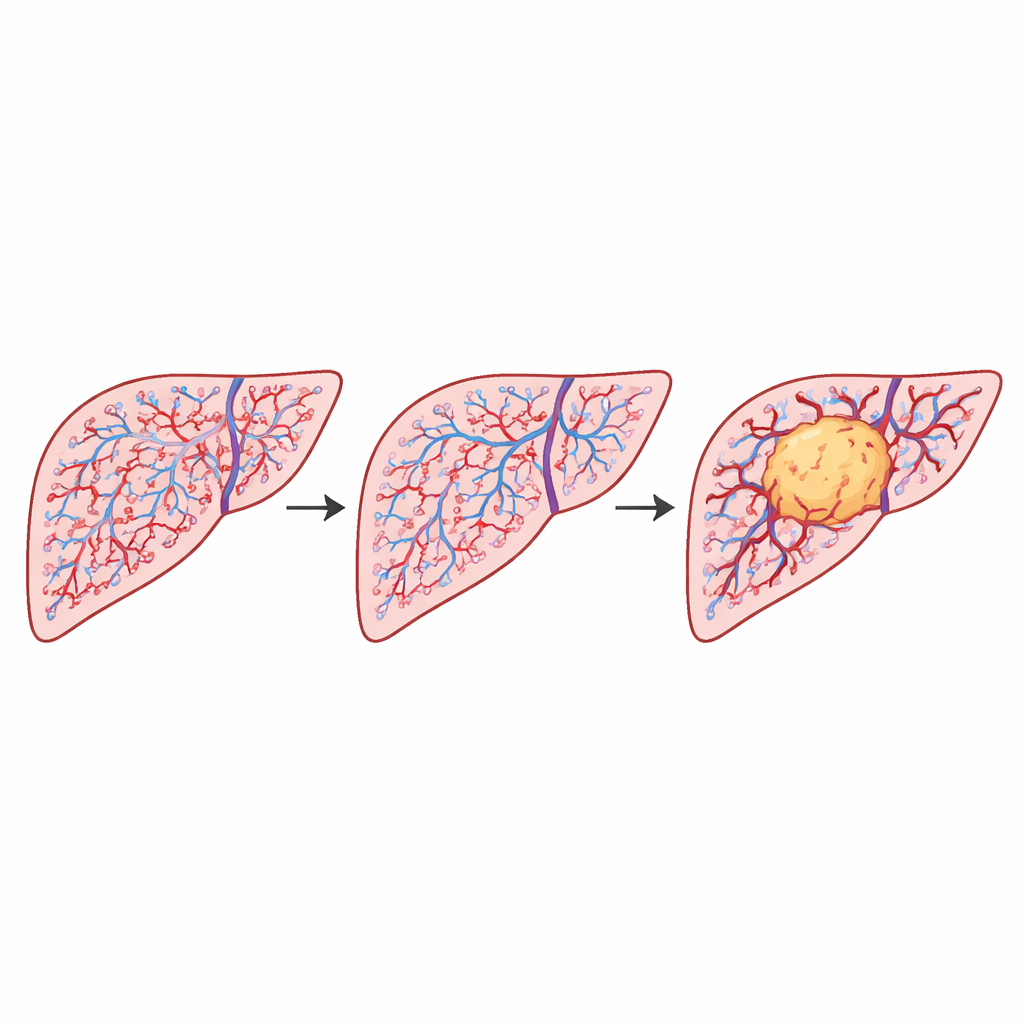
血管形状与尺寸为何重要
为理解这些数值差异背后的原因,作者更细致地观察了单个血管的形状与尺寸。在健康肝脏中,存在大量小而圆的血管堆积,伴随少数较大血管。而在肿瘤区域,总血管面积相似,但血管在尺寸上分布更均匀,且更常呈拉长或不规则形状。简单模型表明,富含许多小而圆血管的网络在“覆盖”模式时需要更多的小格子,从而提高其复杂性测度。相比之下,小血管较少且尺寸更统一的网络即便总血管面积相近,看起来也不那么错综复杂。这种几何学上的转变与肿瘤内复杂性下降的观察结果相吻合,并解释了血管形状分布的细微变化如何重塑整体血管模式。
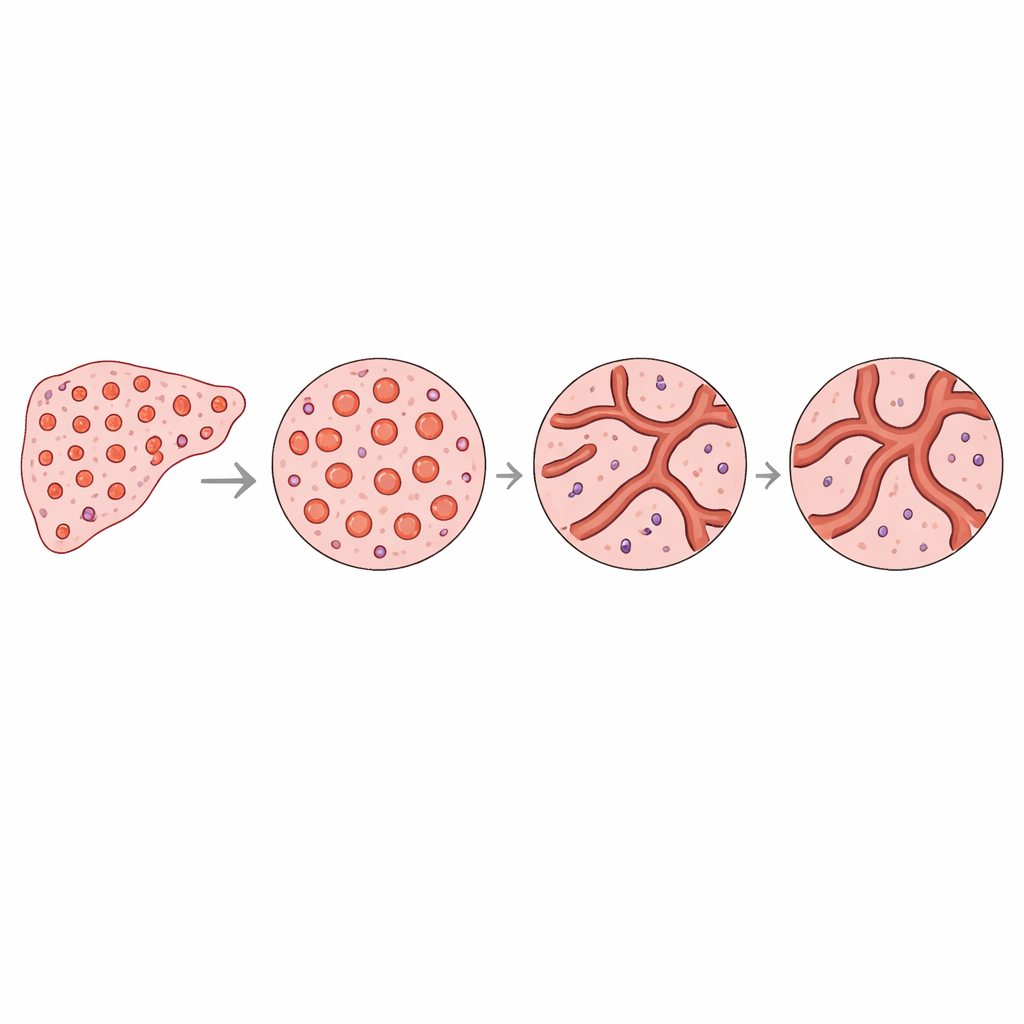
这对未来影像学可能意味着什么
对非专业读者而言,主要结论是:肝肿瘤不仅仅是长出更多血管;它们以一种不同且可测量的方式重新组织血管,并将这种影响扩展到周围组织。这些差异可以被简洁的数学描述符捕捉,概括血管及其间隙的排列方式。研究表明,未来先进的影像方法可能在无需活检的情况下估算这些描述符,提供关于肿瘤影响范围及其血供结构的新型无创生物标志物。同时,研究也显示,微观层面上的血管侵袭并不一定在大尺度血管模式上留下可识别的指纹,这强调并非所有危险的肿瘤行为都能仅通过血管结构被观察到。
引用: Penney, J., Nardon, V., Beaufrere, A. et al. Fractal analysis of hepatocellular carcinoma vasculature shows regional differences independent of vascular invasion. Sci Rep 16, 11049 (2026). https://doi.org/10.1038/s41598-026-38580-x
关键词: 肝癌血管, 血管分形结构, 肝细胞癌, 肿瘤微环境, 无创影像生物标志物