Clear Sky Science · zh
粪便代谢信号与克罗恩病中微生物群及系统性代谢通路的变化相关
为什么你的肠道化学很重要
克罗恩病是一种慢性疾病,免疫系统攻击消化道,导致疼痛、腹泻和长期损伤。虽然我们知道肠道细菌参与其中,本研究提出了一个更深入的问题:肠道中产生并在血液中循环的微量化学物质如何将肠道微生物与全身健康联系起来?通过追踪来自有无克罗恩病个体的粪便和血液中的这些化学信号,研究者显示肠道化学成分的变化可能助长有害微生物的繁荣,并可能为基于饮食和代谢的治疗开辟新途径。
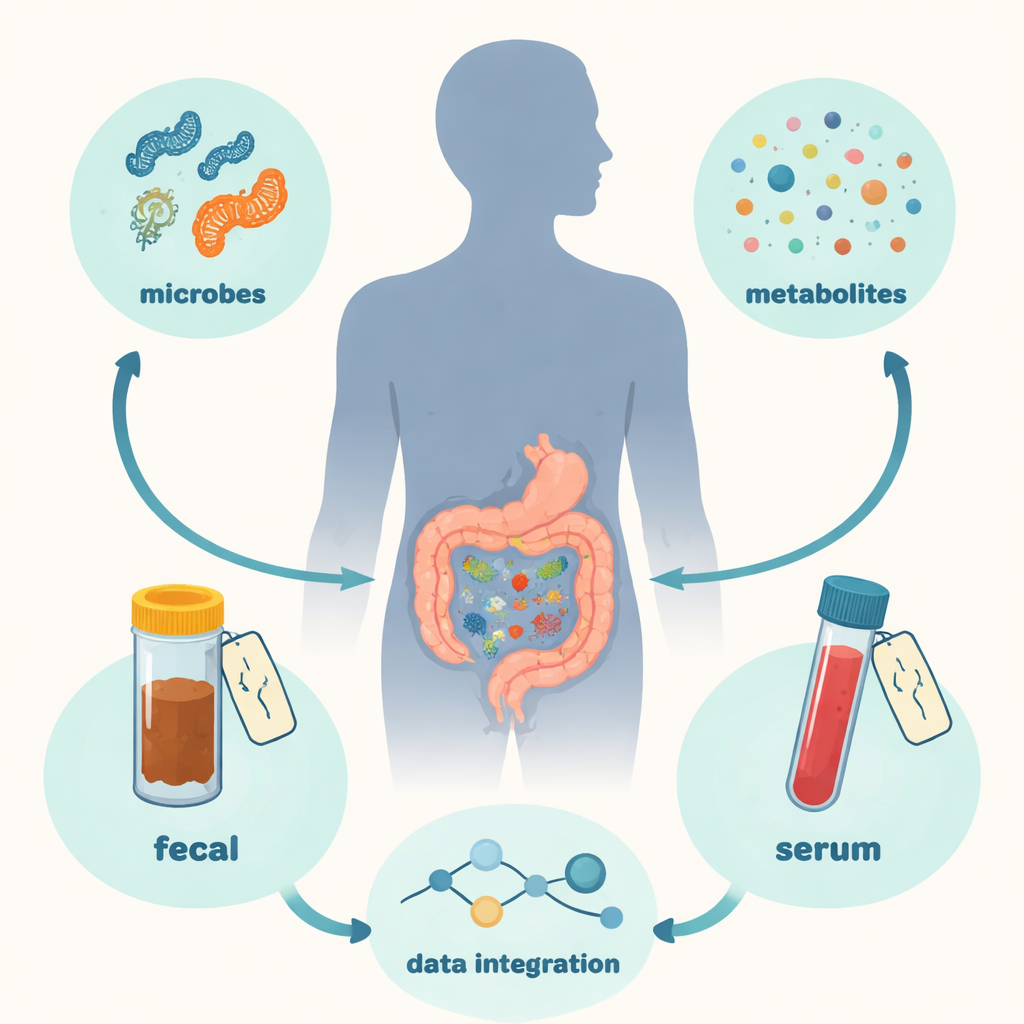
数据背后的人群
研究团队追踪了123名成人,其中包括80名克罗恩病患者和43名健康志愿者。对每位受试者采集了粪便和血液样本,有时随访并重复采样。从这些样本中,他们使用被称为质谱的高灵敏技术测量了数百种小分子(代谢物),并通过DNA测序绘制了肠道细菌群落图谱。这种“多组学”方法让他们不仅看到哪些微生物存在,还能识别肠道和血液中哪些化学通路处于活跃状态,以及这些模式如何随疾病发作或缓解而改变。
肠道糖类与不速之客的口腔细菌
粪便样本中最引人注目的发现之一是:克罗恩病患者的粪便中多种复杂糖类含量更高,包括海藻糖、棉子糖、紫苏糖、葡萄糖和果糖。与此同时,这些糖类与通常存在于口腔的细菌(例如维氏菌属和链球菌属)密切相关,这些细菌已迁移到发炎的肠道中。数据表明,肠内过量或吸收不良的糖类可能作为“燃料”,帮助这些位置不当且与炎症相关的微生物定殖并持续存在。这与通过限制某些碳水化合物和加工添加剂的饮食干预治疗克罗恩病的做法相符,提示了为何这些饮食在某些患者中可能有效的具体化学理由。
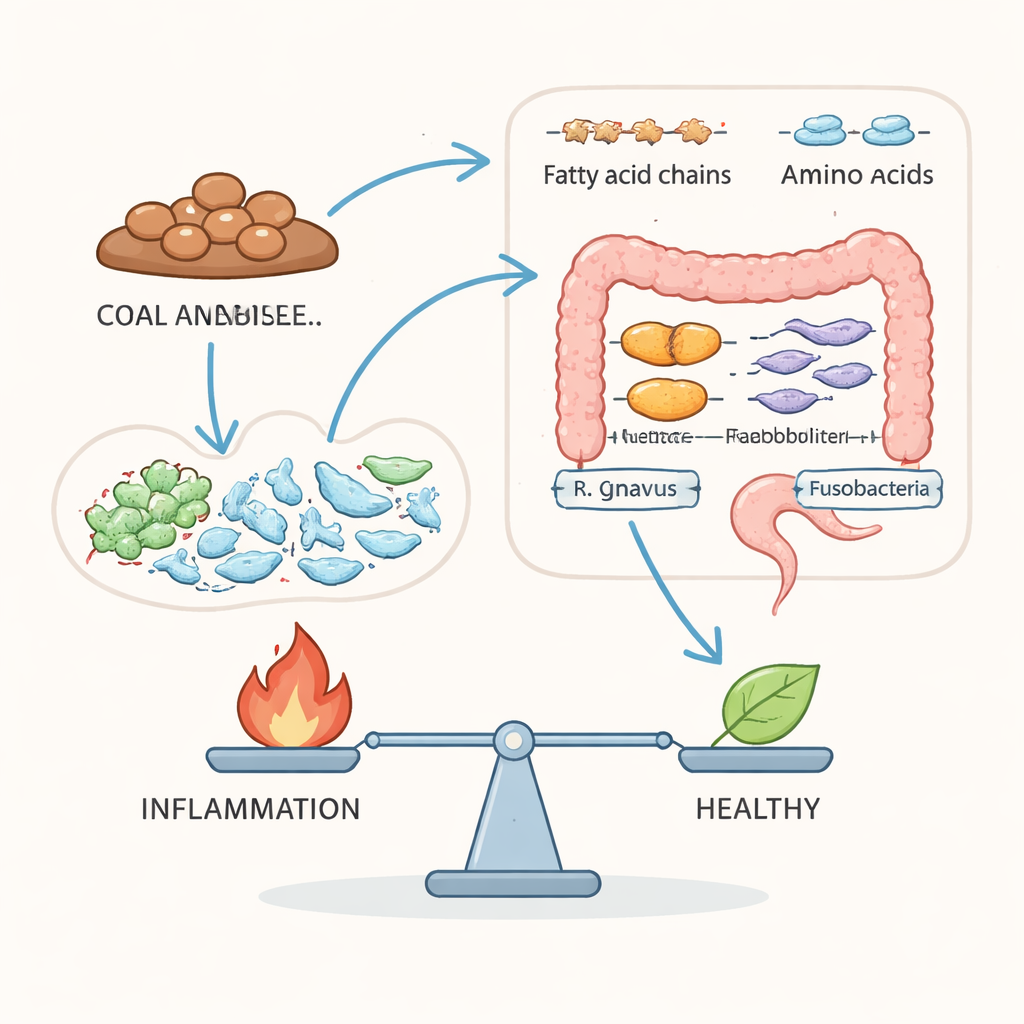
脂肪分子、氨基酸与能量利用的转变
研究还发现了克罗恩病中能量代谢的更广泛重塑。在血液中,克罗恩病患者表现出对与糖分解和细胞“能量工厂”(线粒体)相关的经典能量通路使用减少的迹象,同时与脂肪利用相关的信号增加。粪便中的模式则相反:与糖分解和核心能量循环相关的通路更为活跃,而长链脂肪的分解——结肠上皮细胞的重要燃料——似乎受损。某些由花生四烯酸衍生的促炎脂质在粪便中富集,并与先前与克罗恩病相关的肠道细菌(如Ruminococcus gnavus和梭杆菌属)紧密相关。与此同时,色氨酸、酪氨酸、苯丙氨酸和组氨酸等必需氨基酸在活动期的粪便中积聚,但在血液中往往下降,提示鹅病期吸收受损并伴随微生物代谢改变。
可追踪疾病活动性的信号
由于对患者在疾病安静期和活动期都进行了采样,研究团队得以探究哪些化学模式与症状以及血液和粪便中的客观炎症标志相一致。许多能将克罗恩病与健康区分开的粪便代谢物,随着发作、C反应蛋白升高或粪便钙卫蛋白升高而发生变化。这些代谢物还与先前建立的“菌群失调指数”相关,该指数衡量一个人肠道微生物组偏离健康状态的程度,以及与肠道细菌的总体多样性相关。换言之,粪便中特定的化学特征持续地同时与炎症活动和微生物群落受扰动的程度相关联。
这对患者意味着什么
综合来看,这些发现将克罗恩病描绘为微生物与代谢交织的疾病。肠道中额外的糖类以及脂肪和氨基酸处理的改变似乎支持与炎症相关的细菌,而这些细菌反过来可能产生更多促炎分子,形成自我加强的循环。虽然该研究并不证明因果关系,但它强调了粪便代谢物作为可能的杠杆,能够通过饮食、靶向补充剂或未来重塑微生物代谢的药物将肠道生态系统引向更健康的状态。对患者而言,这项工作强化了这样一个观念:肠道内发生的化学变化不仅仅是疾病的副产物——它们可能是驱动疾病的部分引擎,因此在未来几年内成为更精确、侵入性更小治疗策略的有前景的靶点。
引用: Levhar, N., Hadar, R., Braun, T. et al. Fecal metabolic signals are associated with changes in microbiota and systemic metabolic pathways in Crohn’s disease. Sci Rep 16, 6991 (2026). https://doi.org/10.1038/s41598-026-38558-9
关键词: 克罗恩病, 肠道微生物组, 代谢组学, 肠道炎症, 饮食与肠道健康