Clear Sky Science · zh
比较并联合使用 xevinapant、ATR 抑制剂和 PARP 抑制剂以提高对 HPV 阴性头颈部鳞状细胞癌细胞的放射增敏作用
为何增强放疗很重要
放射治疗是口腔和咽喉癌的主要治疗方法,但许多肿瘤对此具有抵抗性,迫使医生采用可能损伤正常组织的高剂量。本研究提出了一个对患者影响重大的实际问题:在几种旨在使肿瘤细胞更易受损的现代抗癌药物中,哪些在与放疗联合时对实验室培养的难治性 HPV 阴性头颈癌细胞效果最佳?
现行治疗及其局限
局部晚期头颈部鳞状细胞癌患者通常接受放疗与顺铂化疗相结合的治疗,或先手术后再行放疗。虽然这种方案可以控制癌症,但常常使患者出现严重的长期副作用,如吞咽困难、口干、听力问题和肾损伤。许多年长或体弱的患者根本无法耐受顺铂。这推动了人们对“放射增敏剂”的浓厚兴趣——即那些使肿瘤细胞更易被放射线杀死的药物,从而使治疗更有效或可能更温和。
曾被寄予厚望却受挫的一种药物
其中一种药物 xevinapant 曾被视为突破性进展。它模拟一种名为 SMAC 的天然蛋白,阻断帮助癌细胞逃避程序性细胞死亡的分子。在早期研究中,将 xevinapant 加入标准的放化疗能够改善头颈癌患者在一项 II 期临床试验中的结局,因而人们一度希望它能成为新的治疗标准。但一项规模更大的 III 期试验(TrilynX)在中期分析时被提前终止,结果显示 xevinapant 组不仅未获益,反而生存更差且不良反应更多。这一意外失败迫切需要重新评估 xevinapant 对放疗的实际帮助程度,并将其与其他更新策略进行比较。
将三种策略进行正面比较
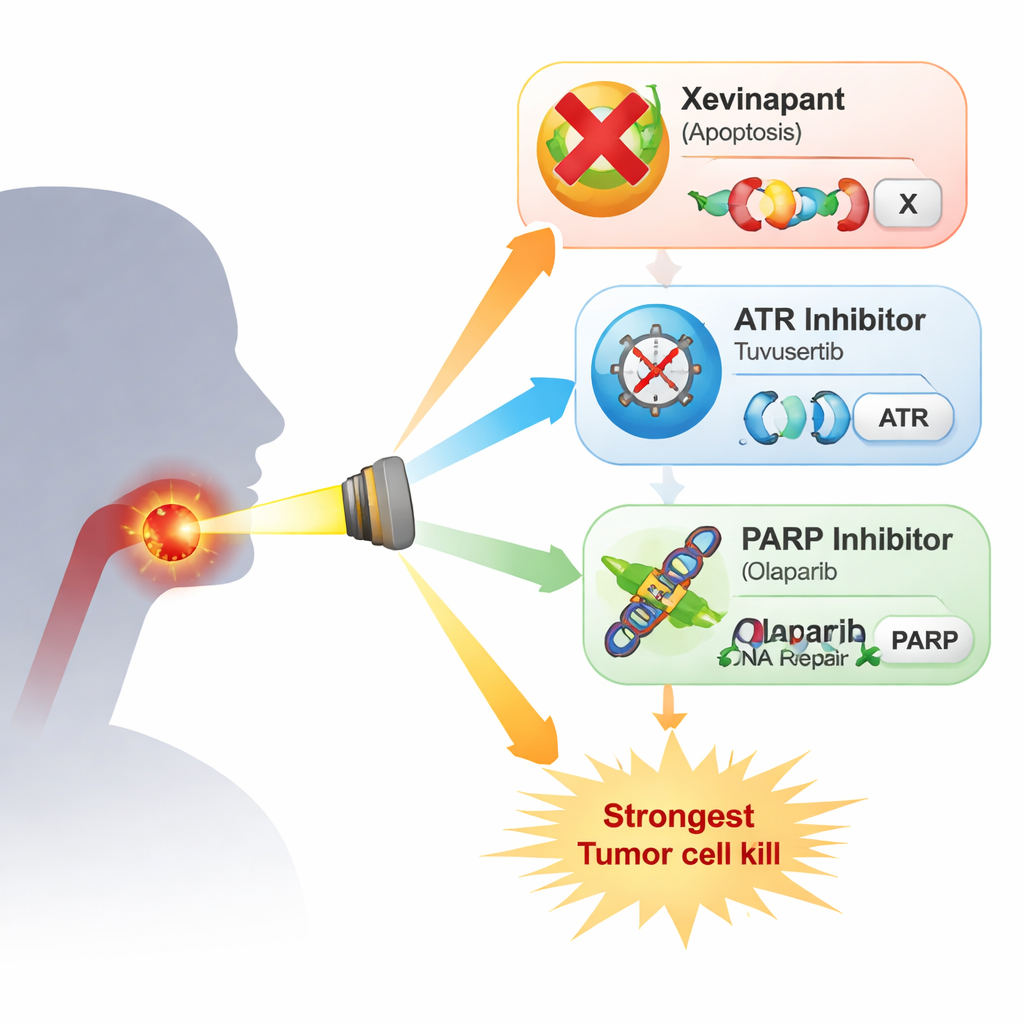
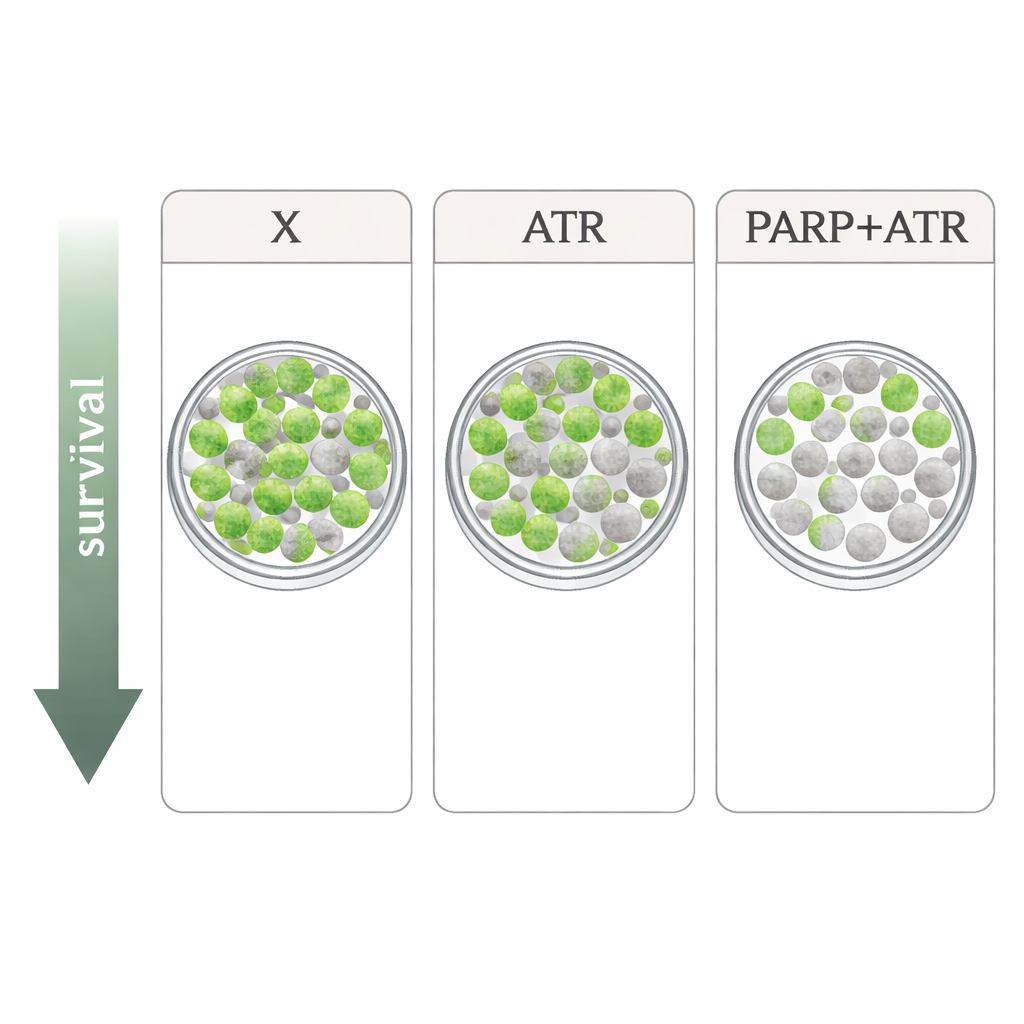
研究人员使用四种耐放射的 HPV 阴性头颈癌细胞系进行研究。他们将 xevinapant 与两种针对细胞 DNA 损伤响应的药物进行比较:ATR 抑制剂 tuvusertib 和 PARP 抑制剂 olaparib,剂量均接近患者可达水平。ATR 和 PARP 是在细胞受到 X 射线等损伤后帮助细胞暂停细胞周期并修复 DNA 的关键因子。在简单的增殖测试中,单药对细胞增殖的抑制仅是有限的,且不同细胞系表现不一。当在最严格的测定中——统计单个细胞是否还能长成克隆——将药物与放疗联合时,结果更为清晰:在若干细胞系中 xevinapant 仅表现出轻微或无额外的放射增敏作用,而 tuvusertib 和 olaparib 均持续地增强了放射致死性。影响最强的是同时抑制 ATR 和 PARP,这在四个细胞系中的三个显示出特别明显的克隆存活率下降。
细胞死亡信号并非全部
因为 xevinapant 的设计初衷是触发细胞死亡,研究组还测量了处理后(有无放疗)细胞出现凋亡或裂解的数量。在某些情形下——尤其是在名为 HSC4 的一株细胞系和药物联合时——这些死亡标志明显增加,但并不能可靠地与放疗对长期存活的抑制程度相对应。换言之,短期的死亡读数并不能良好预测真实的放射增敏效果。这一不一致强调了药物开发的一个关键教训:只有持续观察足够长时间以确定细胞能否重新生长的测定——例如克隆形成试验——才能恰当地评估放射增敏剂是否有效。
对未来治疗的启示
从这些体外实验来看,xevinapant 确实在某种程度上能增强 HPV 阴性头颈癌细胞对放疗的敏感性,但其效果比直接干扰 DNA 损伤处理的 ATR 和 PARP 抑制策略更弱且不够一致。将 ATR 和 PARP 抑制剂配合使用产生了最强的效果,提示在谨慎剂量设计下,这类药物与放疗的组合可能比继续推进 xevinapant 更有前景,至少对这种癌型而言。将这些发现转化到临床并不简单,因为此类药物同样会对正常的快增殖组织造成压力,早期试验中已需要降低剂量。不过,这项工作仍然将临床医生和研究者的注意力引向以 DNA 修复为靶的策略,作为更有说服力的候选,以期使放疗更有效,并可能为无法接受标准化疗的患者带来更安全的选择。
引用: Roehrle, J., Perugachi-Heinsohn, A., Gatzemeier, F. et al. Comparing and combining xevinapant with ATR and PARP inhibition for the radiosensitization of HPV-negative HNSCC cells. Sci Rep 16, 5882 (2026). https://doi.org/10.1038/s41598-026-38550-3
关键词: 头颈部癌症, 放射治疗, DNA 修复抑制剂, xevinapant, 放射增敏