Clear Sky Science · zh
高脂饮食诱导的代谢相关性脂肪肝疾病中的FK506结合蛋白-5
这项研究为何与日常健康相关
许多人担心长期高脂饮食如何损害肝脏和整体代谢,导致脂肪肝和2型糖尿病等疾病。本研究关注一种与应激相关的蛋白FKBP5,并展示了它如何出人意料地将我们的饮食、肠道细菌和肝脏健康联系起来。研究表明阻断该蛋白可以保护小鼠免受脂肪肝和肥胖的影响,这一发现提示可通过作用于基因与肠道微生物来预防饮食相关的肝损伤。
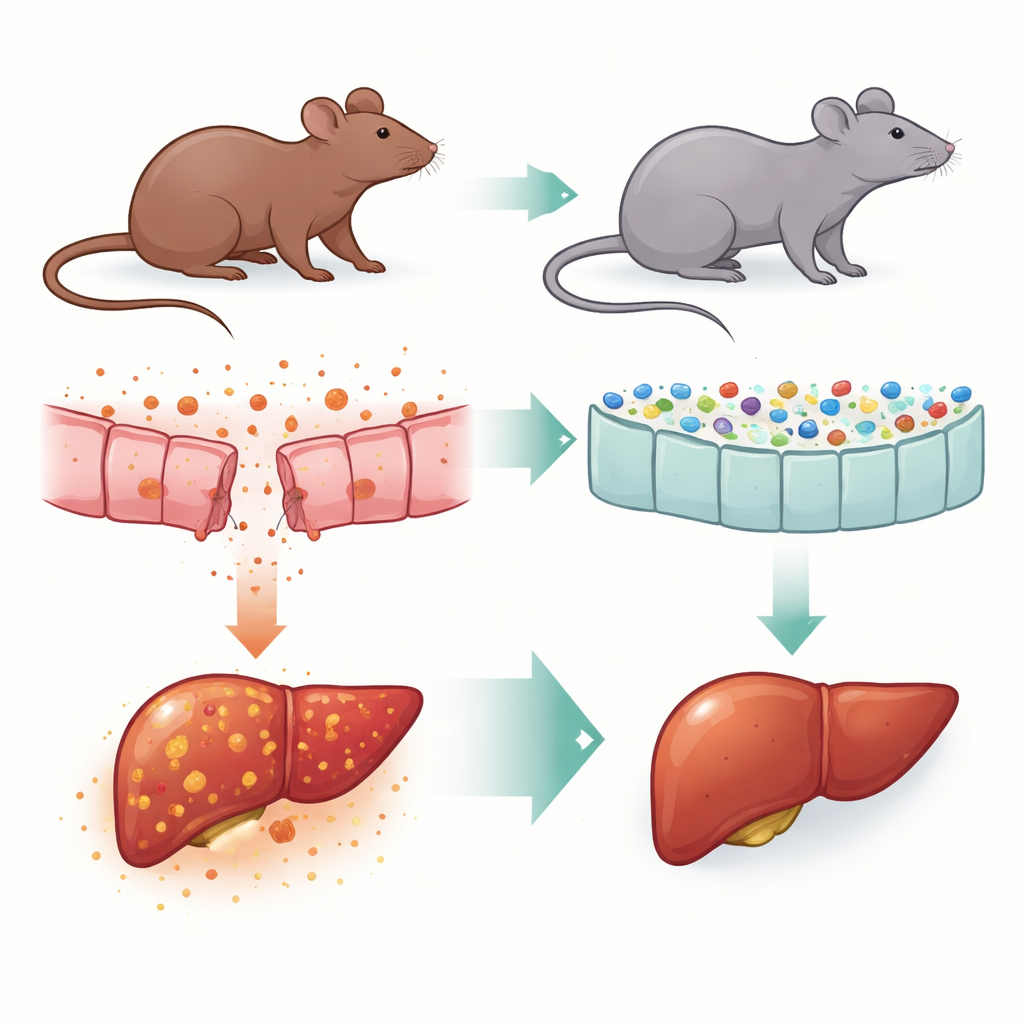
从高脂饮食到肝脏病变
当动物(以及人)长期摄入高脂饮食时,常会体重增加、肝脏脂肪堆积并且血糖调控恶化。研究者比较了正常小鼠与基因改造缺失FKBP5的小鼠,并让两组分别喂以常规饲料或高脂饮食16周。正常小鼠在高脂饮食下体重增加、血液和肝脏脂肪增多,并表现出更高的肝损伤标志。而缺失FKBP5的小鼠保持更瘦、肝脏和血脂更低、葡萄糖耐受性更好,且肝纤维化和炎症迹象更少。组织学上它们的肝脏脂肪含量更低,并且驱动脂肪储存、组织硬化和炎性损伤的基因表达较少。
肠道细菌与肠壁:关键的把关者
研究团队接着探究为何缺失FKBP5具有强烈保护作用。他们关注肠道微生物群——肠内庞大的细菌群落——以及将这些微生物与血液分隔开的薄肠壁。通过基于基因的细菌群落调查,他们发现高脂饮食使正常小鼠的肠道细菌发生变化,呈现与肥胖和肝病相关的模式,包括两大类群Firmicutes与Bacteroidetes之间平衡的变化。然而,缺失FKBP5的小鼠显示出一种不同的细菌谱系,这种谱系对高脂诱导的扰动更具抵抗力,并富含与瘦体型和有益代谢产物(如丁酸)相关的细菌群体。
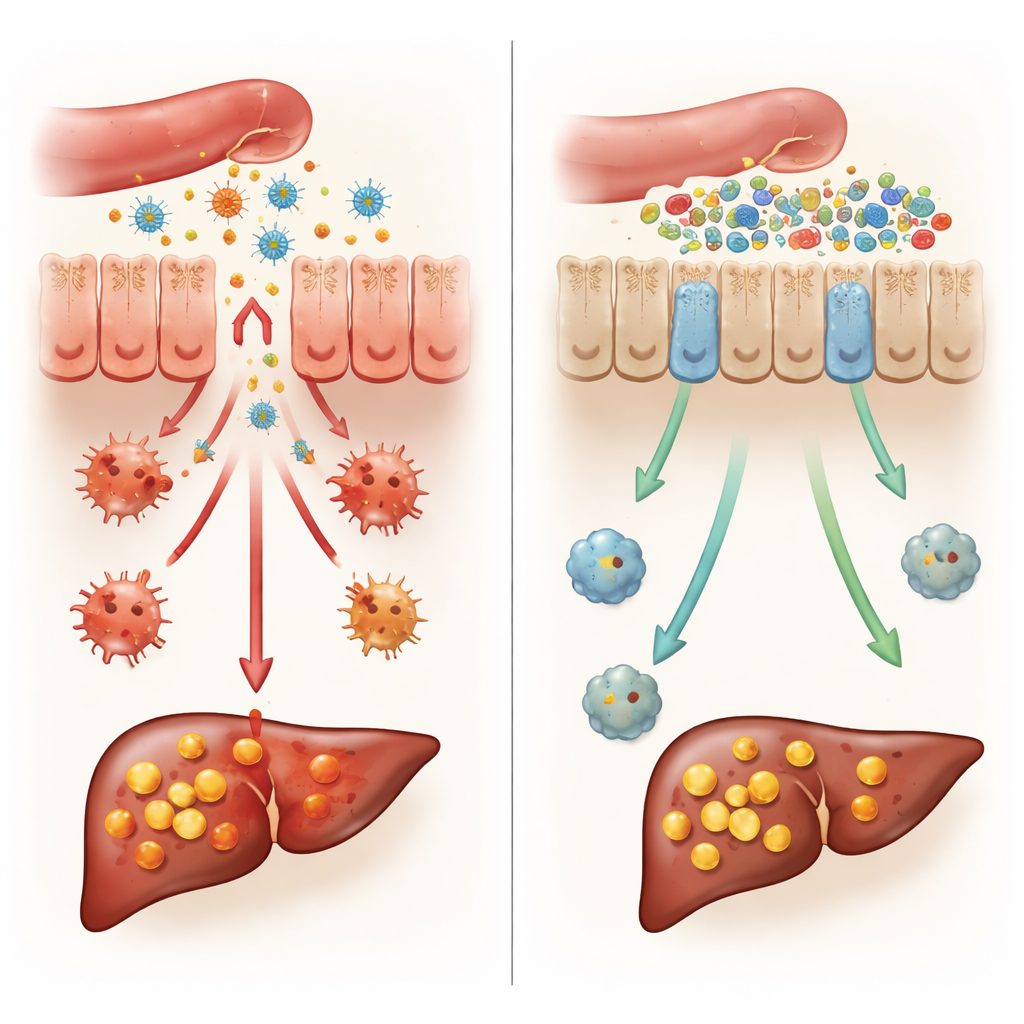
保持肠屏障紧密并抑制免疫反应
高脂饮食常削弱肠道屏障,使细菌组分渗入血液并到达肝脏,引发慢性炎症。在高脂饮食下的正常小鼠中,研究者观察到肠道更易渗漏、产生黏液的杯状细胞减少,以及通常将相邻肠细胞封闭的“紧密连接”受损。而在缺失FKBP5的小鼠中,这些有害变化在很大程度上被阻止:肠屏障保持更紧密,杯状细胞更多,示踪染料从肠道进入血液的通透性明显降低。与此同时,FKBP5缺失小鼠在肠道和肝脏中表现出更少的炎性免疫细胞和较低水平的炎性分子,表明更平静的免疫环境与更好的屏障功能并存。
益生菌作为辅助手段
鉴于一些有益细菌因高脂饮食而减少,研究者测试了一种商业益生菌混合制剂VSL#3是否能进一步改善结果。向高脂喂养的小鼠给予VSL#3可降低体重增加、改善血糖控制、增强肠道屏障,并减少肝损伤和炎症的标志物。接受益生菌处理的小鼠肠道细菌多样性更丰富,循环中与慢性低度炎症相关的免疫细胞更少。值得注意的是,这些益处在正常小鼠和FKBP5缺失小鼠中均可见,表明增强有益微生物和加固肠道屏障可以补充FKBP5缺失所提供的遗传性保护。
对未来治疗的意义
总体而言,这项研究将FKBP5描绘为一个关键开关,将应激通路、肠道微生物、肠道屏障与高脂饮食下的肝脏健康相连。去除小鼠体内的FKBP5改变了肠道微生物、保护了肠壁完整性、降低了有害的免疫细胞活动,并使肝脏免受脂肪堆积与纤维化侵害。尽管仍需更多研究在人体中验证这些发现,但结果提示阻断FKBP5的药物,结合以微生物组为靶的策略(如益生菌),未来可能成为预防或治疗由不健康饮食驱动的脂肪肝及相关代谢疾病的新方法。
引用: Wu, LL., Liao, YJ., Peng, WH. et al. FK506-binding protein-5 in high-fat diet-induced metabolic dysfunction-associated steatotic liver disease. Sci Rep 16, 9241 (2026). https://doi.org/10.1038/s41598-026-38549-w
关键词: 脂肪肝疾病, 肠道微生物组, 高脂饮食, 益生菌, 代谢综合征