Clear Sky Science · zh
用非羟肟酸[1,2,4]三唑并[4,3-a]喹啉化合物实现HDAC8的靶向抑制
给儿童癌症带来新希望
神经母细胞瘤是一种起源于神经细胞的侵袭性儿童癌症,一旦发生转移通常难以治疗。本研究探讨了一种通过关闭名为HDAC8的关键细胞开关来减缓或杀死神经母细胞瘤细胞的新方法。研究人员构建了一类新型类似药物的分子,能对该开关极具选择性,目标是开发既能更有效抑制肿瘤又对机体其他部分更温和的治疗方案。
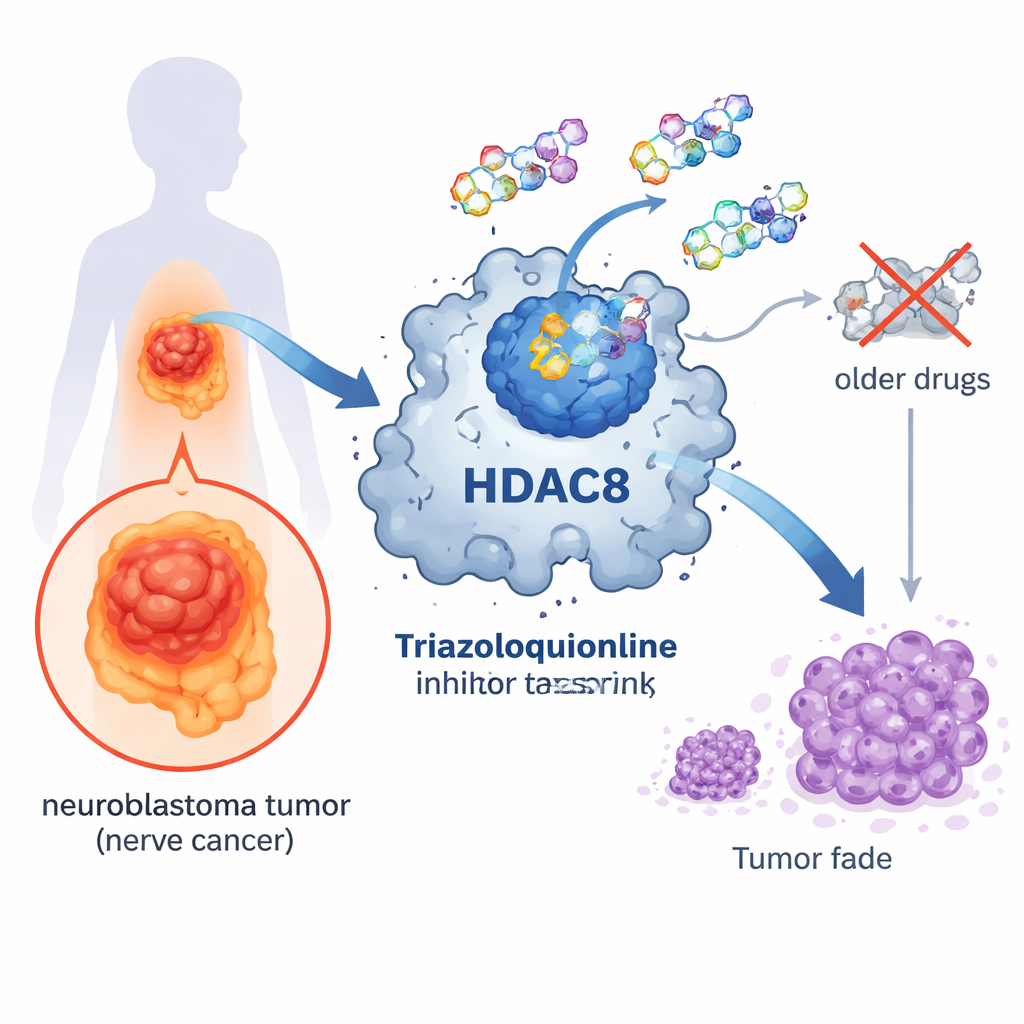
位于癌症核心的分子开关
在细胞内,基因不断被开启或关闭。其中一项重要的调控机制依赖于附着在与DNA相关蛋白上的微小化学标记——乙酰基。组蛋白去乙酰酶(HDAC)类酶会移除这些标记,使DNA的包装更紧密,通常会降低基因活性。HDAC8是该酶家族的一个成员,并与多种癌症(包括神经母细胞瘤)有关。当HDAC8过度活跃时,癌细胞更容易生长、存活并扩散,因此它成为开发新药的有吸引力的靶点。
旧有HDAC药物的局限性
已有若干阻断HDAC的药物获批用于某些血液癌,但它们往往同时作用于多种HDAC类型。大多数此类药物使用羟肟酸基团与酶活性位点中的金属离子结合。尽管有效,但该基团对金属的结合非常强,这可能导致副作用并限制药物区分不同HDAC的精确性。因此,患者可能出现毒性反应,正常细胞也会受到损害。研究人员一直在寻找替代的化学设计,以在保留抗癌效果的同时减少不良影响。
设计新型靶向抑制剂类别
在这项工作中,团队设计并合成了21种以三唑喹啉为骨架的新化合物,通过一段柔性连接体连接到可与HDAC8活性位点中锌原子结合的“α-氨基酰胺”区域。借助计算机引导的设计,他们选择了这种结构以契合HDAC8特有的狭窄“乙酸盐释放通道”,这一结构特征有助于实现高度选择性。详细的对接研究和分子动力学模拟显示,若干新分子——尤其是被称为9m和9r的化合物——在HDAC8口袋内形成稳定、持久的相互作用,其结合强度与或优于一已知参考抑制剂。重要的是,生化测试证实,最佳化合物能强效抑制HDAC8,同时对其他HDAC家族成员几乎不受影响。
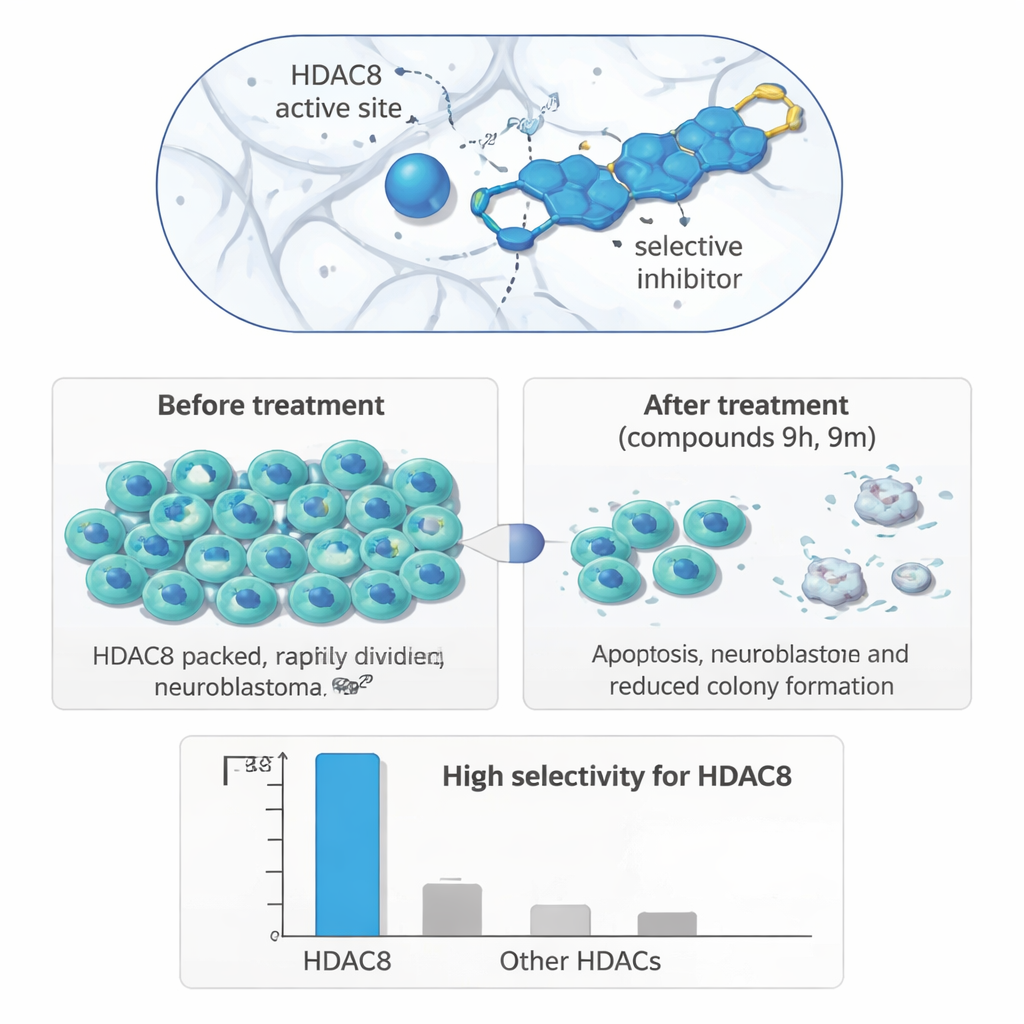
从试管到肿瘤细胞
为评估这种精准酶抑制能否转化为有用的生物学效应,研究人员在一系列人类细胞系上测试了这些化合物。在神经母细胞瘤细胞系(IMR‑32)中,两种分子9h和9m表现尤其突出:它们在微摩尔浓度下能明显抑制细胞生长,并且对神经母细胞瘤的作用强于对乳腺或结肠癌细胞或非癌性肾细胞的作用。长期克隆形成实验显示,处理过的神经母细胞瘤细胞在药物暴露后失去了大量再生能力。在划痕愈合实验(用于追踪细胞填补细胞层中划痕的速度)中,两种化合物均减缓了神经母细胞瘤细胞的迁移,提示其转移潜能可能降低。
探究这些化合物如何杀死癌细胞
流式细胞术实验显示,9h和9m在神经母细胞瘤细胞中诱导程序性细胞死亡(凋亡),并导致细胞在与DNA损伤或细胞死亡相关的细胞周期阶段(Sub‑G1)积累。为确认这些效应确由HDAC8阻滞引起,团队测量了称为SMC3的蛋白的乙酰化状态,SMC3是已知的HDAC8靶标,参与保持姐妹染色体在细胞分裂时配对。当HDAC8被抑制时,乙酰化的SMC3会累积。用9h或9m处理后,乙酰化SMC3水平显著上升,而SMC3总量保持不变——这强烈证明这些化合物在活细胞中直接作用于HDAC8并干扰其在染色体控制中的正常功能。
这对未来治疗的潜在意义
综上所述,化学合成、计算建模、酶学测试和基于细胞的实验共同描绘出一致的图景:新开发的三唑喹啉化合物是强效且高度选择性的HDAC8抑制剂,能抑制神经母细胞瘤细胞的生长与扩散,同时较少影响其他HDAC酶。由于它们避开了传统的羟肟酸基团,可能为利用HDAC8作为治疗靶点提供更安全的途径。尽管仍需大量工作——尤其是动物研究和最终的临床试验——但这项研究为开发针对儿童神经母细胞瘤以及可能由HDAC8驱动的其他疾病的更精确药物奠定了坚实基础。
引用: Bandaru, N.V.M.R., Fathima, A., Sengar, S. et al. Targeted HDAC8 inhibition with non-hydroxamate [1,2,4]triazolo[4,3-a] quinoline compounds. Sci Rep 16, 7472 (2026). https://doi.org/10.1038/s41598-026-38490-y
关键词: HDAC8 抑制剂, 神经母细胞瘤, 表观遗传疗法, 三唑喹啉, 靶向抗癌药物