Clear Sky Science · zh
GluN2A介导的电流与人源iPSC衍生神经元内的钙信号
为什么这些在实验室培育的小脑细胞很重要
科学家越来越多地使用实验室培养的人类脑细胞来研究我们大脑如何发育,以及探究自闭症、癫痫和阿尔茨海默病等病症中出现的问题。本研究提出了一个简单但关键的问题:这些实验室制造的神经元是否以真正类似人脑的方式成熟并建立连接,尤其是在处理一种名为谷氨酸的关键化学信号时?答案揭示了如何构建更真实的“迷你大脑”模型,并为检查大脑健康与疾病提供了新的途径。
从重编程细胞构建神经元
研究者以人类诱导多能干细胞为起点——即被“重编程”回干细胞状态的普通细胞。从那里,他们将细胞推动分化为神经前体细胞,最终形成由神经元和支持性星形胶质细胞组成的网络,模拟发育中的人类皮层。他们比较了两种广泛使用的培养配方(培养条件)。一种称为 BrainPhys 培养基,旨在促进活跃、对电刺激有反应的神经元,并倾向产生更多星形胶质细胞。另一种是更传统的神经维持培养基,偏向产生星形胶质细胞较少的神经元。在六十天内,团队跟踪了这些培养物在外观、基因活动和细胞类型上的变化,发现使用 BrainPhys 的培养物生成了更复杂的神经元形态,并且神经元与星形胶质细胞的比例更接近真实人脑。
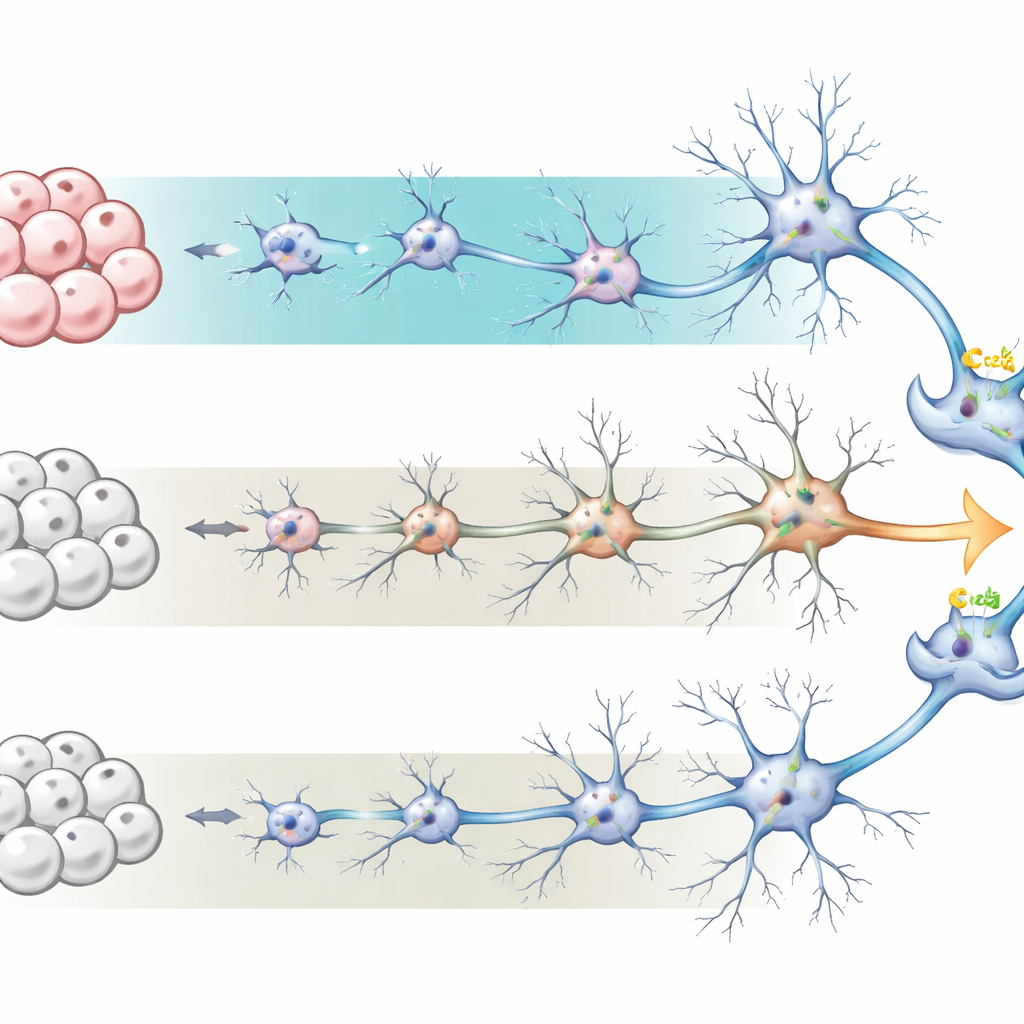
细胞成熟的迹象
为了评估神经元的“成熟”程度,团队在第60天利用RNA测序测量了全局基因表达。与标准培养基相比,BrainPhys 培养的细胞有将近两千个基因表达水平不同,其中许多与神经元分化、突触形成和电活动相关。与星形胶质细胞功能和炎症相关的基因也更高,反映了更大的星形胶质细胞群体。这些模式共同表明,BrainPhys 培养物更能重现大脑发育的晚期阶段,具有更精细的神经元间通信点和更接近生物组织的支持性环境。
化学通讯中的关键转换
大脑成熟的一个标志是NMDA受体组成的变化——NMDA受体是神经元上的分子门,当它们对谷氨酸开放时,帮助建立与学习相关的连接。在发育早期,一种称为 GluN2B 的亚基占主导;随后 GluN2A 接替,改变受体开放的持续时间和强度。通过显微镜观察,团队显示随时间推移越来越多的 NMDA 受体迁移到突触——神经元之间的接触点,尤其是在 BrainPhys 培养物中。针对性的基因测量显示“早期”GluN2B 亚基下降而“后期”GluN2A 亚基上升,表明神经元正在经历这一典型的发育转换。
追踪细胞内的电流和钙信号
功能性检测证实了这些分子变化的重要性。研究者用细尖电极记录了由 NMDA(一种选择性激活 NMDA 受体的药物)触发的电流。两种培养方法的神经元都显示出强烈的电流,但阻断 GluN2A 亚基会将这些电流大约减半,证明 GluN2A 现已成为信号传导中的主要成分。随后团队使用荧光染料追踪钙——一种关键的细胞内信使。暴露于 NMDA 时,BrainPhys 培养的神经元中有更大比例出现强烈的钙激增,且信号幅度更大。基因分析提示了原因:BrainPhys 培养物上调了多种钙通道和钙释放通路的组成部分,使细胞能够将 NMDA 受体的激活转化为广泛且协调的钙信号。
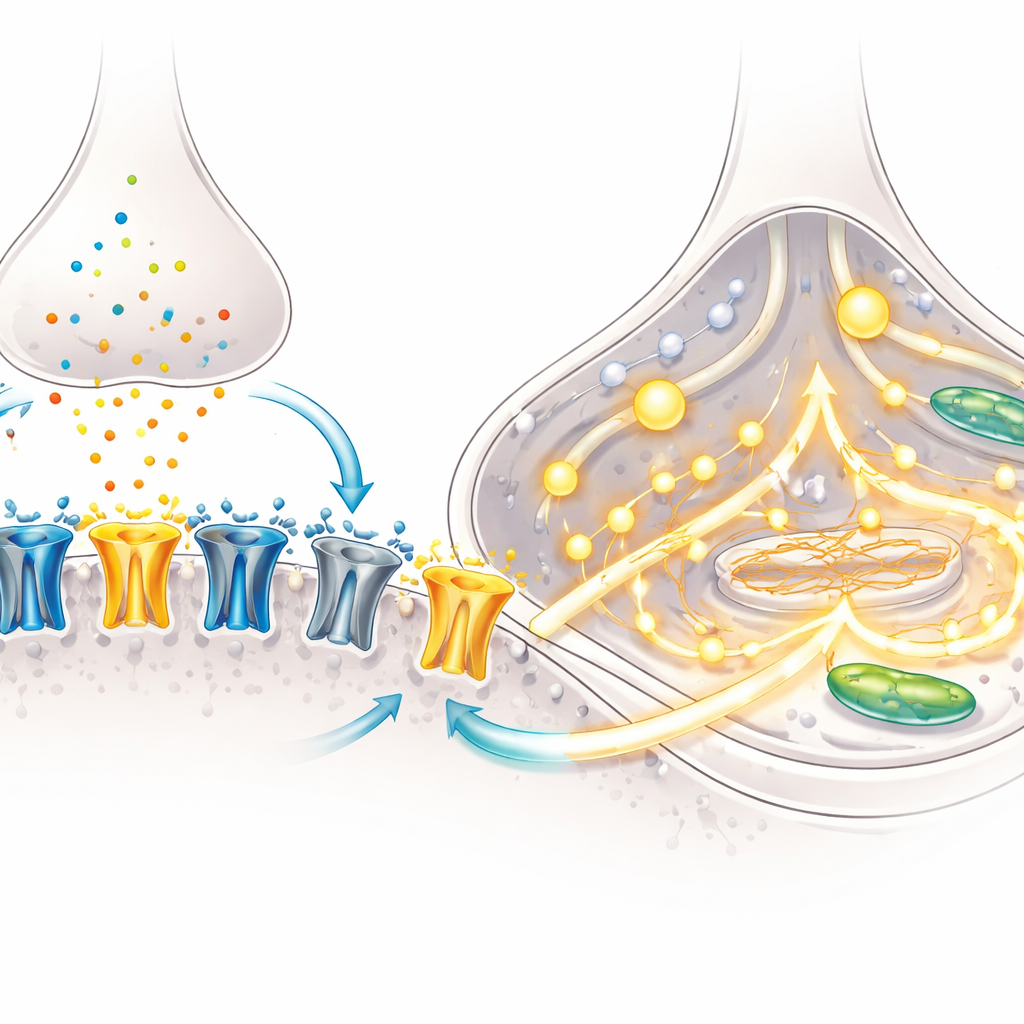
这对研究脑疾病意味着什么
总体而言,这些发现表明人类干细胞衍生的神经元在仅两个月内就能达到功能性成熟状态,尤其是在支持活跃网络和真实神经元—星形胶质细胞组合的培养条件下。在这种状态中,“类成体”的 GluN2A 亚基在 NMDA 受体电流中占主导并强烈参与钙信号传导,这与发育中人类大脑的表现类似。对非专业读者来说,结论是研究者现在拥有一个更忠实的体外模型,用于研究人类兴奋性神经元如何成熟、如何建立连接以及如何对谷氨酸作出反应。这使得探究微小基因变异或疾病过程如何破坏这些精细调节机制成为可能,为从癫痫到阿尔茨海默病等多种病症提供观察窗口,并为未来疗法的设计与测试提供指导。
引用: Escamilla, S., Avilés-Granados, C., Peralta, F.A. et al. GluN2A-mediated currents and calcium signal in human iPSC-derived neurons. Sci Rep 16, 9736 (2026). https://doi.org/10.1038/s41598-026-38482-y
关键词: NMDA 受体, 干细胞神经元, 大脑发育, 钙信号传导, 突触成熟