Clear Sky Science · zh
双重G9a抑制剂兼组胺H3受体拮抗剂A-366在BTBR T + tf/J小鼠中改善重复和社交行为并减轻神经炎症
这项小鼠研究为何与自闭症相关
与自闭谱系障碍(ASD)共同生活的家庭常面临零散的治疗选择,这些治疗通常一次只能缓解少数症状。本研究探讨了一种新的实验性化合物A-366,该化合物被设计为同时作用于两种截然不同的生物系统。在一种广泛使用的类自闭行为小鼠模型中,A-366减少了重复行为、改善了社交互动并抑制了脑内炎症,提示未来可能出现一种药物能够同时应对ASD的若干核心特征。
一个由多重因素构成的状况
ASD并非单一疾病或由单一因素引起。它表现为社交沟通困难、重复行为,以及常伴的焦虑或注意力问题等其他挑战。在这些外在表现之下,是一系列牵扯脑内化学物质与基因调控改变的复杂网络。现有药物,如抗精神病药阿立哌唑,主要作用于多巴胺和血清素等脑内信使系统,并仅获批用于治疗如易激惹等相关症状。与此同时,研究表明,脑细胞内DNA的包装和化学标记方式——即表观遗传学——在ASD中也发生变化,脑内免疫与炎症反应的活性也有异常。这些多重层面表明,“每次只针对一个靶点”的策略可能过于狭隘。
同时打击基因开关和脑内信使
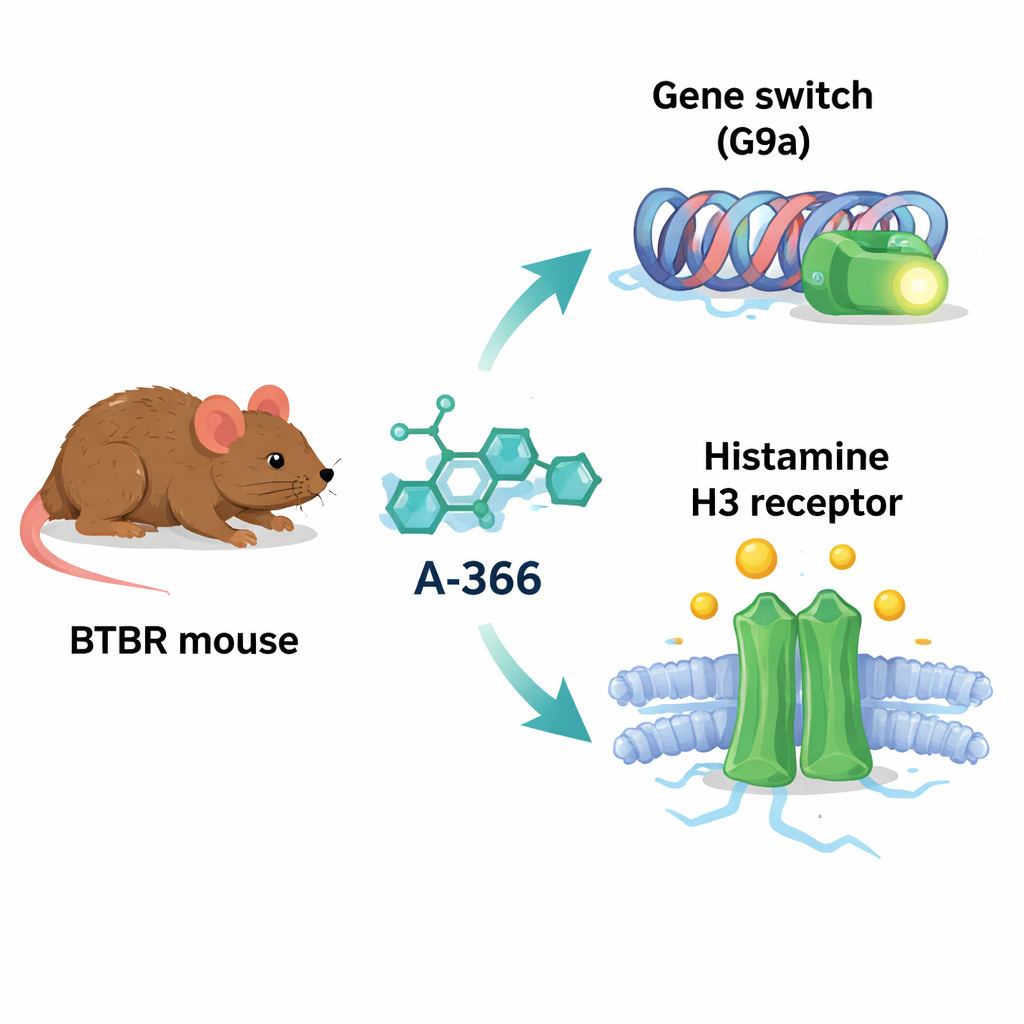
A-366最初被开发为阻断名为G9a的蛋白,这是一种向组蛋白添加化学标记并往往使基因表达下降的酶。在若干脑疾病中,G9a的活性及其留下的标记增加,可能抑制对学习、记忆和健康脑回路至关重要的基因。有意思的是,A-366的化学构型也类似于阻断组胺H3受体的药物,H3受体是控制组胺及其它递质释放的开关,已与注意力、觉醒和社交行为相关。基于这一重合,作者猜测A-366可能充当一种“双重作用剂”:通过抑制G9a来减轻有害的基因沉默,同时通过阻断H3受体来增强组胺信号传导。
在类自闭小鼠中检验A-366
研究团队使用了BTBR T+tf/J小鼠,这一品系天生表现出社交性低、强烈的重复梳理与挖掘行为以及升高的脑内炎症——这些特征呼应了ASD的关键方面。雄性BTBR小鼠每天接受三周的A-366注射,分为三种不同剂量,并将其行为与典型的C57小鼠以及接受pitolisant(常用H3受体阻断剂)或阿立哌唑处理的BTBR小鼠进行比较。在多个行为任务中,A-366以剂量依赖的方式减少了重复的挖掘、撕扯和自我梳理,并改善了Y迷宫空间工作记忆测试的表现。在三腔社交测试中,A-366不仅恢复了小鼠与另一只小鼠相比空笼子更愿意待在一起的偏好,而且在最高剂量下将社交评分提高到典型小鼠的水平,且效果超过了pitolisant和阿立哌唑。
抑制炎症并验证作用靶点
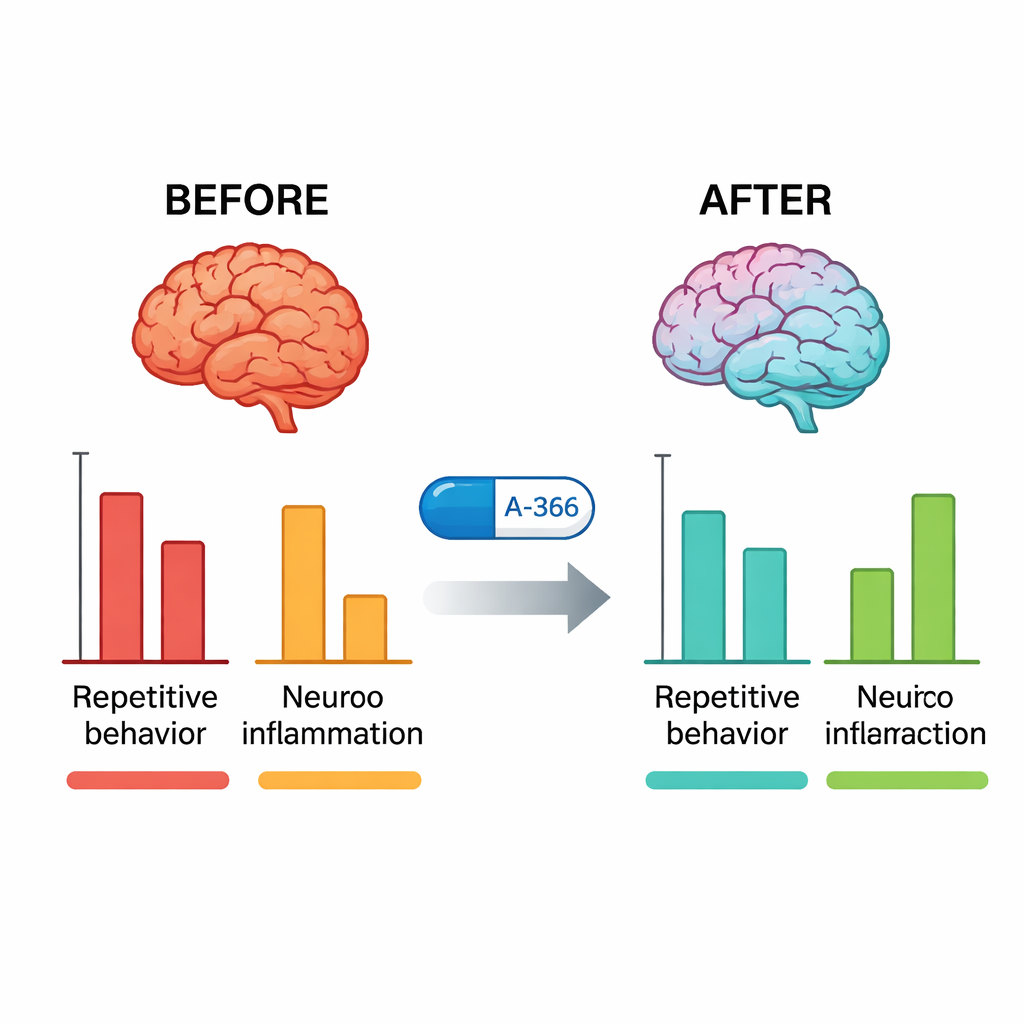
在行为学测试之后,研究者检查了小鼠的大脑。未经处理的BTBR小鼠在海马和小脑中的G9a活性明显高于典型小鼠。A-366处理显著降低了这种活性并趋于正常,而单用pitolisant则没有这种效果,证实A-366确实作用于其表观遗传学靶点。与此同时,关键炎症分子——TNF-α、IL-6和IL-1β——在BTBR小鼠中显著升高,A-366能显著降低这些水平,其效果优于阿立哌唑。当科学家在A-366基础上加入激活H3受体的药物(RAMH)时,行为学和抗炎益处只有部分被逆转,而G9a活性的下降仍然存在。该模式支持一种联合机制:通过G9a抑制提供稳定的表观遗传缓解,同时通过阻断H3受体带来组胺介导的贡献。
这对未来治疗可能意味着什么
对非专业读者来说,这些发现表明有可能设计同时作用于大脑“软件”和“信息传递系统”的药物。在这个类自闭行为的小鼠模型中,A-366通过同时减轻有害的基因关闭和调整组胺信号,缓解了重复行为、改善了社交参与并减少了慢性脑炎症的迹象。A-366本身最初为其他疾病开发,若用于人体还需优化和广泛的安全性测试。不过,它为一种针对ASD复杂生物学的新型多靶向药物提供了蓝图——在这一领域,仅针对单一通路的做法迄今收效有限。
引用: Hajar, M., Jayaprakash, P., Stark, H. et al. The dual G9a inhibitor and histamine H3 receptor antagonist A-366 improves repetitive and social behaviors and attenuates neuroinflammation in BTBR T + tf/J mice. Sci Rep 16, 7105 (2026). https://doi.org/10.1038/s41598-026-38481-z
关键词: 自闭谱系障碍, 表观遗传疗法, 组胺H3受体, 神经炎症, 小鼠模型