Clear Sky Science · zh
aFGF通过调节SIRT1/STAT3通路拯救高糖诱导的衰老成纤维细胞并改善糖尿病性伤口愈合
为什么慢愈合的伤口很重要
对于许多糖尿病患者来说,脚或腿上的小割伤可能变成顽固的溃疡,持续数月,有时导致感染甚至截肢。这些慢性溃疡并非仅是表面问题:本应重建受损组织的皮肤细胞常常提前衰老并失去正常功能。本研究探讨了一种有前景的方法,利用一种天然存在的修复信号“回春”部分细胞,目标是帮助糖尿病伤口更快、更完整地闭合。
过早衰老的细胞
健康皮肤依赖成纤维细胞——存在于真皮深层的支持细胞——增殖、迁移到伤口处并铺设新的基质以重建组织。在糖尿病中,长期高血糖和糖化产物促使这些成纤维细胞进入一种称为细胞衰老或衰老表型的状态。衰老的成纤维细胞不再良好分裂,产生较少用于修复的结构蛋白,反而分泌一系列促炎因子,助长持续的炎症。作者在糖尿病大鼠中发现,伤口周围皮肤含有更多这类衰老的成纤维细胞和更少有利的基质蛋白,这与愈合明显变慢相关。
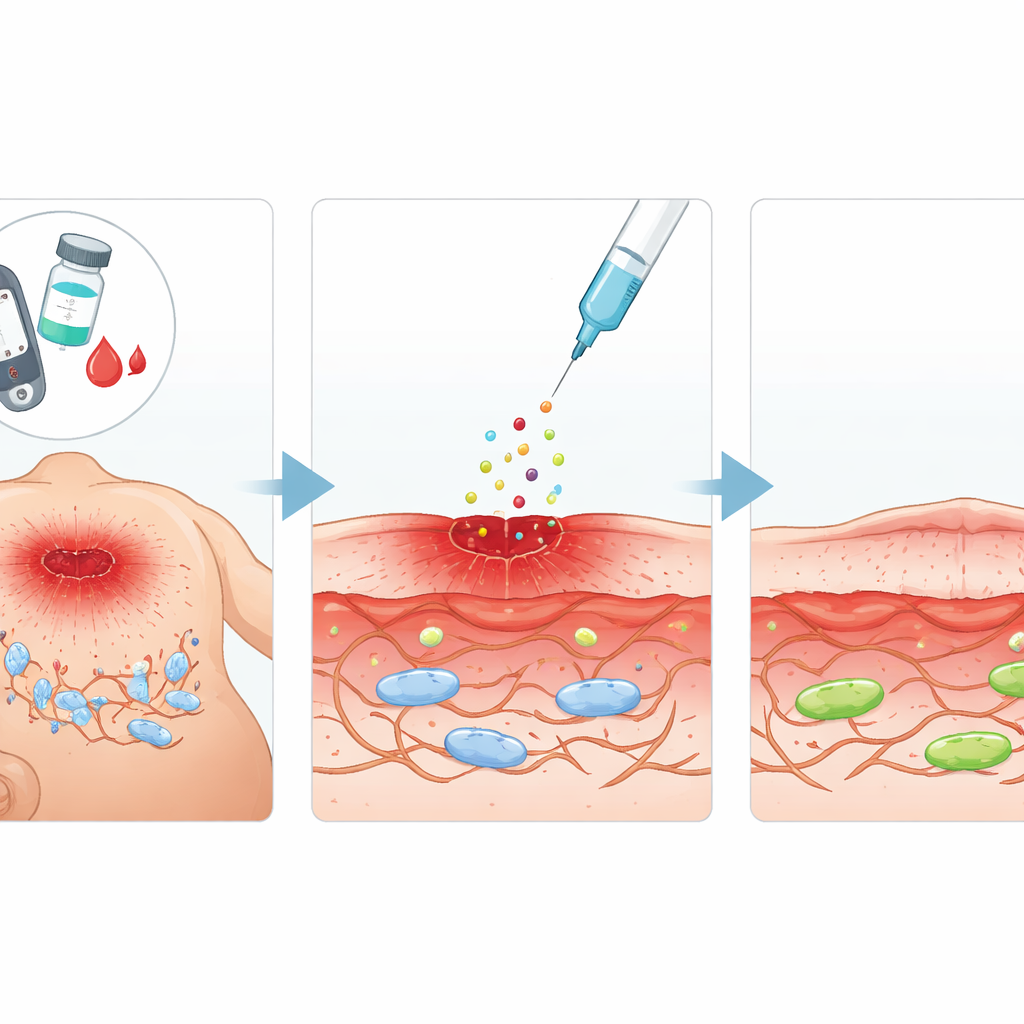
一种有希望的修复信号
研究团队聚焦于酸性成纤维细胞生长因子(aFGF),这是一种天然存在的蛋白,已知能促进细胞生长和组织修复。他们想知道aFGF是否不仅能增强成纤维细胞活性,还能逆转高糖导致的类衰老改变。在糖尿病大鼠中,他们制作了标准化皮肤伤口,并每隔几天在受伤区域周围注射aFGF。与未处理的糖尿病动物相比,接受aFGF处理的大鼠显示伤口面积收缩更快、基底组织重建更好以及细胞衰老标志物水平更低。在并行的体外实验中,使用暴露于极高葡萄糖的鼠源成纤维细胞系,aFGF恢复了细胞的分裂和迁移能力——这两种行为对伤口闭合至关重要。
平抑细胞内的氧化应激
高血糖不仅为细胞提供更多“燃料”:它还推动活性氧(ROS)等不稳定分子的过度产生,这些分子会损伤蛋白质、脂类和DNA。氧化应激是促使成纤维细胞进入衰老的主要触发因素。研究者在细胞模型中测量了几种相关的标准指标,包括有害副产物和细胞自身抗氧化酶的活性。在高糖条件下,成纤维细胞表现出更多损伤和较弱的抗氧化防御。加入aFGF后,这一平衡发生了转变:有害标志物下降,保护性酶活性增强。这表明aFGF有助于恢复更健康的细胞内环境,降低成纤维细胞陷入永久性衰老状态的可能性。
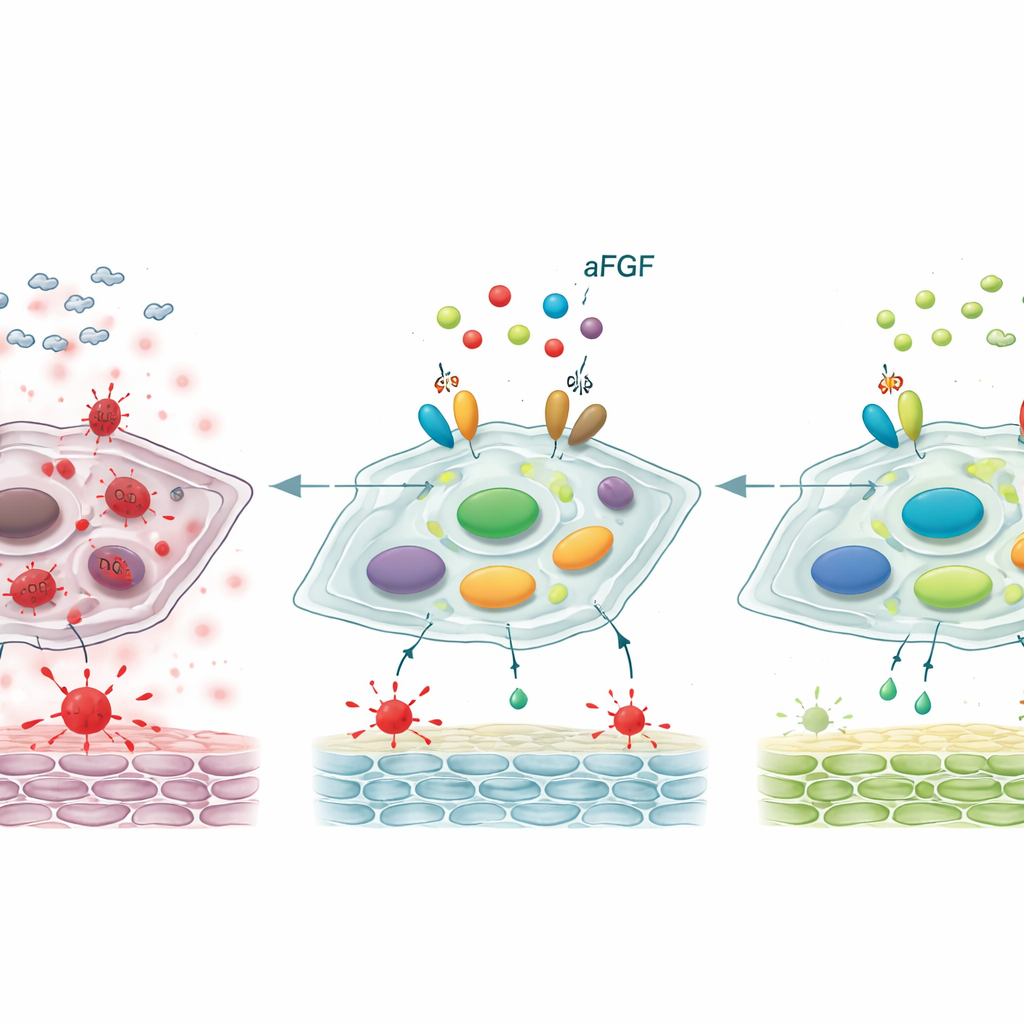
重置一个关键的控制开关
更深入地,科学家们考察了涉及两种蛋白SIRT1和STAT3的分子控制轴,这两者共同影响成纤维细胞是保持年轻态还是转为衰老。在糖尿病伤口和高糖处理的细胞中,与应对应激相关的保护因子SIRT1水平下降,而被激活的STAT3形式——一个驱动衰老和促炎行为的因子——则升高。aFGF处理扭转了这一模式:SIRT1上升,活化的STAT3下降。当研究团队用特异性抑制剂阻断SIRT1时,aFGF降低氧化应激、抑制衰老标志并加速大鼠伤口愈合的能力在很大程度上丧失。这表明aFGF的有益作用在很大程度上依赖于唤醒SIRT1,而SIRT1进而抑制STAT3及其控制的有害衰老程序。
这对患者意味着什么
综合来看,研究结果表明aFGF不仅仅是推动细胞生长。它似乎能将糖尿病伤口中过度劳损的成纤维细胞从破坏性的衰老循环中解救出来,减轻氧化应激并重置关键分子开关,使这些细胞能够再次参与组织重建。尽管该工作是在大鼠和培养细胞中完成的,真人人类的糖尿病伤口比这些模型更复杂,但结果显示aFGF是未来治疗的有希望候选者。如果在人类中能确认类似益处,经过精确给药的aFGF疗法有朝一日可能帮助慢性糖尿病溃疡更快愈合,减轻疼痛、降低感染风险并减少严重并发症的发生。
引用: Wang, X., Lu, M., Jia, S. et al. aFGF rescues high glucose-induced senescent fibroblasts and improves diabetic wound healing by regulating SIRT1/STAT3 pathway. Sci Rep 16, 7856 (2026). https://doi.org/10.1038/s41598-026-38480-0
关键词: 糖尿病伤口愈合, 成纤维细胞衰老, 氧化应激, 生长因子治疗, SIRT1 STAT3通路