Clear Sky Science · zh
粘膜阿克曼氏菌通过抑制铁死亡信号通路影响结肠炎
为何这种微小肠道居民重要
像溃疡性结肠炎这类慢性胃肠疾病会把日常活动——进食、排便——变成痛苦的体验。临床上已经知道免疫系统和肠道微生物都参与其中,但许多细节仍在揭示中。本研究聚焦于一种特定细菌——粘膜阿克曼氏菌(Akkermansia muciniphila),提出了一个简单却关键的问题:这种微生物能否通过阻止一种由铁驱动的细胞损伤形式来保护肠道?答案可能为炎症性肠病带来基于细菌的新型治疗思路。
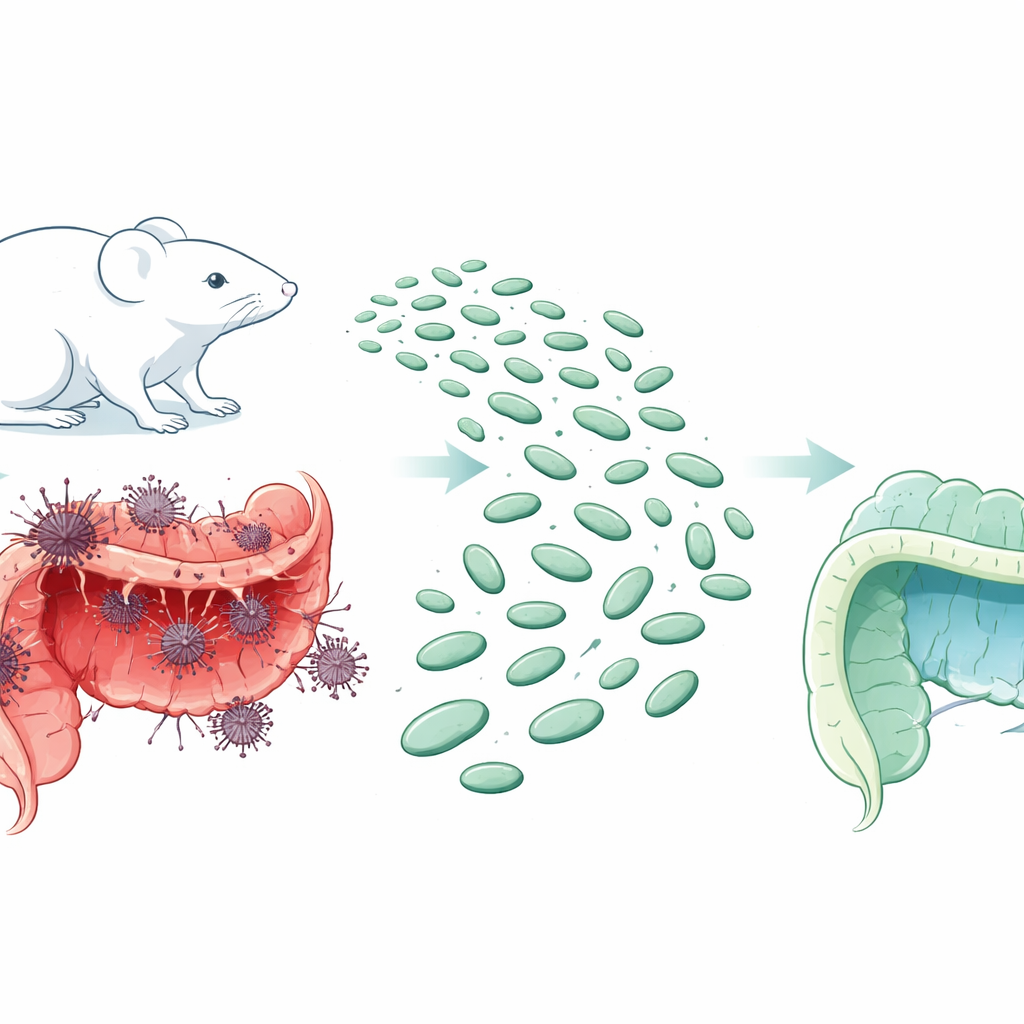
受攻击的脆弱内壁
结肠炎以大肠的肿胀和损伤为特征。正常情况下,内壁由紧密排列的细胞和分泌粘液的杯状细胞覆盖,但在病变中会被侵蚀并出现通透性增加。在这项小鼠研究中,研究者用一种化学物质诱发结肠炎,该模型模拟了人类疾病的多种特征:体重下降、腹泻、出血以及结肠黏膜的广泛损伤。显微检查显示组织层变薄、指状绒毛丧失、杯状细胞减少以及炎性细胞大量浸润——这些都是肠道屏障失衡的迹象。
由铁驱动的细胞损伤作为潜在凶手
研究者关注“铁死亡”(ferroptosis),这是一种新近识别的细胞死亡形式,其中铁促进细胞膜中有毒氧化脂质的积累。在结肠炎模型中,他们发现氧化应激标志物水平升高,如活性氧和受损脂质的分解产物,同时结肠组织中铁含量过高。与此对应,通常保护细胞免受此类损伤的防护蛋白减少,而促使脂质损伤的蛋白则增多。当研究组给予小鼠一种特异性增强铁死亡的药物时,结肠损伤更加严重,表明由铁引发的膜损伤不仅存在,而且会促进结肠炎恶化。
有益细菌出手相助
通过对肠道微生物群的基因学调查,科学家观察到结肠炎时粘膜阿克曼氏菌的丰度显著下降。随后他们在数周内口服补充该细菌给部分结肠炎小鼠。接受处理的动物体重下降较少,粪便更成形、出血减少,组织染色显示结肠组织明显更健康。肠表面更完整,隐窝结构保存更好,肌层排列更有序。电子显微镜显示,经处理小鼠的线粒体外观更为正常,结构性塌陷的迹象减少。化学检测表明,补充阿克曼氏菌后,组织中的铁、活性氧及脂质损伤标志物下降,而对抗铁死亡的关键保护蛋白则回升。即便在给予增强铁死亡的药物时,阿克曼氏菌仍部分逆转了其对肠黏膜的不良影响。
肠道化学与基因的变化
为弄清该细菌如何发挥保护作用,研究组同时检测了结肠组织的基因表达和肠道中产生的小分子代谢物。结肠炎显著改变了数百个与炎症、代谢和细胞存活相关基因的活性。阿克曼氏菌处理使许多这些变化向正常方向回调,尤其是那些参与细胞黏附和应激反应的基因。在代谢方面,该菌增加了有益的短链脂肪酸和若干氨基酸相关化合物,同时减少了某些可刺激肠道的醇类和酚类。当研究者将基因和代谢物数据叠加分析时,发现有19条生物学通路被共同影响,其中许多与脂质处理和脂质过氧化有关——正是推动铁死亡的过程。这种模式表明,阿克曼氏菌通过重塑肠道化学环境和结肠对压力的基因响应,部分平息了结肠炎。
这对患者意味着什么
总体而言,研究表明恢复一种有益细菌可以通过强化肠道屏障并降低肠细胞内由铁引发的膜损伤来缓解小鼠的结肠炎。尽管这项工作仍处于动物和实验室阶段,但它指向了未来:有针对性的微生物或其代谢产物可能成为现有炎症性肠病药物的补充。通过抑制铁死亡并恢复更健康的肠道化学环境,这类方法有望保护脆弱的肠黏膜,减少慢性结肠炎患者的痛苦发作。
引用: Zhang, L., Liu, Y., Wei, K. et al. Akkermansia muciniphila affects colitis by inhibiting ferroptosis signaling pathway. Sci Rep 16, 9250 (2026). https://doi.org/10.1038/s41598-026-38452-4
关键词: 溃疡性结肠炎, 肠道微生物组, 粘膜阿克曼氏菌, 铁死亡, 肠道炎症