Clear Sky Science · zh
通过计算方法发现来源于天然化合物的多靶点抑制剂用于亨廷顿病治疗
对一种毁灭性脑疾病的新视角
亨廷顿病是一种罕见但毁灭性的脑部疾病,会逐步剥夺患者的运动能力、思维能力和独立生活能力。现有药物可以缓解部分症状,但不能阻止或逆转疾病进程。本研究探讨了一种新的计算驱动的寻找治疗方法的途径——寻找一种天然化合物,能够同时作用于疾病过程中的多个薄弱环节;这种策略可能比只针对单一靶点的药物更有效。
为何亨廷顿病难以治疗
亨廷顿病由基因缺陷引起,导致神经细胞逐步退化,通常在中年开始。早期患者可能注意到情绪细微变化、轻微的不自主运动或轻度的计划和注意力困难。在10到12年内,这些症状可能进展为严重的运动障碍、失语、痴呆以及完全依赖照护者。科学家知道亨廷顿病中脑细胞内有多种机制失衡——能量生成受损、有害蛋白质聚集、细胞间的化学信号变得有毒。由于多条通路同时被扰乱,“一蛋白一药”的策略难以带来真正的突破。
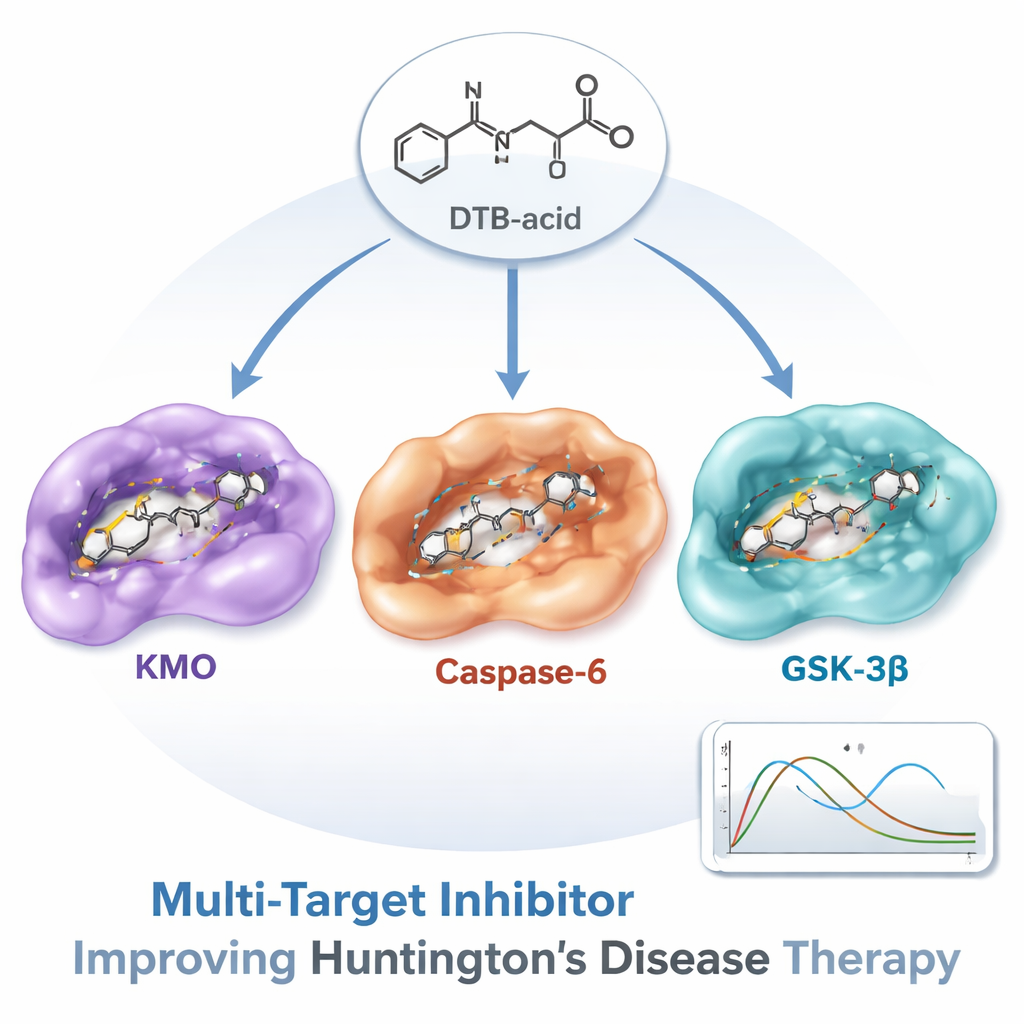
大脑中的三个关键压力点
研究人员聚焦于在亨廷顿病中位于关键控制点的三种蛋白。第一种KMO,调控色氨酸的分解方向,决定生成有毒或有保护作用的代谢产物;当平衡偏向有毒产物时,脑细胞受损。第二种半胱天冬酶-6(Caspase-6)会将突变的亨廷顿蛋白切割成更小且高度有毒的片段,这些片段在疾病早期积累。第三种GSK-3β是一种信号激酶,与异常蛋白缠结和多种脑疾病中的细胞死亡相关。研究团队希望找到一种能够同时抑制这三者有害活性的分子,从而设计出更贴合疾病复杂性的疗法。
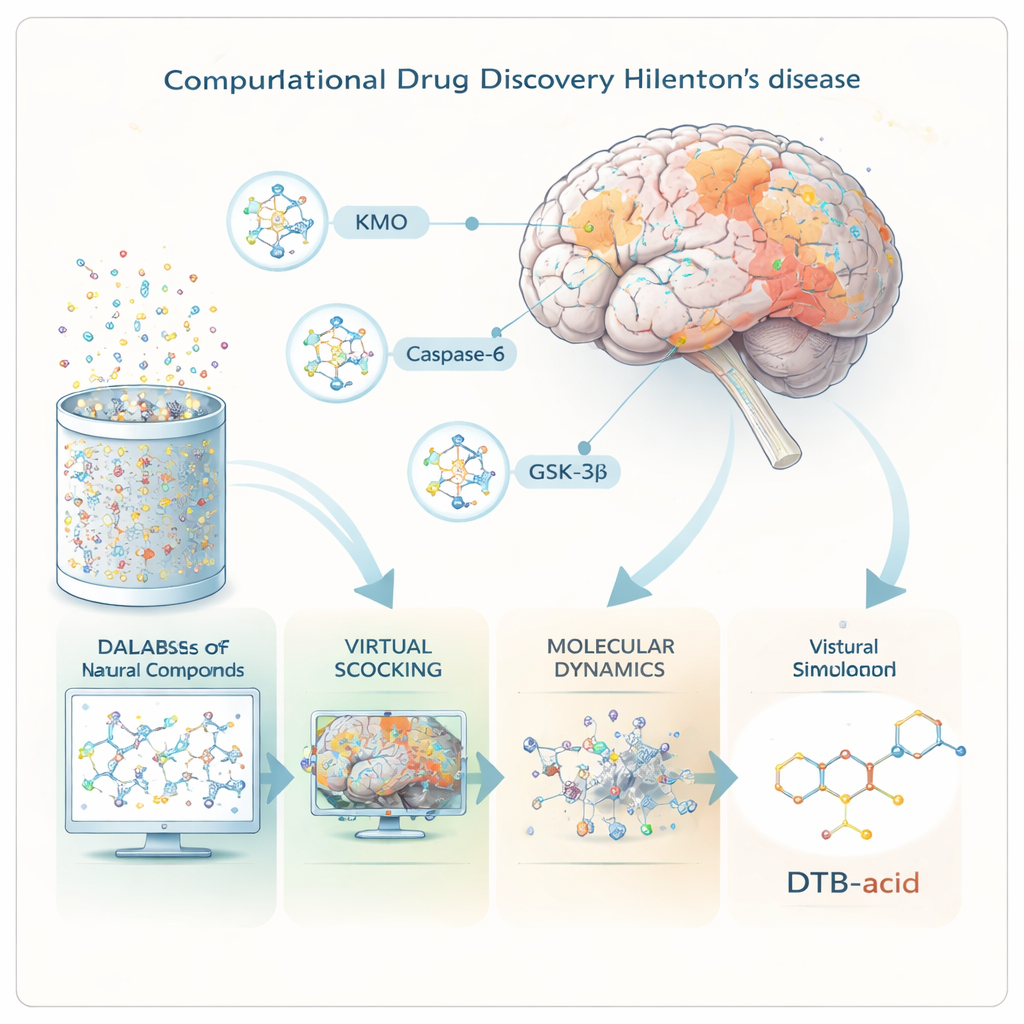
用超级计算机筛选自然界的化合物库
研究者并未在试管中混合化学物质,而是完全“在硅上”进行,使用先进的软件模拟分子行为。他们从一个公共数据库中收集了超过695,000种天然化合物,将每种化合物制备成三维形式。强大的虚拟筛选工具随后预测哪些化合物更可能穿过血脑屏障、在体内表现出类似真实药物的特性并避免主要安全问题。大约只有60,000种化合物通过了这些过滤,并在计算机上测试它们与三个靶蛋白结合口袋的拟合紧密程度。
脱颖而出的一种分子:DTB-酸
在这次大规模搜索中,一种名为DTB-酸的分子——一种与matrinic酸相关的天然生物碱——脱颖而出。详尽的对接研究表明,DTB-酸可以在三种蛋白中形成强而恰当的接触。接着,团队进行了长时程分子动力学模拟,以模拟原子在水中随时间的运动,检查该化合物是否会保持结合而非脱离。在模拟的100纳秒(或100亿分之一秒)运动中,蛋白-药物复合体保持稳定。额外的能量计算表明,与KMO的结合尤其强,而对结合位点中水分子行为的单独分析则显示,与GSK-3β的相互作用在热力学上也是有利的。
从计算命中到未来药物
当然,在屏幕上看起来有前景的分子只是第一步。作者强调,DTB-酸仍需在细胞和动物中进行测试,以确认其是否能够到达脑内、命中预期靶点并在不产生有害副作用的情况下真正保护神经元。即便如此,这项工作展示了发现用于复杂脑疾病的多靶点药物的一条高效且强大的路径。对非专业读者而言,核心信息是:与其用一系列各自针对狭窄靶点的药物治疗亨廷顿病,不如有可能设计出像DTB-酸这样精心定制的单一化合物,同时应对多种致损驱动因素——为减缓或改变这一无情疾病的进程带来新的希望。
引用: Zheng, B., Banday, M., Gangwar, S. et al. In silico discovery of natural compound-derived multi-target inhibitor for Huntington’s disease therapy. Sci Rep 16, 7716 (2026). https://doi.org/10.1038/s41598-026-38430-w
关键词: 亨廷顿病, 多靶点药物, 计算药物发现, 天然化合物, 神经退行性疾病