Clear Sky Science · zh
整合多数据集筛选以预测肝细胞癌患者预后并识别免疫治疗基因靶点
这对肝癌患者为何重要
肝细胞癌是最常见的原发性肝癌,每年夺去数十万人的生命。即便病期相同,患者对治疗的反应差异很大,尤其是针对激活机体自身免疫系统的现代免疫疗法。本研究提出了一个简单但关键的问题:我们能否像读取指纹一样通过肿瘤的基因活动来预测哪些患者预后较差、哪些人会对免疫药物有反应,以及哪些基因可能成为最佳的新治疗靶点?
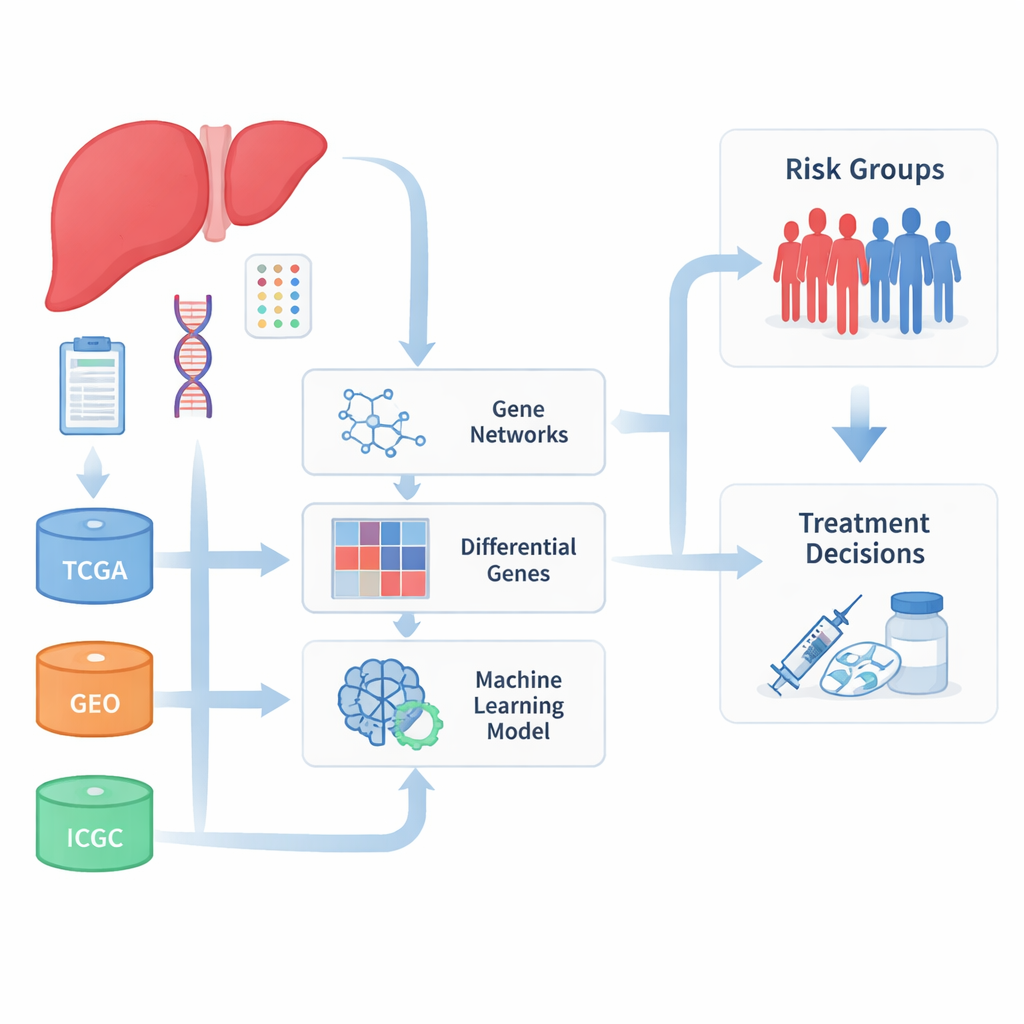
整合多项数据集
研究者首先汇集了来自若干国际数据库的大规模肝癌样本,这些数据库存储了肿瘤基因表达和临床结局信息。通过合并来自癌症基因组图谱(TCGA)、国际癌症基因组联盟(ICGC)以及多个基因表达综合(GEO)研究的数据,他们构建了比任何单一医院或项目都更大、更具多样性的患者集合。由于这些数据由不同实验室和不同方法产生,团队首先投入大量工作纠正技术差异,以确保推动结果的是生物学信号而非实验室噪音。
发现与结局相关的基因模式
在处理过的清洗数据上,团队寻找那些倾向于共同开启或关闭并且与患者结局相关联的基因群。采用网络化方法,他们将数千个基因聚类为模块,然后聚焦于与肿瘤行为和患者生存最强相关的模块。同时,他们将肿瘤组织与非肿瘤组织比较,以找出在癌症中明显上调或下调的基因。两种视角的交集产生了一组93个基因,这些基因既在肝癌中发生改变,又与疾病关键特征紧密相关,许多与肝脏药物代谢和有毒化学物质处理有关。
构建十基因风险评分
为了把这些基因列表转化为医生最终可能使用的工具,作者采用了机器学习方法。他们测试了100多种特征选择与生存预测算法组合,依据这些方法在多个独立队列中将患者准确分为预后较好与较差组的能力来评判。从大量搜索中,他们提炼出紧凑的十基因特征,共同构成一个风险评分。高评分患者在总体生存、无病生存和无进展生存方面均显著较短,这一结果在主要数据集和外部验证组中都得到一致验证。在这些基因中,TYMS 是不良预后的强烈指示因子,而 APOL3 和 FBXO2 与较好的结局相关联。
来自肿瘤免疫环境的线索
该研究不仅停留在预测层面,还探寻这些基因为何重要。通过多种计算工具,团队评估了每个肿瘤中存在哪些类型的免疫细胞,以及十基因评分与该免疫景观的相关性。高风险肿瘤往往表现出与更多突变及免疫逃逸迹象相关的免疫模式和基因改变,包括与已知免疫检查点分子(如 PD-1 和 CTLA-4)的关联。他们还检查了实际的突变谱,发现高风险肿瘤在经典癌症驱动基因(如 TP53)上更常见改变。最后,患者与健康志愿者的血液检测证实 TYMS 在肝癌患者中升高而 FBXO2 降低,支持这些基因在疾病中具有生物学活性,而不仅仅是统计学信号。
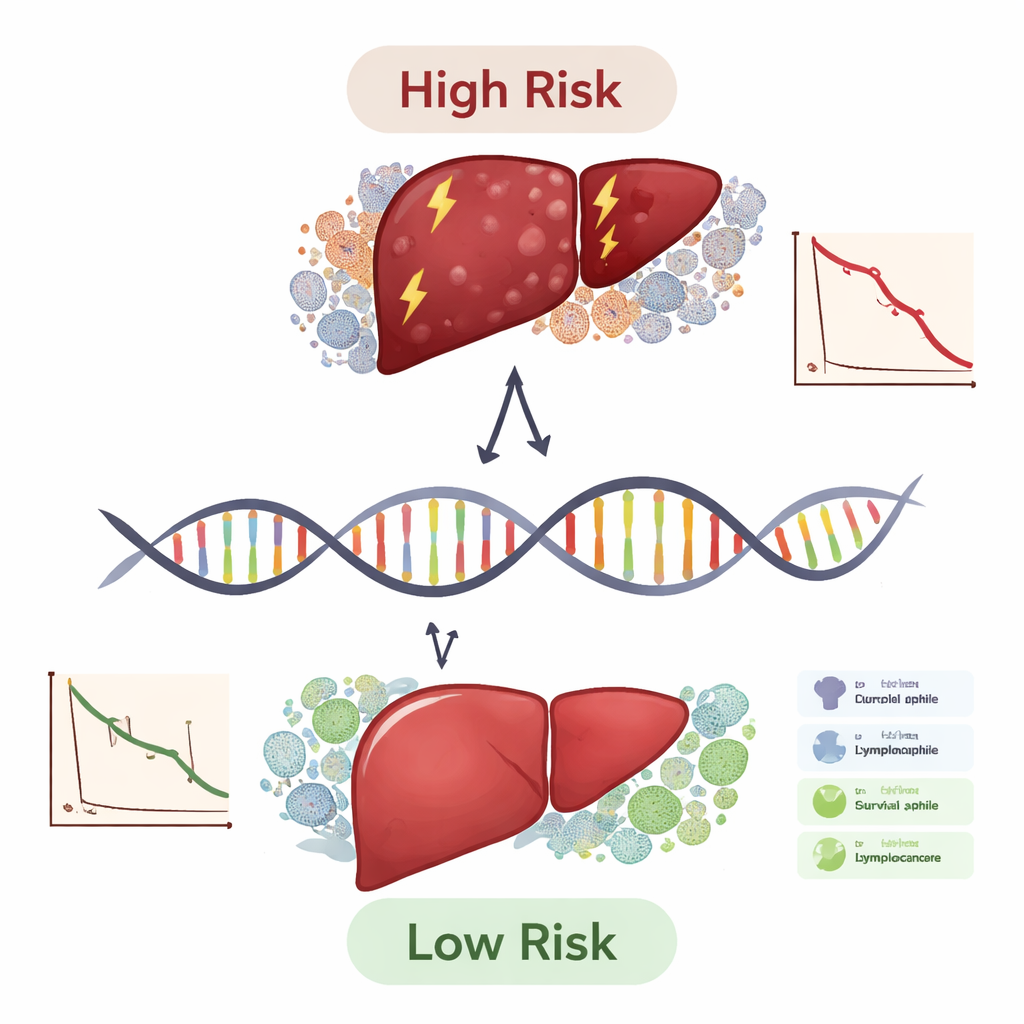
对患者和医生的意义
在实践层面,这项工作提供了使用小型基因面板将肝癌患者分层并提示谁可能从免疫疗法中获益的蓝图。该十基因评分尚未达到临床检测标准,但其表现优于单独的标准分期系统,并在不同患者亚组中保持有效。正如胆固醇检测指导心脏病预防一样,类似的基因面板未来可帮助肿瘤科医生为高风险患者选择更积极的治疗,避免对低风险患者造成不必要的副作用,并引导药物研发者关注如 TYMS、APOL3 和 FBXO2 等新靶点。仍需更大规模的前瞻性研究和实验室验证,但这项整合分析标志着朝着更个体化、以生物学为驱动的肝癌护理迈出的重要一步。
引用: Zhou, L., Zhang, W., Liu, Z. et al. Integrated multi-dataset screening to predict prognosis and identify immunotherapy gene targets in hepatocellular carcinoma patients. Sci Rep 16, 7014 (2026). https://doi.org/10.1038/s41598-026-38424-8
关键词: 肝细胞癌, 基因特征, 免疫治疗, 预后, 肿瘤微环境