Clear Sky Science · zh
母体芽孢杆菌益生菌通过脾脏IGF-1/mTOR和FOXO1/IL-10通路调节后代生长与免疫
为何母亲的微生物对后代重要
准父母常常好奇自身健康如何影响子女。本研究探讨了这一问题的一个特定版本:如果母亲在妊娠期间服用某种益生菌,是否能悄然重编程其后代的生长与免疫系统?研究人员以小鼠为模型,展示了给妊娠母鼠服用一种常见的芽孢杆菌益生菌,可以促进其后代更好的生长,并在以脾脏为中心的免疫防御中形成更平静、更高效的反应。
在恰当时间给予的友好细菌
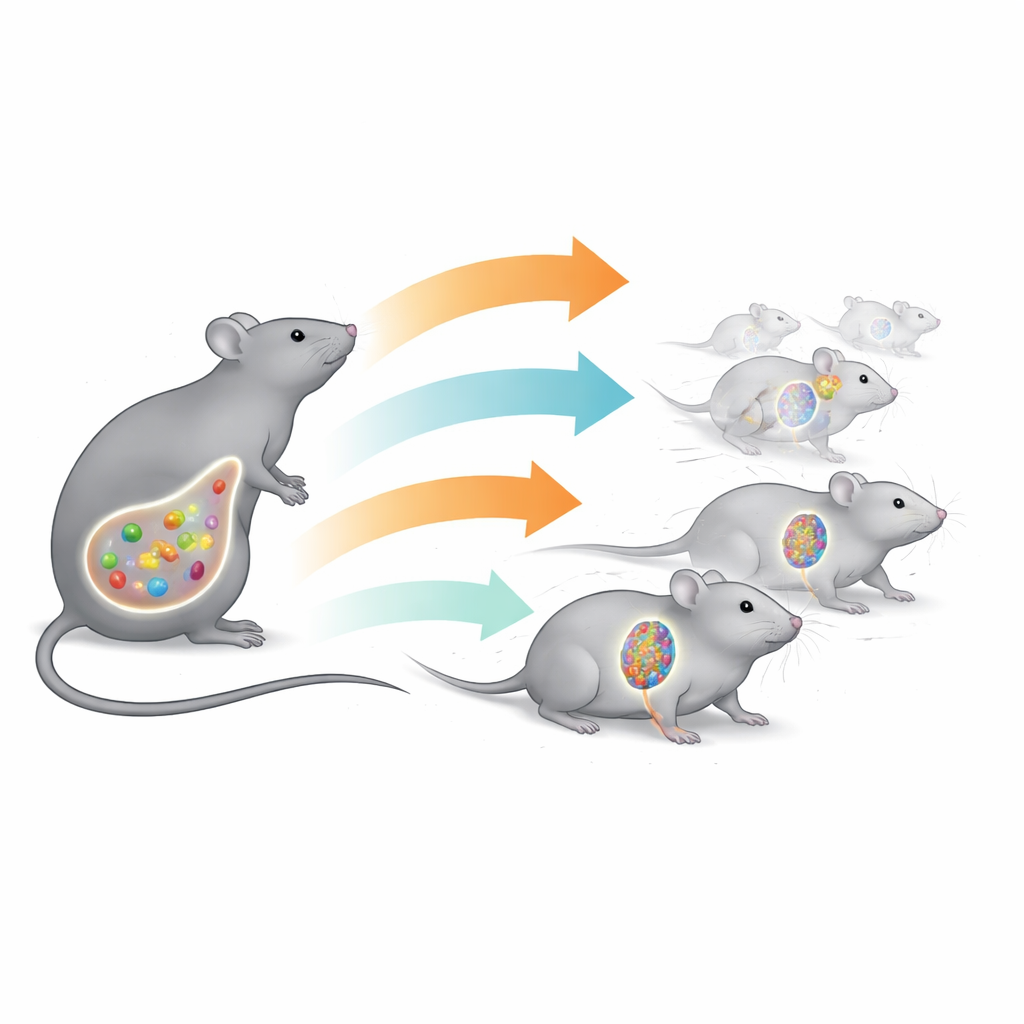
团队关注的是Bacillus clausii,一种已在人类用于支持肠道健康的形成孢子细菌。他们让雌鼠交配,并将怀孕的动物分为四组。一组吃标准饲料并饮用普通水。其余三组则在日常饲料中混入益生菌并每日给予,但开始时间不同:妊娠第0天(非常早)、第8天(中期)或第16天(晚期)。这一设计让科学家测试时间点是否对塑造下一代发育有影响。
更强的生长与更“忙碌”的脾脏
当雄性后代达到28天龄——约为小鼠的早期幼年阶段——研究人员对其称重并检查血液和脾脏。母体从怀孕一开始就接受益生菌的幼鼠体重最重,脾脏相对体重也最大。它们血液中生长激素及其配对信号胰岛素样生长因子1(IGF-1)水平较高,这两者共同促进体型生长。与此同时,常规血细胞计数保持正常,表明益生菌并未给动物带来应激或扰乱基础造血。
更平和、更平衡的免疫反应
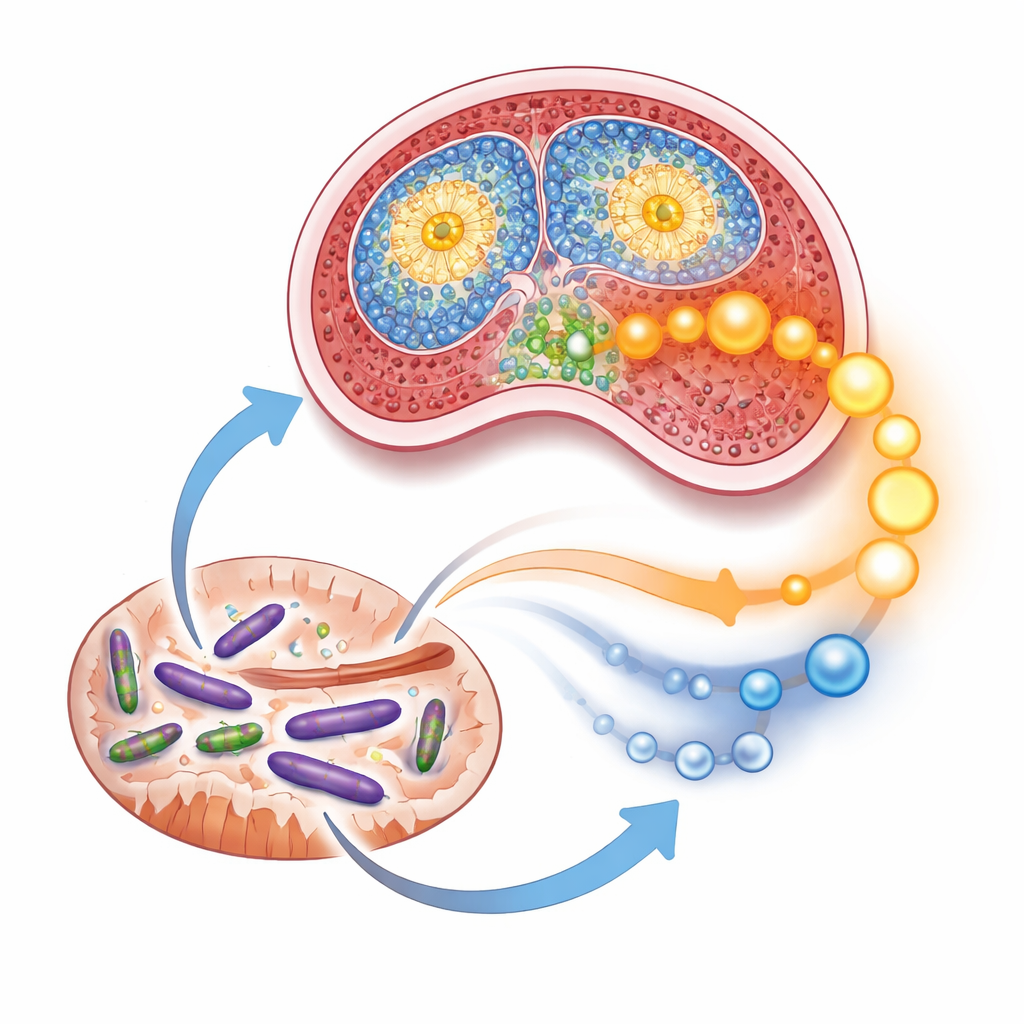
脾脏是巡逻血液的免疫细胞的中心聚集点。在接受益生菌的后代中,尤其是早期开始组,脾脏的内部结构在显微镜下显得更成熟。富含B细胞和T细胞的白髓区域更大且组织更有序,生发中心清晰,在此处产生抗体的细胞扩增。血液检测也反映了这一模式:保护性抗体IgA和IgG水平升高,而经典的促炎信号蛋白如肿瘤坏死因子-α(TNF-α)和干扰素-γ下降。相反,抗炎信使IL-10显著上升。综合这些变化,显示出一种更能应对威胁但不易发生有害过度反应的免疫系统。
脾脏控制回路内部
为超越简单指标,科学家们深入观察脾脏细胞内的分子控制开关。他们发现以mTOR蛋白复合体为中心的生长相关通路更为活跃,脾脏组织中IGF‑1信号更丰富。与此同时,一种名为FOXO1的转录因子——在静息免疫细胞中有助于维持静止状态——在其通常的细胞核位置上活性降低。该模式在母体从怀孕开始就给予益生菌时最为显著,而当补充在较晚开始时则较弱。这指出了早期发育期间存在一个窗口期,在此期间来自母体肠道的信号可以调节后代的免疫连接方式。
这对早期生命健康意味着什么
通俗来说,这项小鼠研究表明,母亲在早期妊娠期间服用恰当的益生菌,可能会将其后代引导向更好的生长和更精细调节的免疫系统。通过重塑脾脏结构并将化学信号倾向于抗炎反应,母体的Bacillus补充似乎产生出既更健壮又不易发生过度免疫反应的幼鼠。尽管仍需更多工作——尤其是在人体中——以确定安全性、时间和确切机制,这些发现强调了一个诱人的想法:母体肠道微生物的简单改变或许提供了一种低成本方法来增强儿童的长期免疫韧性。
引用: Aldayel, T.S., Abdelrazek, H.M.A., El-Fahla, N.A. et al. Maternal Bacillus probiotic regulates offspring growth and immunity via spleen IGF-1/mTOR and FOXO1/IL-10 pathways. Sci Rep 16, 8500 (2026). https://doi.org/10.1038/s41598-026-38412-y
关键词: 母体益生菌, 婴儿免疫, 克劳氏芽孢杆菌, 脾脏发育, 早期生命微生物组