Clear Sky Science · zh
使用光学相干断层扫描血管造影并结合集成机器学习分类器用于帕金森病诊断
眼睛为何能揭示隐匿的大脑疾病
帕金森病通常要等到震颤、僵硬或运动迟缓出现后才被诊断——这些症状意味着大脑已经在多年内发生了变化。本研究探索了一条意想不到的捷径:用无痛的成像扫描观察眼底微小血管,再借助人工智能来筛查可能早期患有帕金森病的人,从而比现有体检手段更早、更客观地发现病情。
通过眼睛观察大脑
眼后部的感光组织——视网膜,本质上是大脑中易于接近的一部分。它拥有与大脑相似的神经和血管,但可以在门诊中进行无创检查。研究者使用了一种名为光学相干断层扫描血管造影(OCTA)的技术,它能生成视网膜血流的精细、无需注射染料的图谱。由于帕金森病与全身小血管问题有关,团队探讨了这些视网膜血管网络中的细微变化是否可作为窥视早期疾病的“窗口”。
将眼部扫描转化为数字
在一项回顾性研究中,团队收集了53例帕金森病患者和39名年龄匹配健康志愿者的OCTA扫描图像。他们关注视网膜的两个血管层:靠近表面的浅层和下面的深层。从每一层自动分割出中央黄斑无血管区——这个维持清晰视力的小凹——以及其周围的毛细血管。随后将每张图像转化为22项数值测量。有些指标描述了无血管区的形状,例如边缘有多圆、有多平滑或多不规则。另一些则捕捉了整体血管密度以及黄斑周围环形区域的密度。综合这些测量可以比人工肉眼判读更细致地量化微血管健康状况。 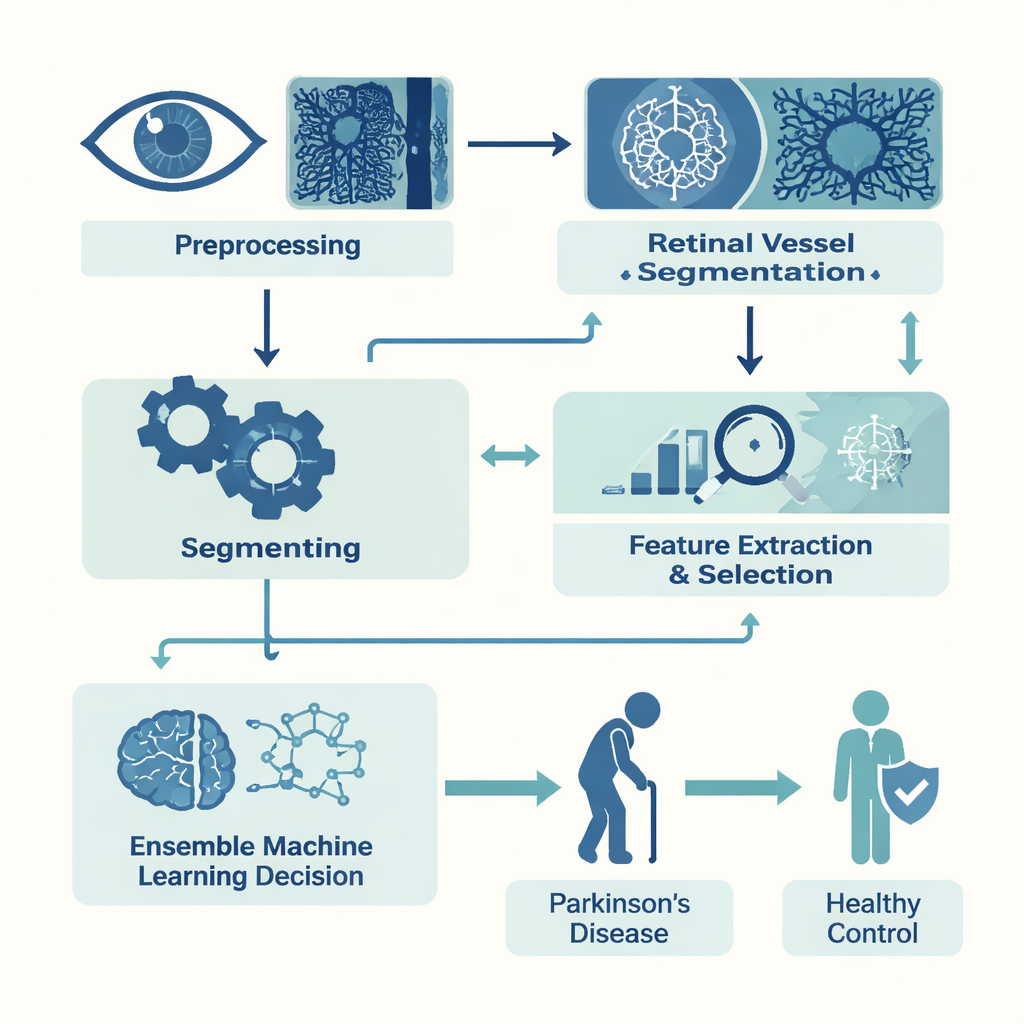
训练人工智能识别帕金森模式
基于这些测量值,研究者构建了计算模型以区分帕金森病与健康的扫描。由于数据集规模有限,他们首先使用特征选择技术将22项测量精简为信息量最大的子集,以减少噪声和过拟合。随后训练了几种常见的机器学习算法,包括基于决策树的方法和k最近邻分类器。最后,他们将表现最好的三种模型——XGBoost、随机森林和k近邻——组合成一个加权“集成”模型,使每个模型的投票按其表现权重计入最终决策。
模型在视网膜中发现了什么
与健康志愿者相比,帕金森病患者显示出明显的视网膜微循环改变。血管密度指标较低,中央黄斑无血管区在形状上更不规则——在浅层和深层血管层中均表现为较不圆、较不平滑、较不致密。在对未见过的数据进行测试时,集成模型总体上能正确分类约四分之三的眼睛。最显著的是,其敏感性高达90%:即十例帕金森病中能正确识别出九例。特异性则较为有限,仅略高于一半,意味着部分健康个体被误判为患病。受试者工作特征曲线下面积(AUC)为0.75,表明具有实用但并非决定性的识别能力。 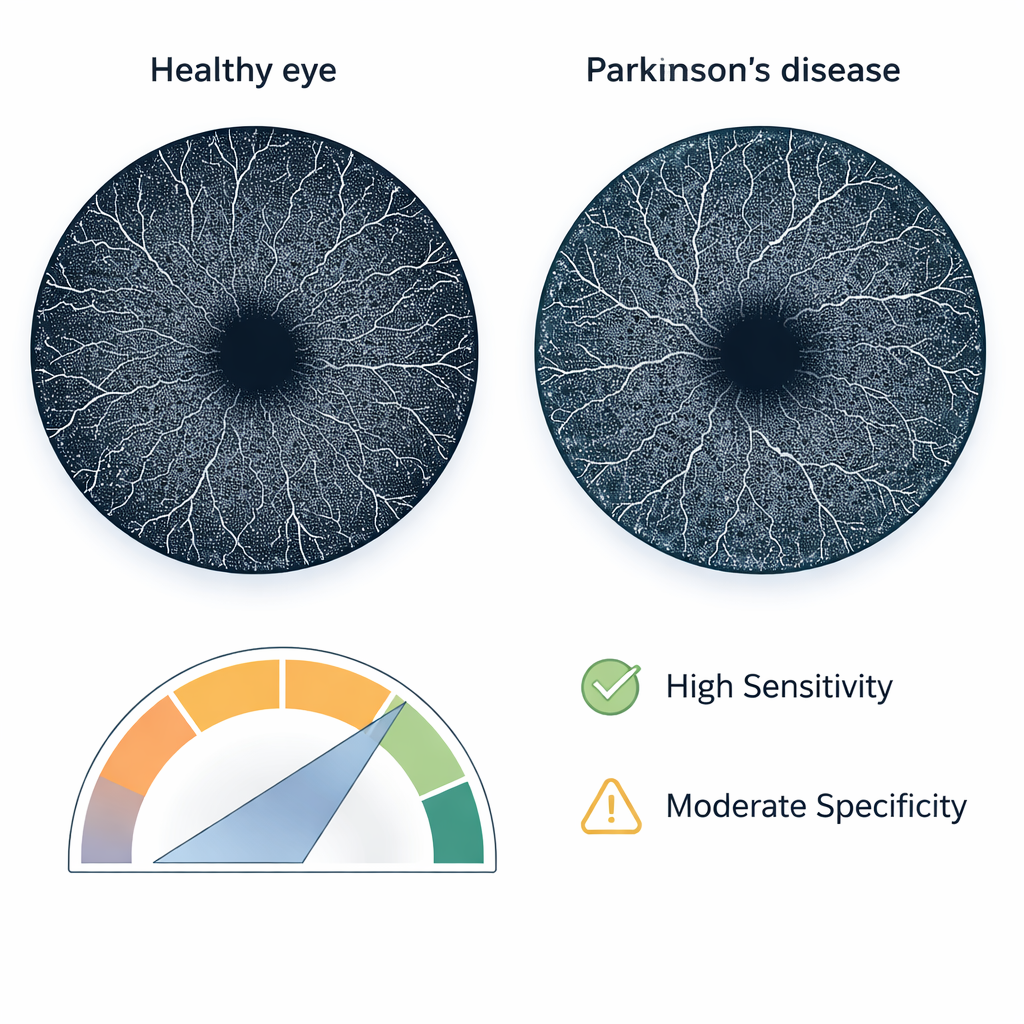
从算法走向临床
为将理论付诸实践,团队将方法封装成名为“帕金森病人工智能”(Parkinson’s Disease Artificial Intelligence,PDAI)的原型软件工具。通过简洁的图形界面,临床医生可以加载OCTA扫描、查看自动描绘的血管和中央黄斑无血管区、查看关键数值特征,并即时获得该扫描是否类似帕金森病病例的预测。由于系统依赖于手工设计且定义明确的测量指标,而非不透明的“黑箱”,每次决策的贡献因素更易为临床医生所理解并可能与潜在生物学机制相关联。
这对患者意味着什么
这项工作尚不能作为独立的帕金森病检测手段,但表明一次快速、无创的眼部扫描,结合精心设计的机器学习方法,能够以高敏感性发现与疾病相关的变化。在临床实践中,这样的工具或可作为筛查辅助手段——帮助眼科医生和神经科医生决定谁应更密切监测或及早转诊进一步评估,远在严重症状出现之前。仍需更大规模、多中心的研究,但研究提示眼睛确实可能为帕金森病提供一种实用的早期预警信号。
引用: Hasanshahi, M., Mehdizadeh, A., Mahmoudi, T. et al. An ensemble machine learning classifier for Parkinson’s disease diagnosis using optical coherence tomography angiography. Sci Rep 16, 7297 (2026). https://doi.org/10.1038/s41598-026-38407-9
关键词: 帕金森病, 视网膜成像, OCTA, 机器学习, 早期诊断