Clear Sky Science · zh
基于机器学习的干性与血管生成相关基因预后模型用于预测肝细胞癌患者的预后与免疫浸润
这项研究对肝癌患者的重要性
肝细胞癌是最常见的肝癌类型,即便经过治疗也常发生复发或转移。本研究探讨了造成这一现象的原因以及如何更好地预测哪些患者面临更高风险。研究人员结合大规模基因组数据与现代机器学习,构建了一个工具,将两种强大的癌症特性——“干性”(像顽固种子一样的细胞)和新血管生成——与患者的生存机会及其对免疫治疗的潜在反应联系起来。
癌症“种子细胞”和新血管
许多肿瘤含有一小群像种子一样的细胞。这些癌症干细胞能够自我更新、耐受治疗,并在手术或化疗后重新启动肿瘤。同时,肿瘤需要通过新血管为自身输送氧气和营养以实现生长与扩散。近来的研究表明,这两个过程相互交织:类干细胞释放促血管生长的信号,而富含血管的微环境又有助于这些种子细胞存活。理解并同时靶向这一合作关系在肝癌中尤为重要,因为肝癌高度血管化且易复发。
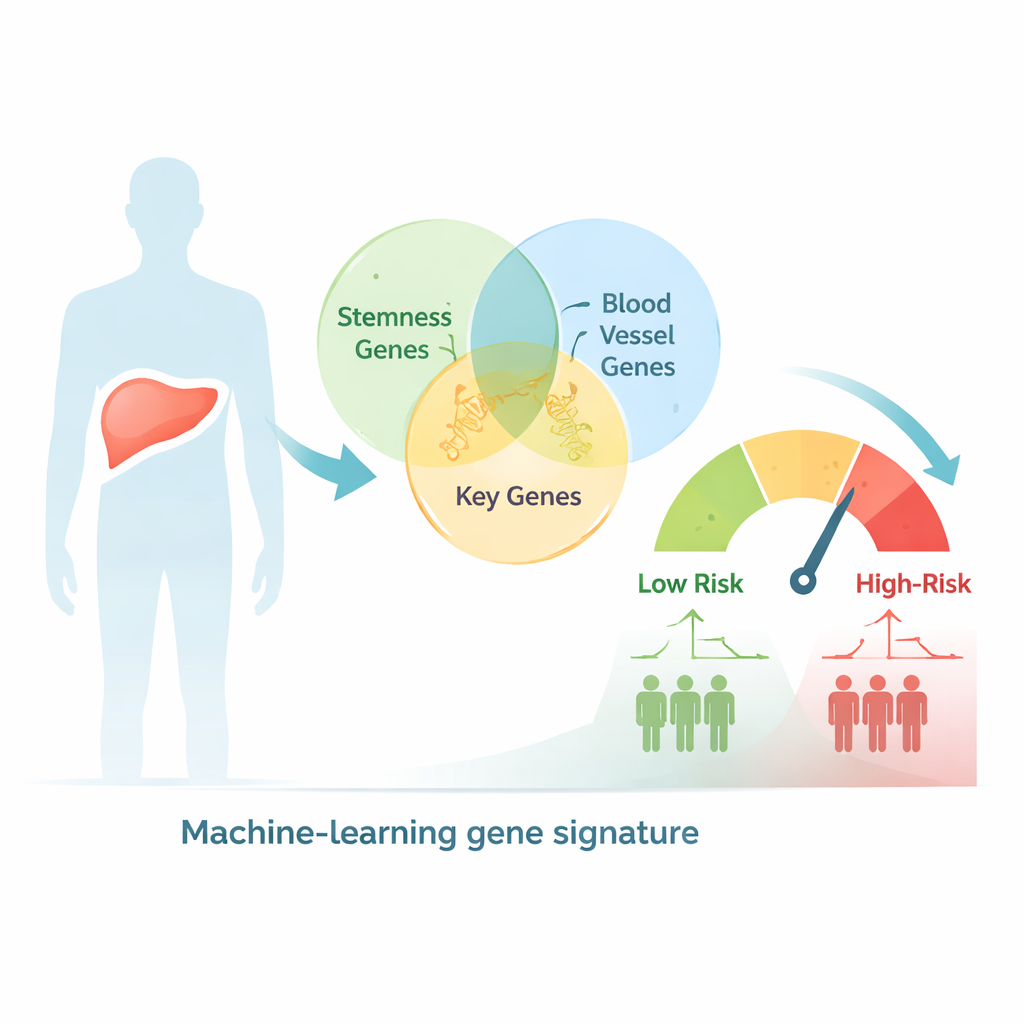
利用大数据将患者按风险分类
研究人员首先在大型人类基因数据库中筛选与干性行为和血管形成均相关的基因,得到超过2600个重叠候选基因。随后,他们审查了数百例肝癌样本,这些样本在公共癌症数据库中记录了肿瘤基因表达和临床结局。通过统计检验与聚类方法,他们将患者分为两种基因亚型,这两组在分期、肿瘤大小和生存方面表现出明显差异,表明联合的干性与血管相关信号反映了该疾病的重要生物学特征。
构建九基因风险评分
从这一庞大基因池中,研究团队采用机器学习方法缩减至9个关键基因,其联合表达对患者生存时间的预测效果最佳。以这9个基因计算出每位患者的风险评分。肿瘤评分较高的患者总体生存显著较短,这一点在原始数据集和用于验证的独立肝癌队列中均得到证实。该模型的准确性与许多现有工具不相上下或更优;当将该评分与诸如肿瘤分期等简单临床信息结合并绘制为列线图(nomogram)时,对1年、3年和5年生存的预测进一步改善。
与免疫系统及治疗反应的关联
研究团队还探讨了九基因评分对肿瘤免疫微环境的提示。低风险肿瘤往往更具“炎性”特征,伴有更多种类的免疫细胞以及更强的攻击通路信号。相比之下,高风险肿瘤显示出免疫逃逸的模式,并在诸如TP53等重要基因中具有更高的突变率。利用已建立的计算工具来估计肿瘤对现代免疫治疗药物的潜在反应,研究表明低风险患者可能比高风险患者对免疫检查点抑制剂反应更好。尽管这些预测仍需在真实治疗环境中验证,但它们为识别可能最能从此类药物中受益的患者提供了实用途径。
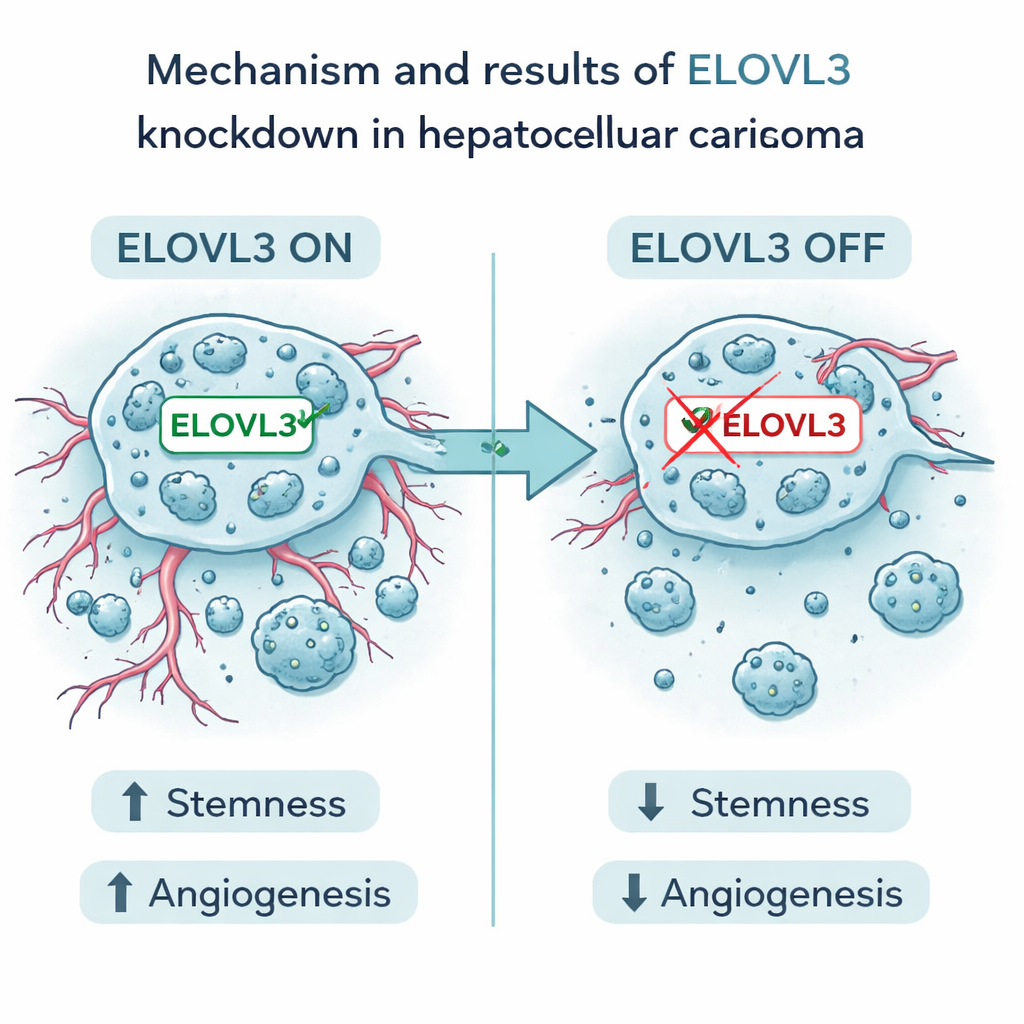
聚焦一个有前景的靶点
在这9个基因中,名为ELOVL3的基因尤为突出。该基因高表达与较差生存相关。在实验室研究中,作者在人体肝癌细胞中下调ELOVL3。这使细胞形成类干簇的能力下降,已知的干性标志物水平降低。与此同时,促血管的两种主要因子VEGFA和FGF2的产生与释放也减少。癌细胞的增殖、迁移和侵袭能力减弱,在小鼠模型中,下调ELOVL3的肿瘤更小且具有较少的侵袭性特征。这些发现支持ELOVL3在促进肝癌细胞的种子样行为及其构建支持性血管方面发挥作用的观点。
对未来治疗的意义
简言之,这项工作传递了两个主要信息。其一,基于肿瘤样本的简单九基因评分可以将肝癌患者分为高低风险组,并提示他们对免疫治疗的可能反应。其二,评分中的一个基因ELOVL3似乎位于肿瘤再生能力与新血管生成能力的交汇点,使其成为一个有吸引力的未来药物靶点。尽管该模型和靶点需要在前瞻性临床试验中得到确认,但它们为更个体化的肝癌治疗以及同时阻断癌症“种子细胞”和其血液供应的组合策略打开了大门。
引用: Cheng, F., Shi, Y., Gao, X. et al. Machine learning-based prognostic model of stemness and angiogenesis-related genes for predicting prognosis and immune infiltration in patients with HCC. Sci Rep 16, 7271 (2026). https://doi.org/10.1038/s41598-026-38379-w
关键词: 肝细胞癌, 癌症干细胞, 血管生成, 预后基因特征, ELOVL3