Clear Sky Science · zh
抑制加拉宁受体3通过调节炎症与氧化应激反应减缓视网膜色素变性中的视网膜退行性变
为何保护渐弱的夜间视力至关重要
视网膜色素变性是一组遗传性疾病,缓慢夺走患者的夜间和周边视力,常在中年导致严重视力丧失。目前尚无普遍有效的治疗方法,部分原因在于许多不同的基因突变都可致病。本研究采用不同思路:与其修复受损基因,不如探讨是否通过抑制有害的炎症和视网膜内类似“锈蚀”的损伤,来减缓光感受器的丢失并帮助保留视力。
隐藏在视网膜中的应激开关
位于眼后部的光感受器必须持续平衡能量消耗、氧气、营养和废物清除。在一种常见的视网膜色素变性形式中,视紫红质蛋白的P23H突变导致这种视觉色素折叠异常,堵塞细胞内的机械系统并触发慢性应激。该应激反过来会引发炎症和氧化损伤,二者都能导致光感受器死亡。作者关注一种名为加拉宁受体3(GALR3)的信号蛋白,该受体存在于多种视网膜细胞类型中。他们发现在携带P23H突变的小鼠中,GALR3及其天然配对分子的活性比健康眼更强,提示GALR3可能在退行性视网膜中充当应激放大器。
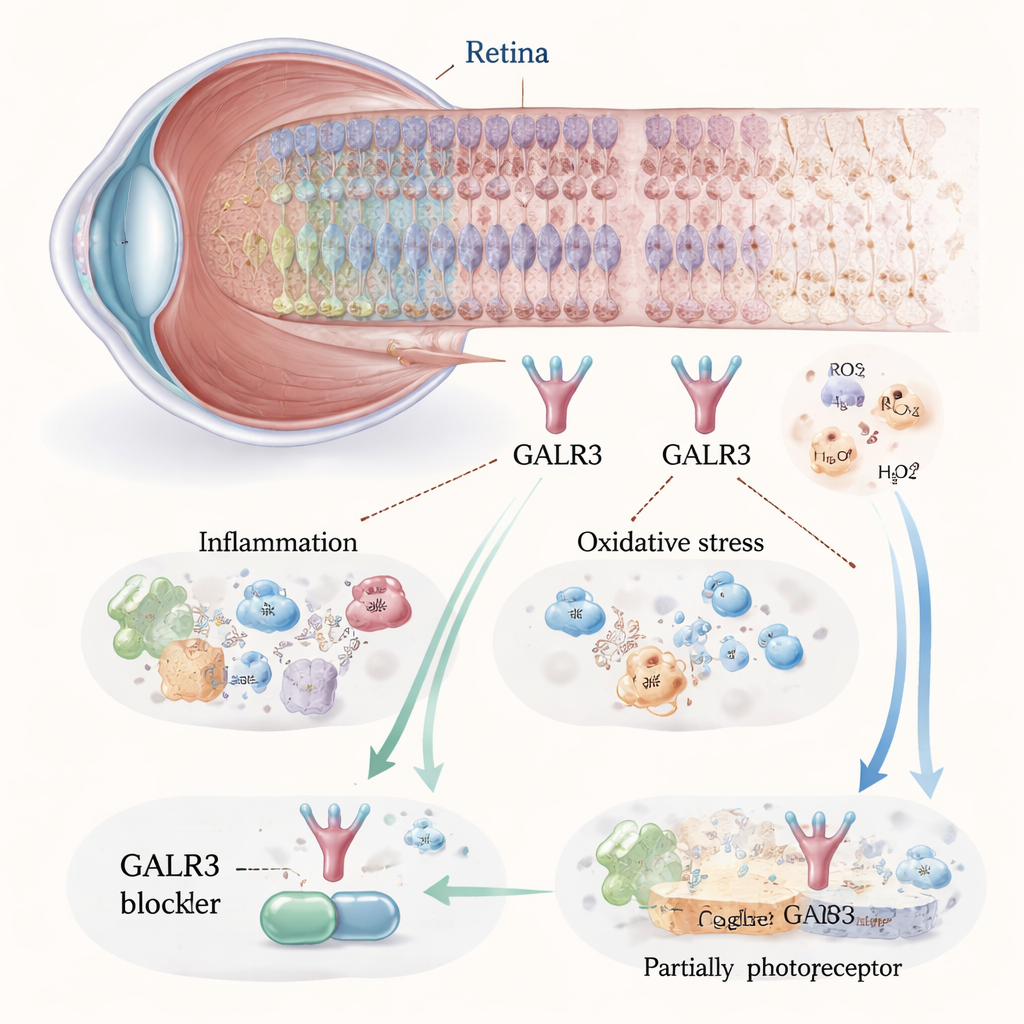
通过阻断有害信号减慢细胞丢失
为检验GALR3是推动损伤还是提供保护,研究者在P23H小鼠中采用了两种策略:培育完全缺失Galr3基因的动物,另对另一组用一种可特异性阻断该受体的药物SNAP-37,889进行处理。数周内,他们用高分辨率成像检查视网膜结构并测量对光的电生理反应。在未处理的P23H小鼠中,容纳光感受器核的那一层到一月龄时比正常小鼠变薄约一半并持续萎缩。阻断GALR3后,这种变薄显著减轻,关键视觉蛋白如视紫红质和锥体光感蛋白保持在更高水平。视网膜的电生理记录也显示,接受处理或缺失GALR3的小鼠对光的反应更强,表明幸存的细胞不仅存在,而且功能更好。
降低炎症并提升防御能力
团队随后探究为何抑制GALR3有益。在视网膜色素变性中,视网膜的支持细胞——穆勒细胞和小胶质细胞——会从维护者转变为过度活跃的反应者,助长慢性炎症。在P23H小鼠中,这种“警戒状态”的标志物(包括胶质细胞中的GFAP和小胶质细胞中的IBA-1)显著升高,一系列炎性分子和危害感知复合体,如NF-κB和NLRP3炎性小体,也处于高表达状态。阻断GALR3能平息这种反应:胶质细胞活化减弱,促炎细胞因子下降,与组织修复相关的抗炎信号如IL‑10和TGF‑β1在疾病早期上升。与此并行,GALR3抑制还强化了视网膜的抗氧化机制。它提升了NRF2(一种抗氧化基因的主控因子)的活性,并增加了中和活性氧种的酶活性,有助于限制代谢应激引发的进一步损伤。
保护眼内屏障
健康的视力还依赖于紧密的“血–视网膜屏障”,以阻止不受欢迎的分子和免疫细胞涌入脆弱的神经组织。在P23H小鼠中,该屏障开始泄漏:视网膜色素上皮细胞之间的连接变得破损,血液蛋白渗入视网膜。无论是通过基因去除还是药物阻断GALR3,这些缺陷都显著减少,屏障的整齐“瓷砖状”结构得以保存并限制了渗漏。在细胞培养实验中,暴露于活化小胶质细胞产生的炎性信号下的类光感受器细胞会增加自身的炎性基因表达,但当光感受器细胞中的GALR3被沉默时,这一效应被削弱。综合来看,这些发现表明GALR3位于连接小胶质细胞活化、氧化应激和屏障破坏到光感受器死亡的枢纽上。
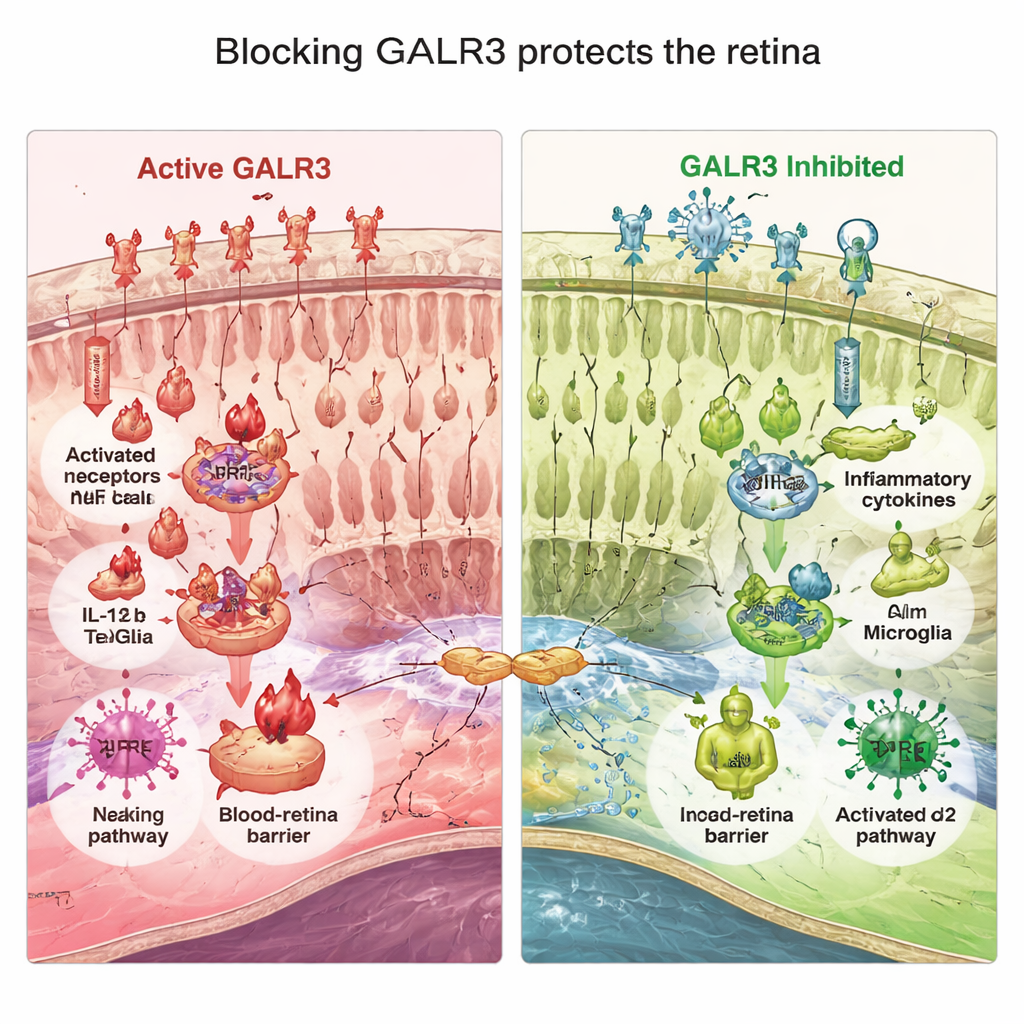
一种不依赖突变类型的保视路径
对于患有视网膜色素变性的人群,尤其中那些可能永远得不到基因特异性疗法的人,能广泛减缓视网膜损伤的策略具有重要价值。本研究确定了GALR3作为在一种广泛使用的小鼠模型中对有害炎症和氧化应激的关键“音量调节器”。阻断GALR3并未治愈视网膜色素变性,但它持续减缓了光感受器的丢失、改善了视网膜对光的反应、减少了有毒炎症、增强了天然抗氧化防御并有助于维持眼内屏障。由于GALR3作用于应激和免疫通路而非单一突变,靶向该受体的药物原则上可能帮助因多种不同遗传原因引起视网膜退行性变的患者。
引用: Azam, M., Pashandi, Z., Liu, M. et al. Inhibition of galanin receptor 3 slows down retina degeneration in retinitis pigmentosa through modulation of inflammatory and oxidative stress response. Sci Rep 16, 7765 (2026). https://doi.org/10.1038/s41598-026-38345-6
关键词: 视网膜色素变性, 视网膜炎症, 光感受器存活, 加拉宁受体3, 氧化应激