Clear Sky Science · zh
DGCR8 调节转录偶联核苷酸切除修复的多重过程
阳光如何与我们的基因“对话”
每次我们走到阳光下,肉眼不可见的紫外线(UV)会照射皮肤并损伤细胞内的 DNA。大多数情况下,细胞会在问题发生前悄悄修复这些损伤。本研究揭示了该保护系统中一个令人意外的参与者:一种名为 DGCR8 的蛋白质,以前以帮助细胞生成 microRNA 而闻名。研究者表明,DGCR8 在暴露于紫外线后可以转换职责,协调关键 DNA 修复通路的多个步骤,从而有助于预防癌症和其他疾病。
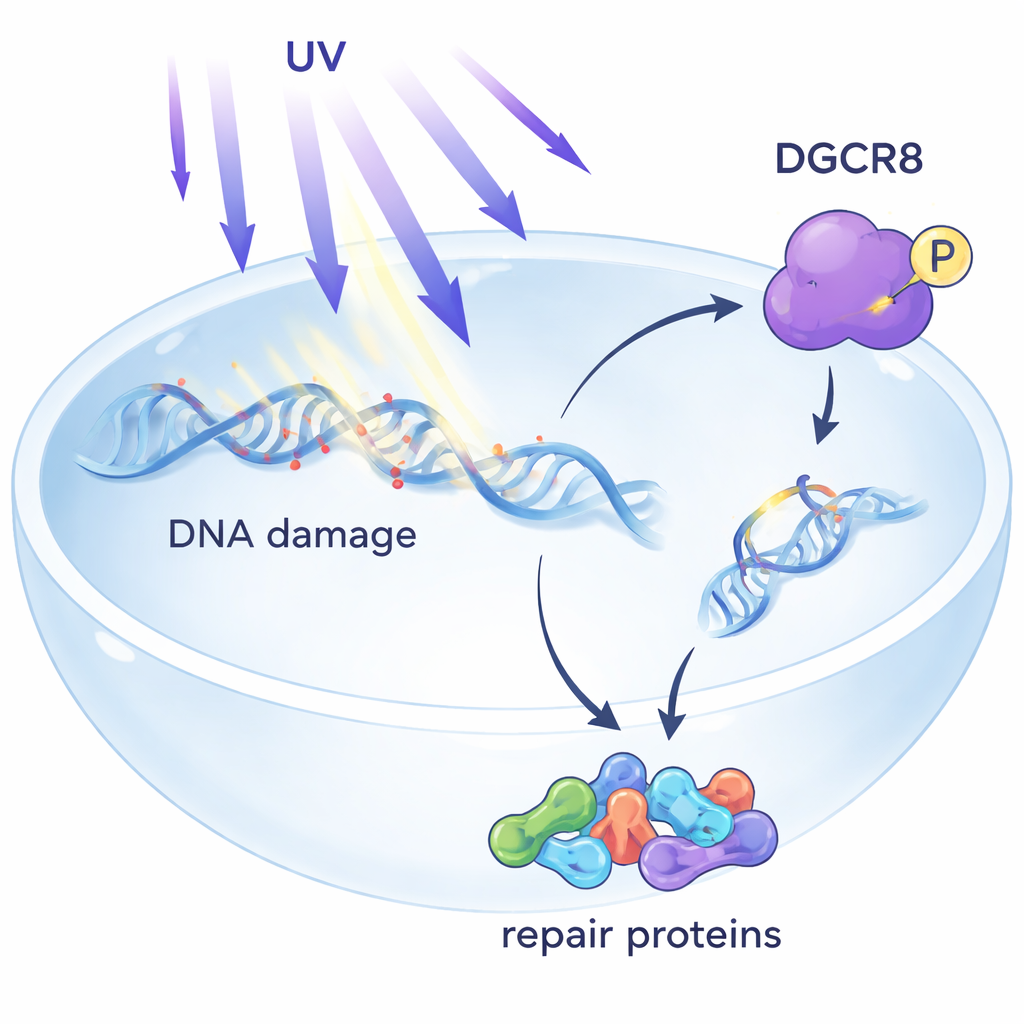
隐藏在 DNA 修复中的守护者
紫外线在 DNA 上产生微小的损伤,这些损伤会阻碍读取基因的分子机器。机体的主要防御之一是转录偶联核苷酸切除修复(TC-NER),它专门修复会使基因读取酶停滞的损伤。迄今为止,DGCR8 主要以处理 microRNA 而为人所知——microRNA 是调节基因表达的短 RNA 分子。早期工作提示 DGCR8 也能保护细胞免受紫外线侵害,但其机制尚不清楚。本文显示,紫外线暴露后,DGCR8 会与 TC-NER 的核心因子发生物理结合,充当组织者,将修复组件汇聚到基因读取被阻塞的位点。
DGCR8 的分子开关
DGCR8 扮演新角色的关键在于其一个氨基酸残基上的单个化学修饰:位于第 153 位的丝氨酸被磷酸化。当这一位点被磷酸化——即加入一个磷酸基团——DGCR8 获得与 TC-NER 核心因子结合的能力,包括 RNA 聚合酶 II(基因读取酶)以及修复因子 CSB、CSA 和 UVSSA。工程化细胞中若引入不能在该位点被磷酸化的 DGCR8 变体(S153A 突变体),这些修复蛋白之间的相互作用减弱或丧失,正常由紫外线触发的修复复合体组装失败。相反,模仿持续磷酸化状态的“磷酸模拟”变体即使在无紫外线时也能强化关键相互作用。这些结果表明,Ser153 的磷酸化充当一个开–关开关,将 DGCR8 从其常规的 RNA 加工角色切换为 DNA 修复协调者。
解开危险的 DNA–RNA 纠结
除了聚集修复蛋白外,DGCR8 还参与管理被称为 R 环的结构——即新合成的 RNA 重新附着到其母体 DNA 上形成的短片段 DNA–RNA 杂交。在少量时,R 环可能有益,但在紫外线照射后积累过多会阻碍 DNA 的复制并破坏染色体稳定性。作者使用特异性抗体和荧光探针发现,缺失 DGCR8 或携带不可磷酸化的 S153A 形式的细胞在紫外线后积累了更多的 R 环。磷酸化的 DGCR8 在这些杂交结构处被观察到,尤其是在与紫外线诱导损伤重叠的区域,提示它有助于在受压的活跃基因位点精确地防止或清除有害的 R 环。
控制 DNA 复制的节奏
当 DNA 损伤或 R 环干扰基因组复制时,细胞通常通过称为 ATR–CHK1 的检查点放慢复制速度以保障安全。纤维追踪实验显示,具备正常 DGCR8 的细胞在紫外线后其复制轨迹变慢,表明检查点已被激活。鲜明对比的是,缺失 DGCR8 或携带 S153A 突变的细胞即便积累了 DNA 损伤和 R 环,复制速度仍接近正常。进一步检测显示,虽然 ATR 本身被激活,但其关键下游分子 CHK1 在这些突变细胞中激活不足。这表明磷酸化的 DGCR8 有助于将来自受损 DNA 和 R 环 的压力信号传递到 CHK1,使细胞能够暂停并稳定复制过程。
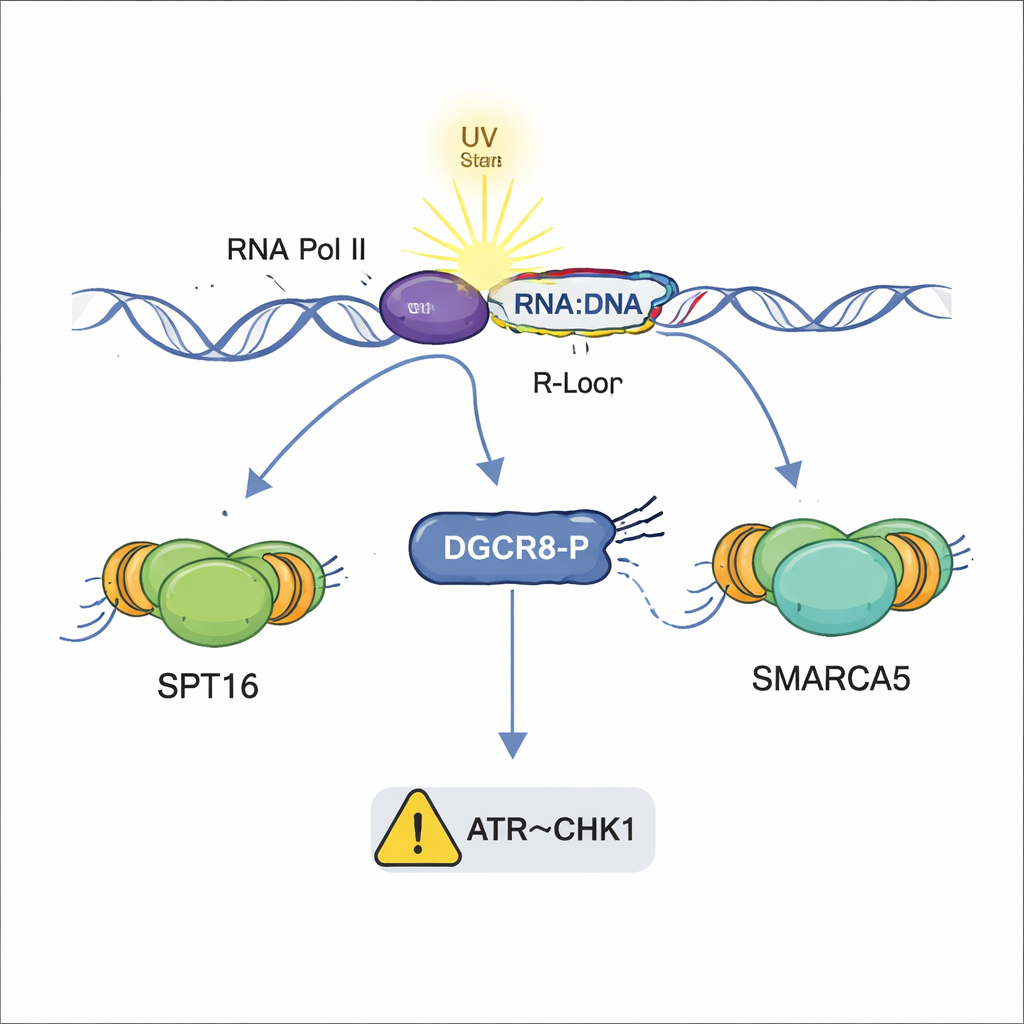
这对健康和疾病意味着什么
综合来看,研究结果将 DGCR8 描绘为一个多才多艺的守护者,它协调紫外线损伤应答的多个层面:组装 TC-NER 修复团队、招募打开染色质的重塑因子、抑制有害的 DNA–RNA 杂交体,并通过 ATR–CHK1 通路帮助触发复制减速。关键的是,这些作用独立于 DGCR8 在 microRNA 生物发生中的传统功能,并依赖于单一位点的磷酸化。鉴于 DNA 修复与 R 环 调控的缺陷与癌症和神经系统疾病相关,而在某些肿瘤中也发现了 DGCR8 的突变,理解这一分子开关可能为诊断或治疗由紫外线损伤和基因组不稳定驱动的疾病打开新的途径。
引用: Watanabe, T., Yoshinami, D., Yamasaki, H. et al. DGCR8 regulates multiple processes of transcription coupled nucleotide excision repair. Sci Rep 16, 7112 (2026). https://doi.org/10.1038/s41598-026-38338-5
关键词: 紫外线 DNA 损伤, DGCR8, DNA 修复, R 环, 基因组稳定性