Clear Sky Science · zh
PARP-1 将 β-连环蛋白/TCF4 信号与子宫内膜异位症中的上皮–间质转化联系起来
这项研究为何与女性健康相关
子宫内膜异位症是一种疼痛性疾病,类似子宫内膜的组织在卵巢等不该出现的部位生长。这些移位的病灶可以侵袭邻近结构、导致瘢痕形成并影响生育,而现有治疗往往不尽如人意,症状常复发。本研究考察了一种称为 PARP‑1 的分子“开关”,探讨它是否促使异位病灶更具侵袭性——以及现有阻断 PARP‑1 的药物是否能温和地将该开关关闭。
深入观察侵袭性病灶的行为
尽管子宫内膜异位症被归类为良性疾病,异位组织往往表现出令人惊讶的侵袭性:它们迁移、着床并持续存在,有点类似缓慢发展的癌症。驱动这种行为的关键过程之一是所谓的上皮–间质转化(EMT),在该过程中排列整齐、形成片层的细胞松动连接并获得更易移动、呈纤维样的特性。作者检查了有无子宫内膜异位症女性的组织,发现卵巢异位病灶呈现明显的 EMT 样模式:粘合蛋白 E‑钙粘蛋白下降,而表示更易移动细胞的标志物(如 N‑钙粘蛋白和波形蛋白)升高。同时,这些病灶中 PARP‑1 以及称为 Wnt/β‑连环蛋白的生长调控通路组分水平也最高,提示这些变化可能协同发生。
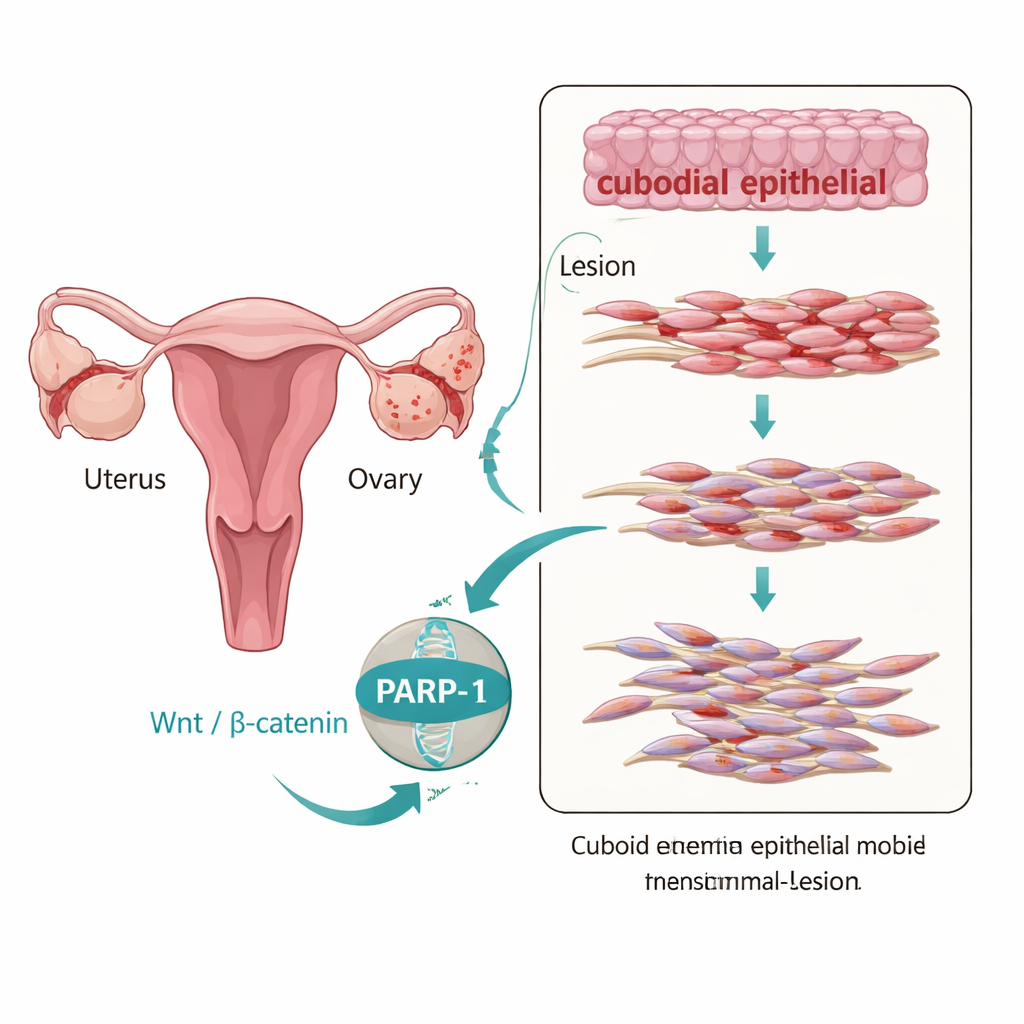
信号与细胞变化之间的分子桥梁
为弄清 PARP‑1 是仅仅存在于病灶中还是在积极驱动这些变化,研究者使用了一种永生化的子宫内膜异位上皮细胞系 12Z。当他们在这些细胞中人为提高 PARP‑1 水平时,EMT 标志朝向更具侵袭性的谱系转变,细胞在模拟伤口愈合和组织侵袭的体外测试中变得更具迁移性和存活性。当通过靶向 RNA 分子降低 PARP‑1 时,这一模式逆转:E‑钙粘蛋白增加,间质标志物下降,细胞的移动和增殖减少。重要的是,PARP‑1 与 β‑连环蛋白和 TCF4 物理结合,这两者是将 Wnt 信号转化为基因活性的关键因子,提示 PARP‑1 是一座分子桥梁,将外部信号与细胞核内的 EMT 基因程式连接起来。
用一种抗癌药物将开关调低
鉴于阻断 PARP 活性的药物已在癌症治疗中使用,团队进一步探问其中一种药物奥拉帕利(olaparib)是否能减弱 EMT 样特征并在小鼠子宫内膜异位模型中减少病灶生长。将子宫组织小片移植到小鼠腹腔后,动物出现了异位病灶,模拟了人类疾病的一些方面。用奥拉帕利处理两周后,这些动物的总病灶体积明显减小,子宫及其附着病灶质量也较未处理对照更轻。经处理的小鼠组织也显示出更“上皮化”的标志物模式——E‑钙粘蛋白更高而 N‑钙粘蛋白、波形蛋白、β‑连环蛋白和 TCF4 更低,表明 PARP 抑制推动细胞脱离侵袭性的 EMT 样状态。
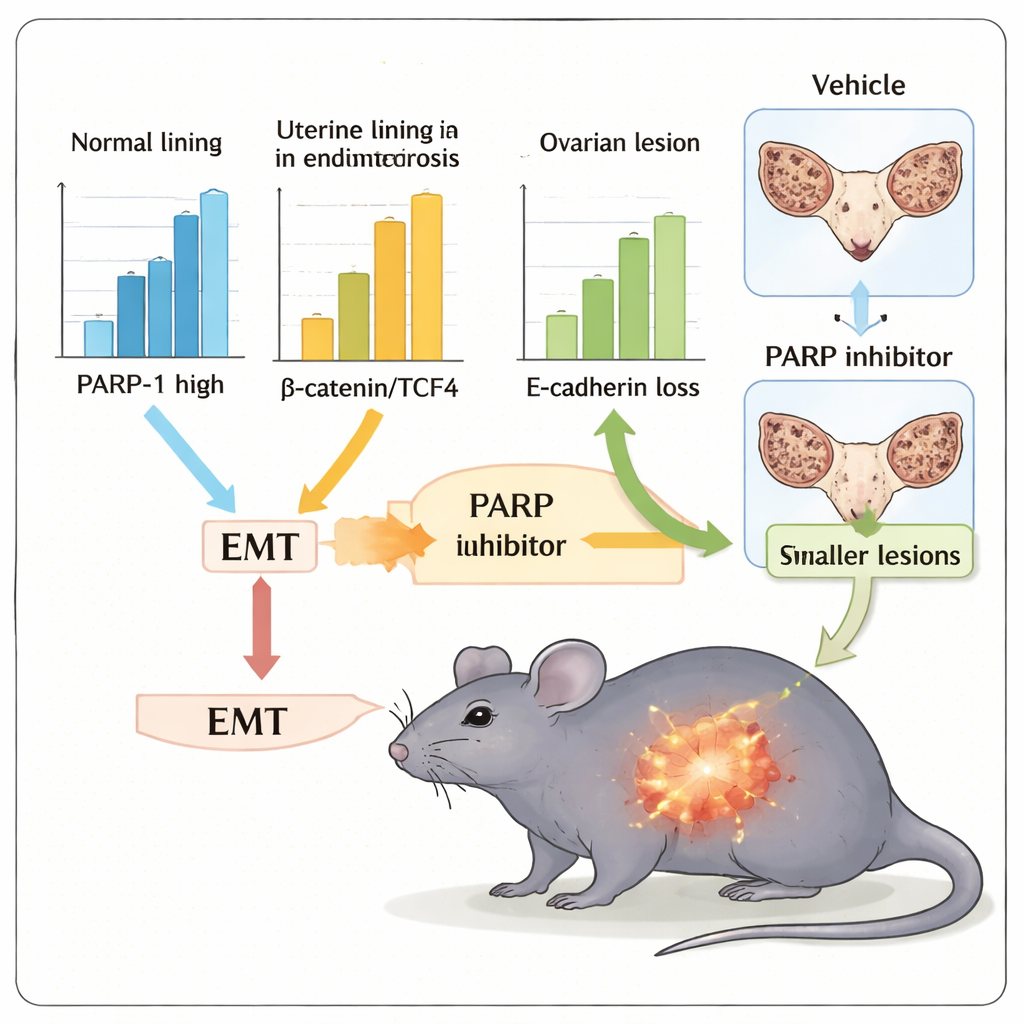
这对未来护理可能意味着什么
综合来自患者样本、细胞培养实验和小鼠模型的发现支持一个统一的观点:PARP‑1 起到一个可被药物靶向的枢纽作用,将 Wnt/β‑连环蛋白信号与子宫内膜异位症中的 EMT 样行为耦合起来。PARP‑1 并非单一的主控开关,而是炎症、氧化应激和激素驱动信号等更大网络中的关键连接点,共同塑造病灶的生长与侵袭方式。由于已有 PARP 抑制剂问世,这项工作提出了重新利用或改造这些药物的可能性——或许与其他通路或免疫靶向药物联合使用——以减少病灶负担、瘢痕形成并可能减轻对生育力的影响。需要更大规模和更长期的研究,但这项研究为针对数百万女性的疾病开辟了通向更具针对性、基于机制的治疗的切实路径。
引用: Zhang, L., Li, X., Kong, L. et al. PARP-1 couples β-catenin/TCF4 signaling to epithelial–mesenchymal transition in endometriosis. Sci Rep 16, 6940 (2026). https://doi.org/10.1038/s41598-026-38335-8
关键词: 子宫内膜异位症, PARP-1, 上皮–间质转化, Wnt/β-连环蛋白, PARP 抑制剂疗法