Clear Sky Science · zh
一种结合人工智能的流动腔室新方法,用于量化红细胞渗透脆性
为什么红细胞脆性很重要
每秒都有数百万红细胞挤过毛细血管,同时运送氧气。细胞在应激下多容易破裂——称为它们的“脆性”——可以反映贫血、血液保存问题以及严重感染(如败血症)的并发症。本研究介绍了一种现代化的、人工智能辅助的显微装置,它测量红细胞在盐溶液中解体的速度,旨在使这一重要检测更快、更精确,并便于在科研实验室以及未来的医院中使用。
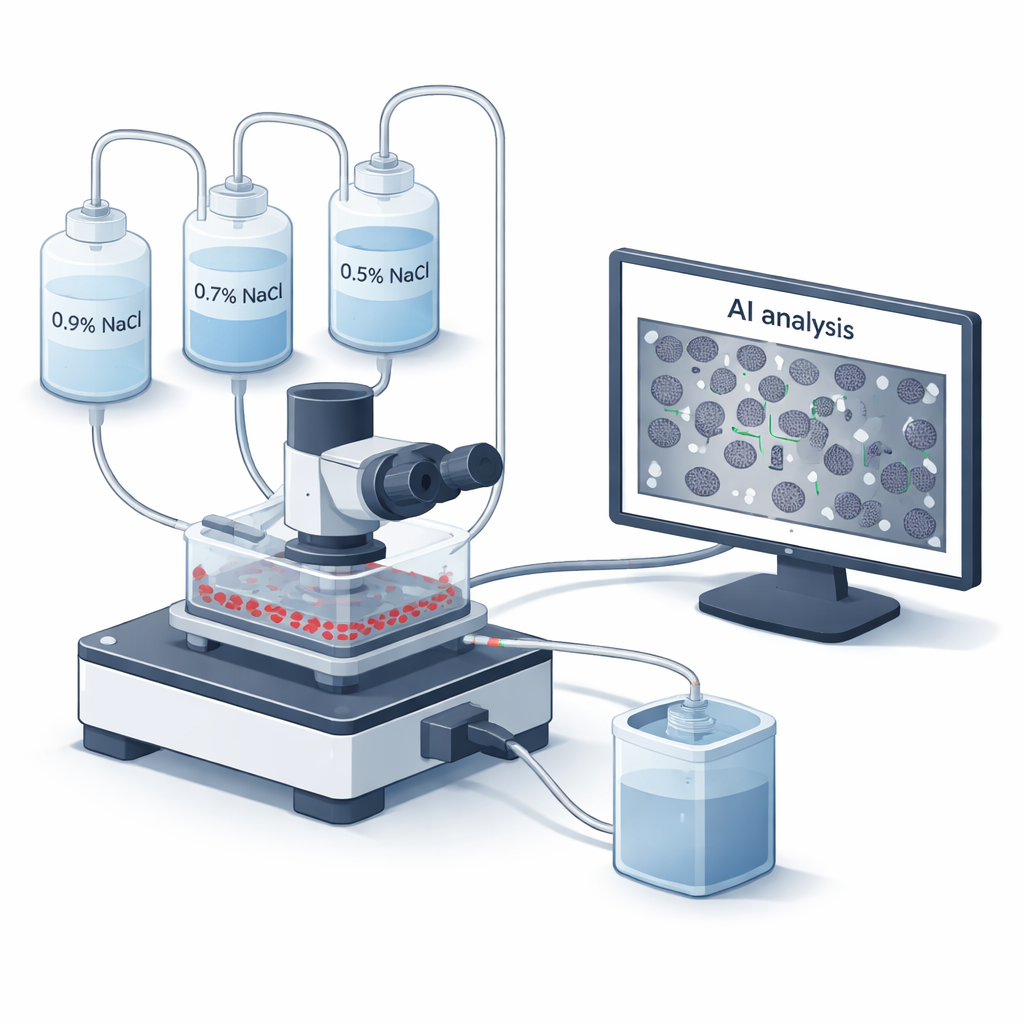
一种观察受压下血细胞的新方法
自20世纪40年代以来,医生就使用渗透脆性试验来评估红细胞膜的稳固性。传统上,将血液与一系列盐溶液混合,用仪器读取细胞破裂时逸出的血红蛋白量。尽管可靠,这种经典方法速度慢、依赖人工操作,且无法看到单个细胞在破裂时的形态变化。论文团队构建了一种新的微流控“流动腔室”系统,名为BioExP,它将红细胞在经处理的玻片上铺成单层。不同盐溶液被泵过这层细胞,同时显微镜和相机实时记录发生的变化,内置软件利用人工智能计数每个盐浓度下仍然完整的细胞数量。
将人工智能与流速控制进行验证
为评估BioExP是否可信,研究人员用来自四位健康供者的血样将其与传统分光光度法进行了直接对比。他们关注的关键指标称为MCF₅₀:即一半红细胞发生溶血时的盐浓度。首先,他们需要调校新系统,确定最佳的“饱和时间”——在给定低盐溶液中暴露细胞多长时间,使最脆弱的细胞已发生溶血而不过度延长。通过追踪在0.4%盐溶液中15分钟内消失的细胞数,他们发现近80%的溶血发生在最初三分钟内。这个三分钟窗口成为了他们的标准暴露时间,在速度与可靠测量之间取得了平衡。
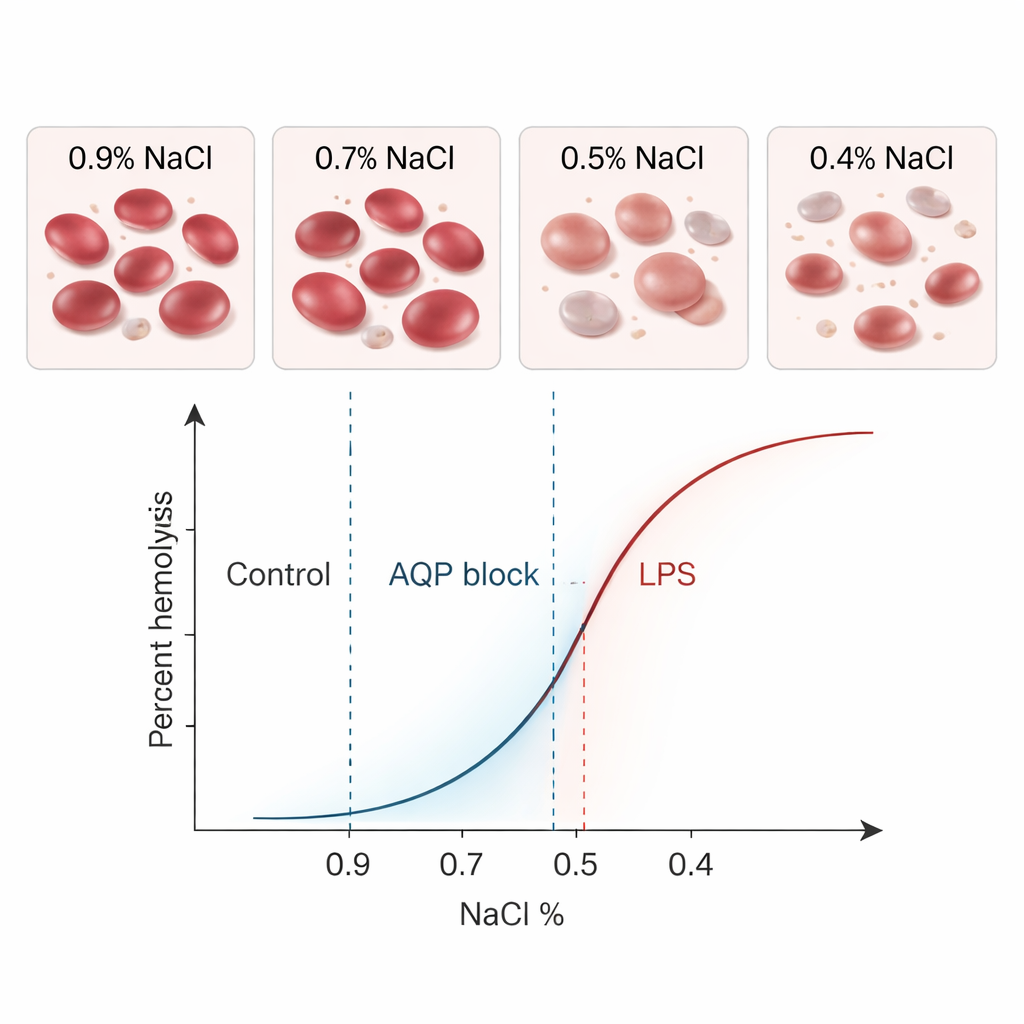
与经典检测的匹配及对真实生物学的探究
在用两种方法检测相同健康样本时,BioExP与经典试验得到的平均MCF₅₀值几乎相同——均为0.41%盐,且变异性相近。统计分析显示两种方法之间无显著差异,大多数配对结果落在狭窄的一致性范围内。换言之,新设备在很大程度上与既有方法“说同一种语言”。然而,BioExP的真正优势在于它能够测试不同条件如何改变细胞脆性。研究人员选择了两种生物学上重要的修饰因子:氯化汞,它阻断细胞膜中的水通道蛋白(称为水通道蛋白),以及与败血症相关的细菌脂多糖(LPS)毒素。
毒素与水通道如何改变细胞坚韧性
阻断水通道使红细胞不易破裂:MCF₅₀向左移,意味着细胞在更低盐浓度下仍能耐受而不破裂。BioExP和经典方法都清晰地检测到了这一左移。LPS则产生相反的影响。当红细胞在无血浆条件下高剂量孵育LPS时,它们变得更脆弱,在更高盐浓度下就会破裂。在显微镜下,许多细胞形态发生变化,变得更球形或出现刺状——这些是细胞膜受损的视觉信号。同样,两种方法在脆性曲线上都记录到了显著的右移。在所有这些测试中,新型流动腔室系统始终追踪到与旧方法相同的生物学趋势,仅在绝对值上略低、且为小而系统性的差异。
这对患者与实验室意味着什么
BioExP平台将检测时间从数小时缩短到不足一小时,仅需极少量血样(可能仅为指尖采血),并用人工智能自动完成计数和曲线拟合,减少了大量手动步骤。由于它随时间成像同一批细胞,能够将细胞形态变化与易碎性联系起来,并能在一次运行中测试多种盐浓度或药物条件。研究表明,这种现代方法在匹配经典渗透脆性测试准确性的同时,提供了更快的速度、更多的灵活性和丰富的视觉细节。如果在更大且多样化的供者群体中进一步验证,此类系统可能成为诊断溶血性贫血、监控血库保存血液以及研究感染或新药如何削弱或保护红细胞的有价值工具。
引用: Fırat, I.S., Alaçayır, Ö., Creutz, T. et al. A novel AI-coupled flow chamber method quantifying erythrocyte osmotic fragility. Sci Rep 16, 7175 (2026). https://doi.org/10.1038/s41598-026-38322-z
关键词: 红细胞, 渗透脆性, 微流控, 败血症, 人工智能