Clear Sky Science · zh
来自骨髓间充质干细胞的外泌体通过减轻炎症和细胞凋亡促进放射性皮肤损伤的修复
为什么放疗后受损皮肤需要新方法
许多接受放射治疗的癌症患者会出现疼痛的皮肤问题,这些问题在治疗结束后仍可能长期存在。常见症状包括红肿、脱皮、溃疡甚至难愈的伤口,而目前临床上缺乏能让皮肤真正恢复的针对性治疗。该研究探讨了一种有前景的生物治疗方法:来自骨髓干细胞的微小修复囊泡,以及它们如何平息放射损伤的皮肤并帮助其重建。
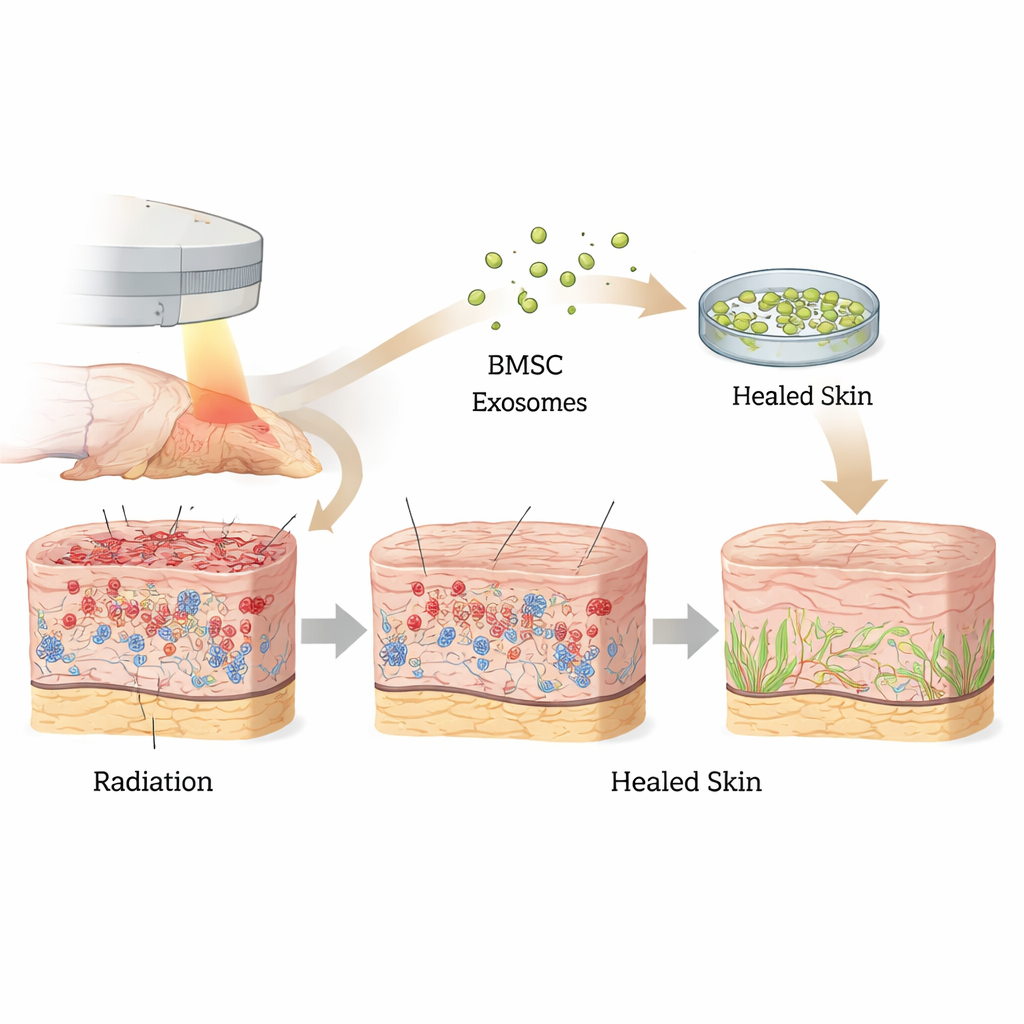
来自修复型细胞的微小信使
我们的骨髓中含有间充质干细胞,这类成体干细胞参与维持和修复多种组织。这些干细胞不仅通过分化成新细胞发挥作用,还不断释放纳米级的囊泡,称为外泌体。每个外泌体都是由膜包裹的载体,携带可改变受体细胞行为的蛋白质和遗传物质。由于外泌体是无细胞的且相对稳定,它们正在被研究作为比干细胞移植更安全、更易控制的组织修复替代方案。
构建一个逼真的放射性皮肤损伤模型
为了评估这些外泌体是否能促进放疗后的愈合,研究人员建立了大鼠放射性皮肤损伤模型。研究者对后肢皮肤施加了聚焦高剂量电离辐射,以模拟严重的治疗相关损伤。接下来的几天里,受影响皮肤出现了剧烈红肿、溃疡和渗液——这些都是严重放射性皮炎的典型表现。在照射后第十天开始,部分大鼠在受伤区域附近皮下注射了骨髓干细胞外泌体,另一些则仅注射生理盐水。随后团队在三周内密切追踪伤口的变化。
可见和显微镜下的更好愈合迹象
接受外泌体治疗的大鼠在皮肤创面闭合速度和完整性方面均优于未治疗组。总体伤口面积缩小更快,标准评分系统显示外泌体组的放射损伤严重程度稳步下降。皮肤的显微镜检查提供了更多线索。未治疗动物的表皮破损,毛囊和其它结构丢失,胶原纤维——赋予皮肤强度的结构纤维——稀少且紊乱。接受外泌体治疗后,表皮开始重建,炎症细胞减少,胶原变得更致密、排列更有序,更接近正常皮肤的状态。
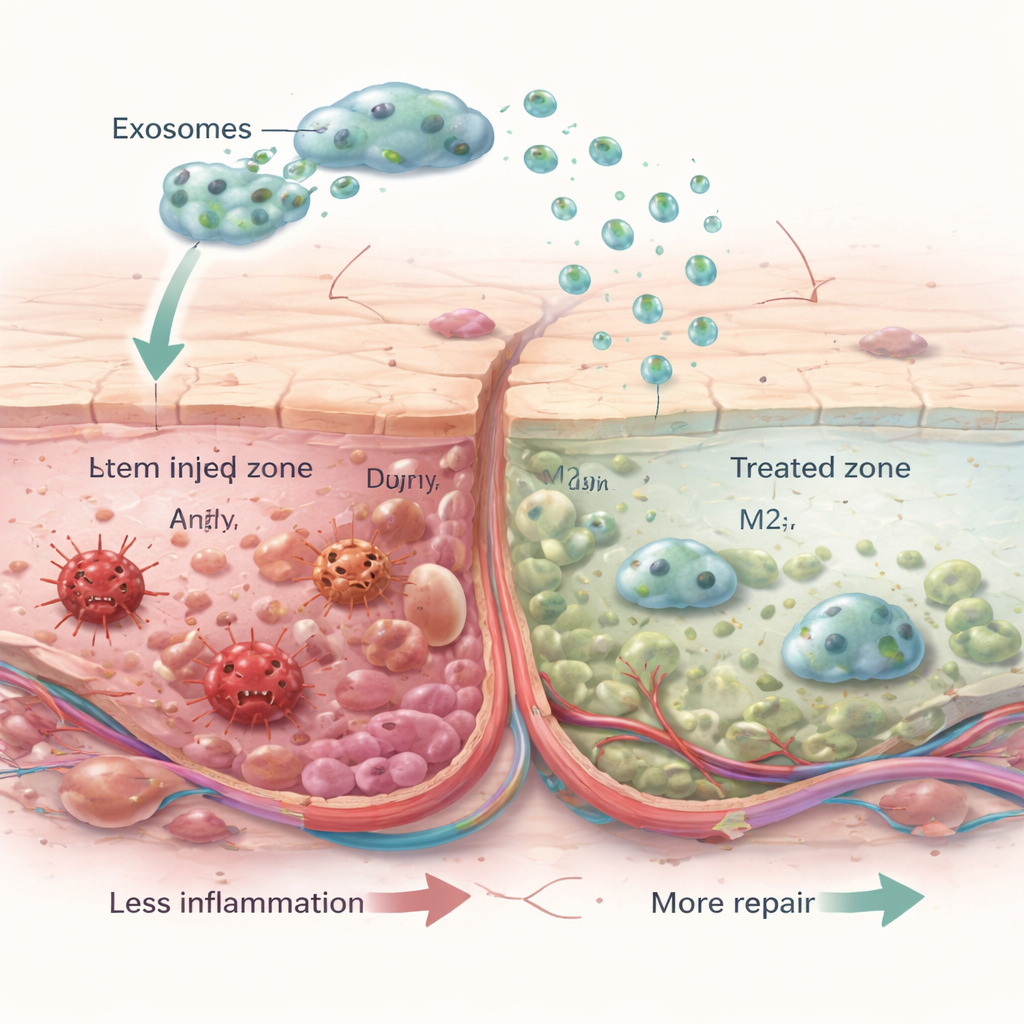
抑制炎症、促进血管生长并挽救细胞
研究还考察了组织免疫与血管系统内部发生的变化。辐射通常会引发长期存在的侵袭性免疫细胞集合,它们释放大量促炎信号并阻碍修复。外泌体处理的皮肤中,此类促炎细胞减少,而更多呈现清理和重建功能的温和免疫细胞增加。促炎分子如TNF‑α和IL‑1β下降,而抗炎信号IL‑10上升。与此同时,新生和成熟血管的标志物增加,提示外泌体有助于恢复为伤口输送氧气和营养的小血管。最后,程序性细胞死亡的检测显示治疗组皮肤细胞的死亡减少,且一个重要生长通路(常称为Akt)中的关键存活蛋白活性增强。
这对接受放疗的人可能意味着什么
综合来看,这些发现表明骨髓干细胞外泌体像是针对放射损伤皮肤的智能修复信号。它们似乎将局部环境从慢性炎症和持续细胞死亡的状态,转向平稳重建和血供改善。尽管这些工作在大鼠身上完成,关于确切参与的分子及最佳给药方式仍有许多未知,但它指向了这样一个未来:可以使用患者自身或供体的干细胞外泌体,以针对性、无细胞的方式预防或治疗严重的放射性皮肤损伤。
引用: Wen, Y., Song, Y., Pan, S. et al. Exosomes derived from bone marrow mesenchymal stem cells facilitate repair of radiation-Induced skin injury by attenuating inflammation and apoptosis. Sci Rep 16, 6918 (2026). https://doi.org/10.1038/s41598-026-38306-z
关键词: 放射性皮肤损伤, 间充质干细胞, 外泌体, 伤口愈合, 炎症