Clear Sky Science · zh
熊去氧胆酸通过TGR5/NF-κB信号通路缓解α-酪蛋白诱导的牛奶蛋白过敏
为什么婴儿乳制品过敏很重要
对许多家庭来说,婴儿健康出现问题的第一个迹象常是喂养后发生令人惊恐的呕吐、腹泻或带血的大便。最常见的罪魁之一是牛奶蛋白过敏,即婴儿的免疫系统对乳中的蛋白质发生过度反应。本研究探讨了一种由胆汁衍生的天然物质——熊去氧胆酸(UDCA)——如何通过修复肠道屏障并抑制炎症来缓解这类过敏反应。
牛奶、微生物与过度活跃的肠道
牛奶蛋白过敏通常表现为肠胃问题,而非剧烈的肿胀或风团。结肠下段发生炎症,肠道保护性上皮受损,婴儿可能无法正常增长体重。近年来,科学家发现肠道中数以万亿计的细菌及其代谢产物与这些问题密切相关。早期研究中,作者发现患有此类过敏的婴儿体内几种由肠道微生物生成的“次级胆汁酸”水平偏低,尤其是UDCA,这提示这一缺失分子可能在控制肠道炎症中具有重要作用。
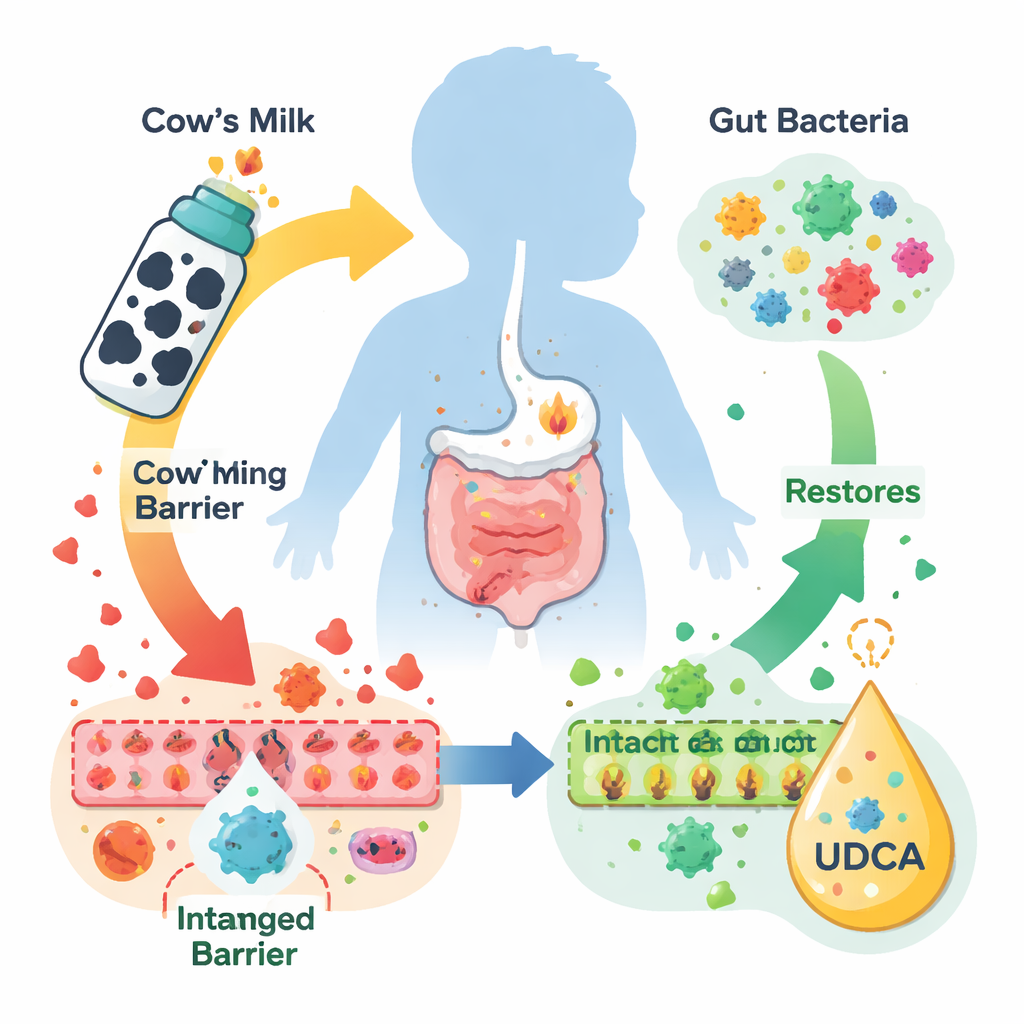
用于模拟乳制品过敏婴儿的小鼠模型
为检验UDCA的作用,研究人员用α-酪蛋白(乳中常引发强烈反应的主要蛋白之一)建立了牛奶蛋白过敏的小鼠模型。反复暴露于α-酪蛋白的小鼠出现了典型过敏体征,如喘鸣、剧烈搔抓和体重增长受损。显微镜下检查发现,其肝脏有损伤并有免疫细胞浸润,结肠出现溃疡、腺体畸形以及分泌粘液的杯状细胞减少,而这些杯状细胞通常有助于保护肠壁。给小鼠口服UDCA,尤其是中等剂量时,可缓解临床症状,帮助恢复体重,并在很大程度上恢复肝脏和结肠的正常结构,包括杯状细胞数量和封闭邻近肠上皮细胞的紧密连接完整性。
降低免疫“火焰”
研究团队接着探讨UDCA如何改变免疫反应。在过敏小鼠的结肠中,编码强效炎性信使分子(如IL-1β和TNF-α)以及招募更多免疫细胞入组织的若干趋化因子的基因被强烈激活。UDCA处理显著降低了这些基因的活性,并提高了编码紧密连接蛋白occludin的基因表达。聚焦于巨噬细胞——既清除损伤又协调炎症的免疫细胞,研究者表明UDCA在培养条件下改善了它们的迁移和“修复”能力,同时减少了炎性分子、一氧化氮和活性氧的产生,这些产物可能损伤周围组织。
免疫细胞内的分子刹车
在分子层面,UDCA通过一种名为TGR5的受体发挥作用,该受体存在于巨噬细胞及其他细胞表面。在过敏小鼠中,结肠中TGR5水平下降,而驱动炎性基因表达的主控开关NF-κB的活性上升。UDCA逆转了这一模式:它增加了TGR5、提高了细胞内信使分子cAMP的水平,并阻断了NF-κB组分p65进入细胞核(p65进入核内会开启炎性基因)。当研究者加入一种特异性阻断TGR5的药物时,UDCA便无法有效抑制NF-κB或减少细胞因子产生,这表明该受体是其作用的关键部分。在暴露于α-酪蛋白的巨噬细胞系中也观察到类似效应,进一步支持相同通路在肠道免疫细胞中发挥作用的观点。
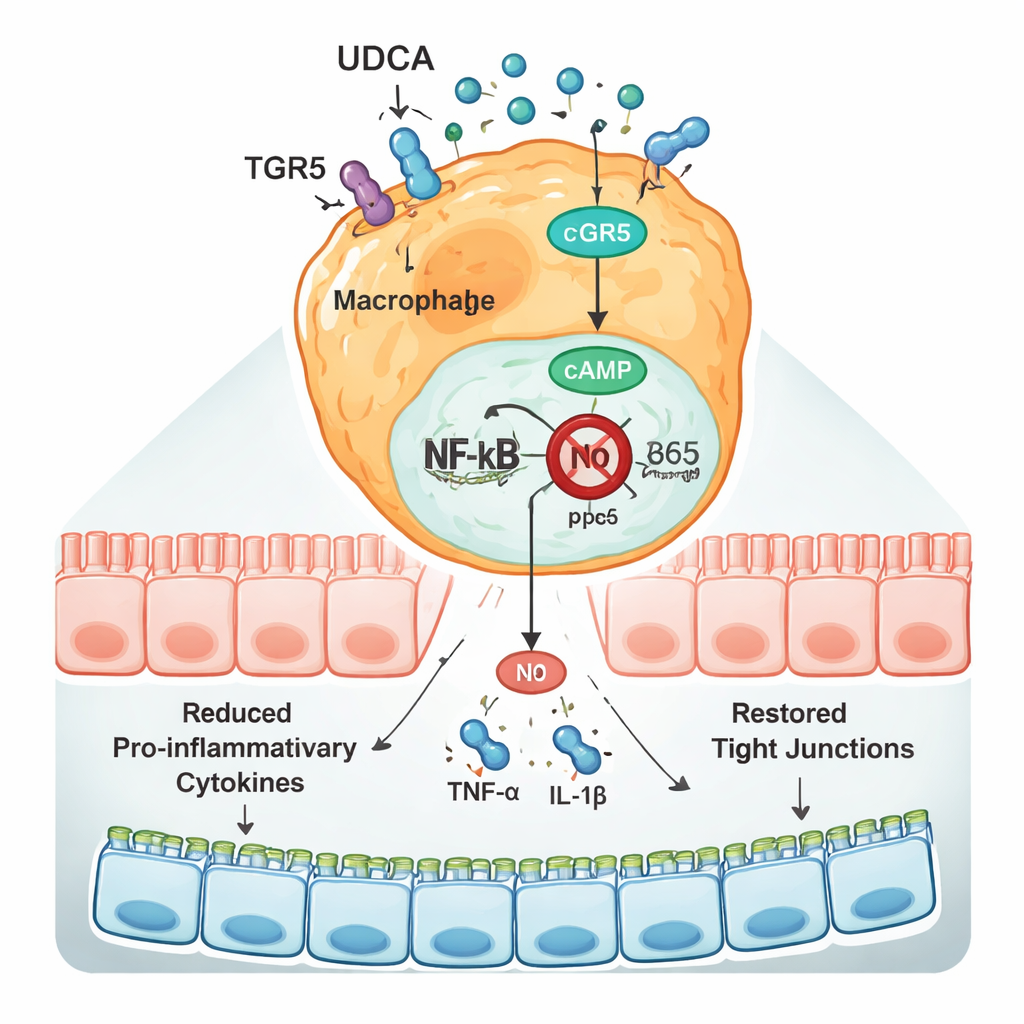
这对儿童可能意味着什么
简言之,这项工作表明UDCA——一种我们自身和肠道微生物都能生成的分子——通过加强肠道屏障并将巨噬细胞重新编程为较不具攻击性、更偏向修复的状态,帮助“冷却”由牛奶引发的肠道过敏。其主要机制是激活TGR5,进而对助长炎症的NF-κB系统施加抑制。尽管这些发现来自小鼠和细胞培养,但它们提示UDCA或能提高其水平或模拟其作用的疗法,可能成为未来缓解牛奶蛋白过敏乃至其他肠源性过敏性疾病的策略。在此类治疗进入临床之前,还必须在人体中进行更多研究,并仔细研究UDCA与发育中肠道微生物群的相互作用。
引用: Yu, Z., Wang, Z., Yue, L. et al. Ursodeoxycholic acid alleviates α-Casein-induced cow’s milk protein allergy via the TGR5/NF-κB signaling pathway. Sci Rep 16, 7808 (2026). https://doi.org/10.1038/s41598-026-38293-1
关键词: 牛奶蛋白过敏, 熊去氧胆酸, 肠道微生物群, 肠道炎症, 巨噬细胞