Clear Sky Science · zh
异质图神经网络通过多组学整合揭示胎盘功能不全中叶酸缺乏的分子机制
这对母亲和婴儿为何重要
叶酸常被人们熟知为孕期维生素,有助于预防先天缺陷,但它在维持健康妊娠中的作用远不止于此。本研究考察了叶酸缺乏如何悄然损害胎盘——这一为胎儿提供营养与保护的器官。研究者将尖端生物学技术与先进的人工智能相结合,展示了基因、蛋白质和小分子如何相互作用,共同导致胎盘营养和功能不足,并探讨了这些发现将来如何帮助医生更早识别高风险妊娠。
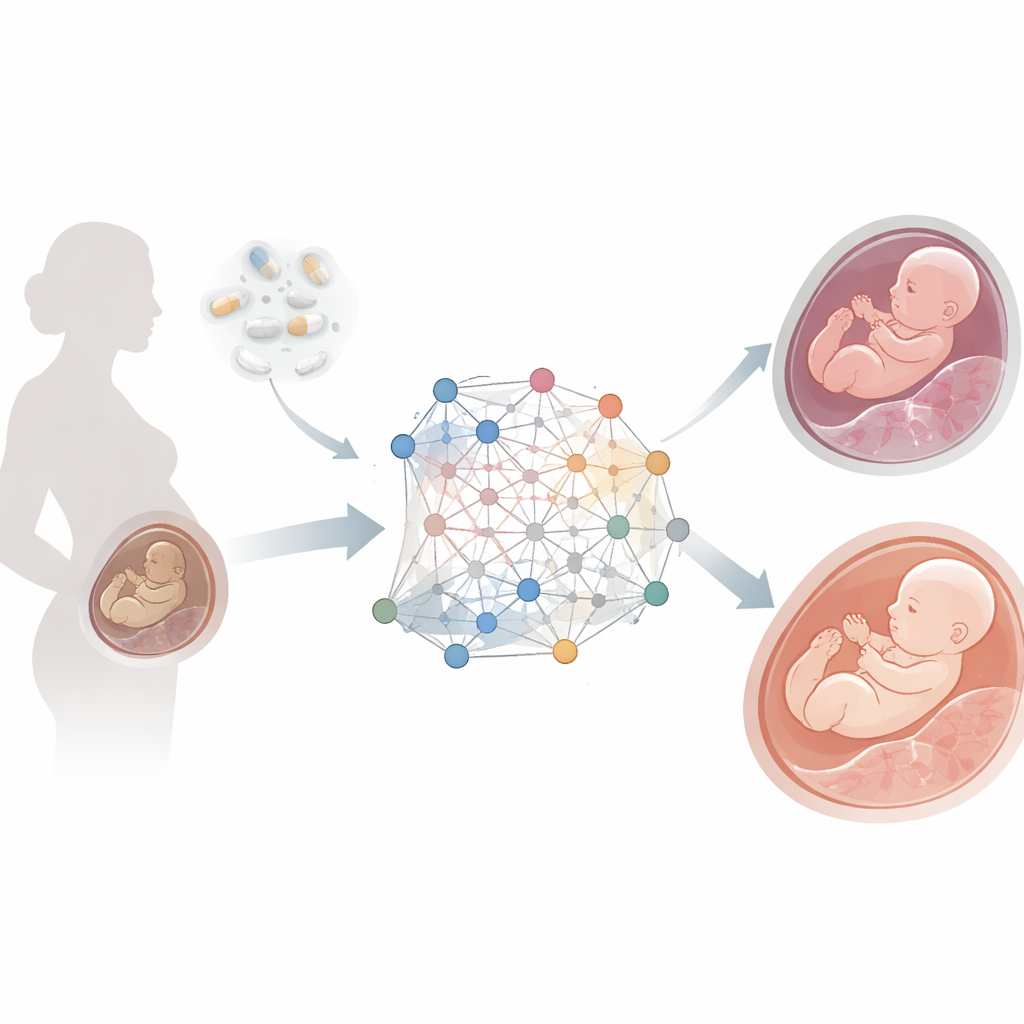
当胎盘无法跟上需求时
胎盘功能不全是指胎盘无法向胎儿输送足够的氧气和营养,进而引发生长受限、妊娠高血压(子痫前期)和早产等并发症。全球约有五到十百分比的妊娠受其影响。叶酸参与多种细胞过程——构建DNA、调控基因的开启与关闭,以及支持血管健康。当叶酸水平过低时,这些系统可能失常,但在胎盘组织中具体的连锁反应难以追踪。传统研究通常一次仅检查一种生物学数据类型,比如基因或代谢物,因此难以把握这些层级如何相互作用的全貌。
用多重视角解读胎盘
为应对这一复杂性,研究团队在分娩时收集了来自156例与叶酸相关的胎盘功能不全妊娠和142例健康对照的胎盘样本。从每个样本中,他们测量了四类不同的分子信息:DNA变化、基因活性、蛋白质水平和小分子代谢物。他们没有把这些测量结果当作孤立的长列表,而是将其链接成一个包含6,704种分子和超过16,000条已知相互作用的大型生物网络。基因、蛋白质和代谢物被表示为不同类型的节点,边则反映了它们在真实细胞中如何结合、调控或相互转化。
训练智能网络识别异常
随后,研究人员在该分子网络上训练了一种特殊的人工智能模型——异质图神经网络。与将每个测量项孤立看待的传统算法不同,该模型“倾听”信号如何在整个网络中传播。它分配注意力权重,以突出对区分病变与健康胎盘最有信息量的分子与连接。在保留测试集上,模型将94.7%的胎盘分类正确,ROC曲线下面积达0.978,接近完美,明显优于传统机器学习方法以及任何仅使用单一数据类型的分析。这表明疾病信号不仅存在于单个标志物中,而是分布于多个生物层级之间的模式中。
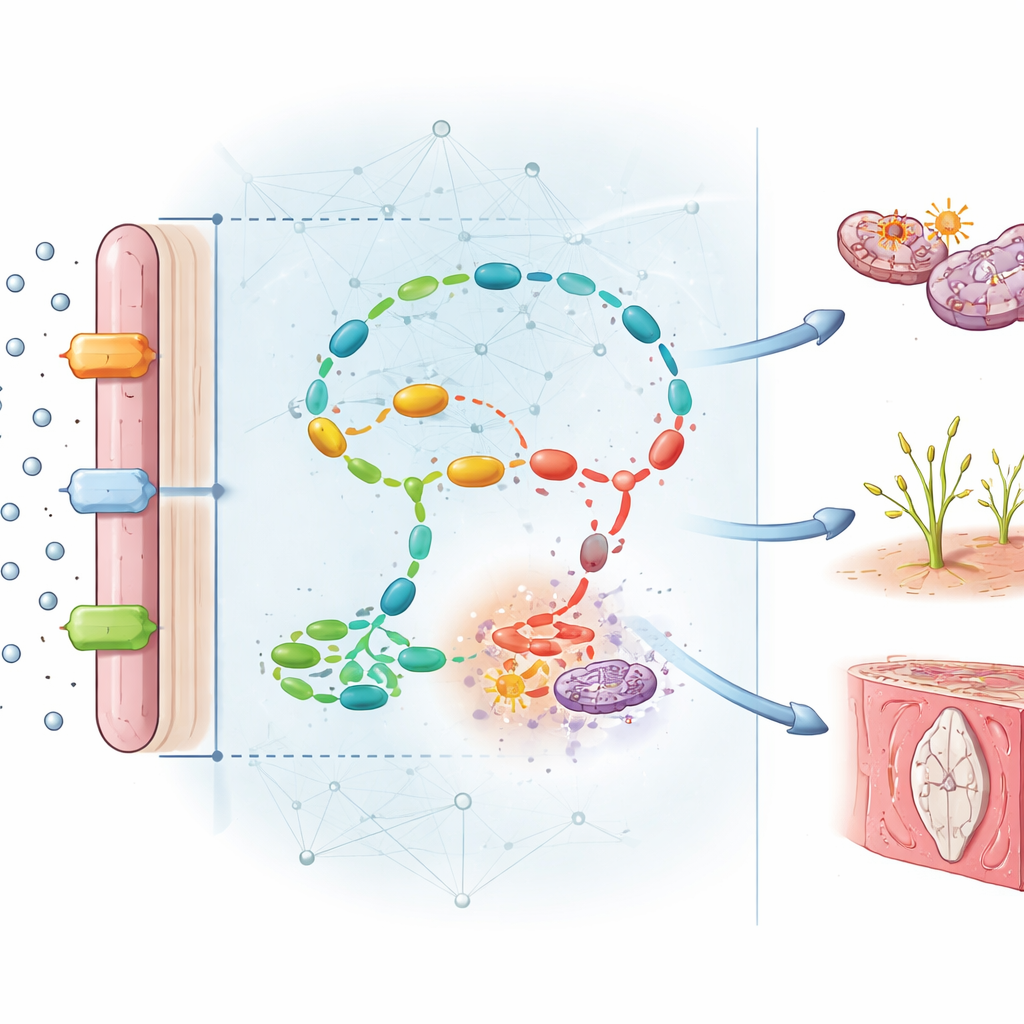
揭示隐匿的损伤链条
除了预测能力外,模型的设计还使作者能够识别在决策中起主导作用的分子。有若干分子特别突出。关键的叶酸处理组分——例如酶MTHFR和叶酸转运蛋白FOLR1——在病变胎盘中显著降低,而有毒副产物同型半胱氨酸的积累则超过六倍。网络分析揭示出七个主要功能模块,将紊乱的叶酸代谢与DNA甲基化减少、氧化应激增加、血管生成受损、炎症以及过度细胞死亡联系起来。换言之,叶酸缺乏并非以单一方式损害胎盘,而是引发一系列相互关联的故障,共同限制了对胎儿的血流和营养供给。
这对未来护理可能意味着什么
目前,这项工作主要是一个强大的显微镜工具,而非床边检测手段。由于所有样本均在分娩时采集,模型尚不能用于妊娠期间的风险预测——而那正是干预最关键的时刻。尽管如此,它揭示的分子特征——尤其是叶酸转运改变、同型半胱氨酸积累和受损血管生成通路的联合变化——为寻找可能反映胎盘状况的血液标志物提供了路线图。通过未来随访母亲并将其血液与胎盘组织进行比较的研究,这一方法有望助力构建早期、无创的筛查工具以及更为个体化的营养或医疗策略,以保护脆弱妊娠。
引用: Xie, X., Li, Z., Xiao, Q. et al. Heterogeneous graph neural networks reveal molecular mechanisms of folate deficiency in placental insufficiency through multiomics integration. Sci Rep 16, 8417 (2026). https://doi.org/10.1038/s41598-026-38288-y
关键词: 胎盘功能不全, 叶酸缺乏, 图神经网络, 多组学, 妊娠并发症