Clear Sky Science · zh
基于EfficientNetB0的多级注意力DeepLab V3+用于MRI扫描中胃肠道器官分割
更精准地瞄准肿瘤
当医生用放射线治疗消化系统的癌症时,需要在两端之间取得微妙的平衡:尽量强力打击肿瘤,同时保护附近的健康器官,如胃和肠道。目前,在每次磁共振成像(MRI)扫描上由人工逐层勾画这些器官,通常每位患者每天可能需要耗费长达一小时。本文介绍了一种自动在MRI图像中描绘这些器官的计算机视觉系统,有望加快、更精确地制定治疗计划并减少患者的副作用。
为何绘制肠道位置很重要
胃肠道癌症常见且致死率较高,总体生存率约为30%。放射治疗是主要治疗手段之一,但消化道在腹腔内排列紧密,健康器官会出现日常的小幅位移。为避免损伤胃、小肠和大肠,专家必须在每次治疗前准确判断它们的位置。人工勾画既耗时又容易在不同专家之间产生差异。一种自动且可靠的勾画方法可以缩短就诊时间,使医生能够治疗更多患者,并提高放射剂量的安全性与准确性。
教计算机“读懂”MRI
研究人员构建了一个人工智能模型,学习在MRI扫描中识别三种关键的消化器官:胃、小肠和大肠。他们在UW–Madison胃肠道数据集上训练该模型,这是唯一公开提供腹部MRI上详细器官轮廓的集合。该数据集包含来自85位患者的38,496张图像,并配有精心准备的标签,标注了每种器官出现的位置或无器官存在的区域。为充分利用这一相对较小的样本,研究组按患者划分数据(确保模型在训练和测试中不会见到同一人),并通过翻转、旋转、调亮和轻度扭曲图像来扩充数据集。这些受控的变换帮助系统应对真实世界中患者体位、图像亮度和细微形态差异的变化。
新型AI模型如何识别模式
在模型内部,结合了若干现代图像识别的思想以提高其对解剖结构的“观察”能力。首先,一个紧凑的网络EfficientNet B0扫描每张图像并构建多层视觉特征——从简单的边缘到复杂的器官形状——同时保持较低的计算开销。接着,一个称为DeepLab V3+的结构在多尺度上分析图像,有点像放大和缩小视野以同时理解细节与整体语境。在此基础上,作者在多个细节层次加入了“注意力”机制。简单来说,注意力帮助系统决定图像的哪些部分和哪些内部信号应被赋予更高权重,以便聚焦那些细微但重要的线索,例如将胃与小肠的回肠袢区分开来。最后,一个解码器阶段将这些线索拼接回一个干净的、全尺寸的掩码,显示出三种器官的位置。
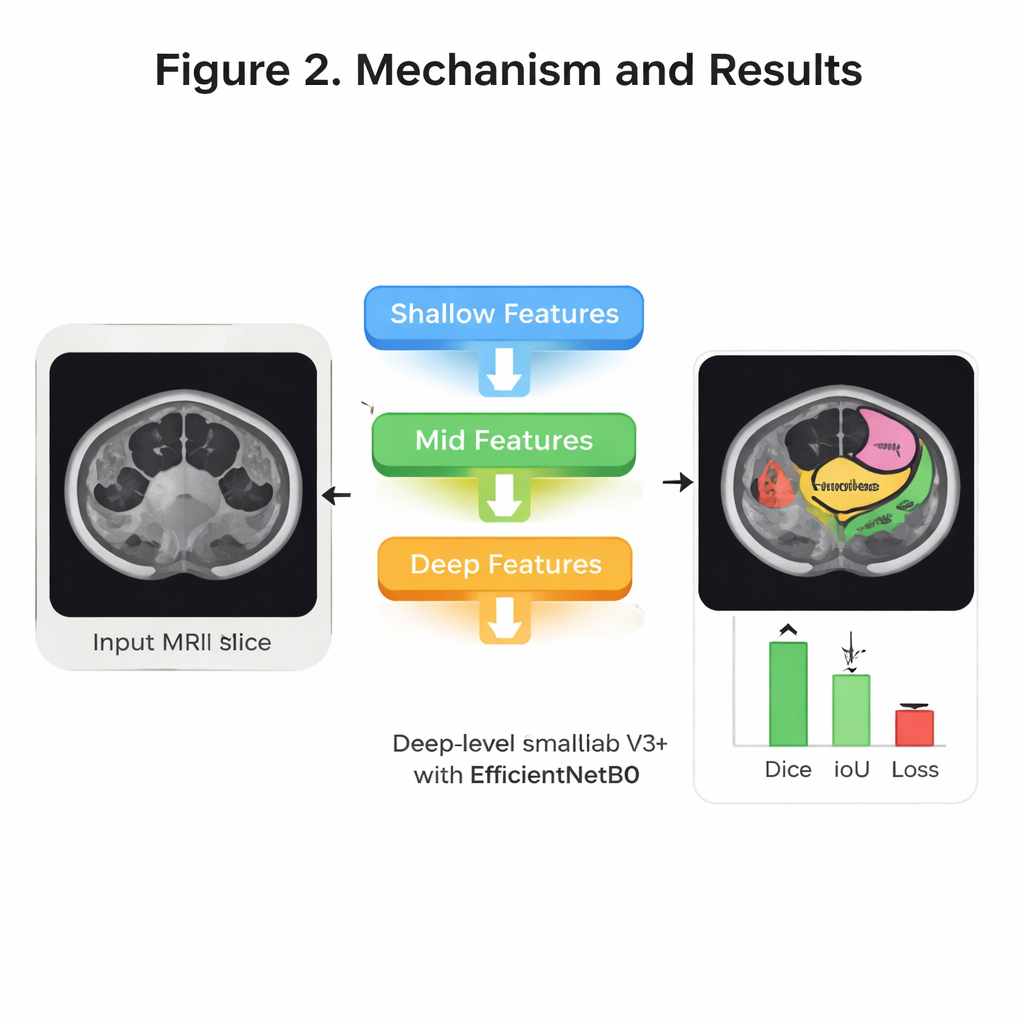
准确性与效率测试
团队系统地调整了训练策略——尝试不同的优化方法、训练轮数以及验证时的数据划分方式。他们的最佳配置使用了名为RMSprop的优化器、四折交叉验证和30轮训练。在留出的测试患者上,模型在总体上正确标记了超过99%的像素,并与专家绘制的轮廓表现出高度重合。一个广泛使用的重合度量Dice系数在三种器官上的平均值约为94%,而另一相关指标交并比(Intersection over Union)约为92%。对医院使用而言同样重要的是,该系统相对轻量:大约有8.3百万可训练参数,并能在约31毫秒内处理一张典型的224×224 MRI切片,足以在日常治疗计划中提供近实时支持。
这对患者可能意味着什么
简而言之,这项研究表明,经过精心设计的AI可以可靠地在MRI影像上勾画出胃和肠道,达到与专家相当的表现,同时速度更快且更具一致性。这项能力可以帮助放疗科医生更精确地围绕敏感组织调整射束,从而在治疗期间减少不必要的损伤和副作用。尽管当前模型是在单一中心、以大多为健康解剖结构的扫描上训练的,但它为未来纳入病变器官和多中心数据的系统奠定了坚实基础。经过进一步测试和改进,此类工具有望成为放疗计划室中的常规助手,默默确保救命的放射照射准确命中最需要的位置。
引用: Sharma, N., Gupta, S., Al-Yarimi, F.A.M. et al. Multi-level attention DeepLab V3+ with EfficientNetB0 for GI tract organ segmentation in MRI scans. Sci Rep 16, 7546 (2026). https://doi.org/10.1038/s41598-026-38247-7
关键词: 胃肠道癌症, MRI分割, 放疗计划, 医学中的深度学习, 医学图像分析