Clear Sky Science · zh
抑制SHH通路并与星形胶质细胞共培养在胶质母细胞瘤及癌症干细胞中诱导不同反应
为什么脑肿瘤如此难治
胶质母细胞瘤是最致命的脑癌之一,即便采用手术、放疗和化疗,只有极少数患者能活过五年。原因之一是这些肿瘤并非由单一细胞类型构成。肿瘤中存在一小群特别顽固的“癌症干”细胞,它们能在治疗后幸存并促使肿瘤复发。本研究提出了关键问题:当阻断一个驱动生长的信号时,不同的肿瘤细胞如何响应?正常脑支持细胞——星形胶质细胞的存在又如何改变这种响应?
更近距离地观察肿瘤中最难对付的细胞
研究者使用了常见胶质母细胞瘤模型的两类主要细胞:肿瘤主体细胞和一小部分以CD133蛋白标记的亚群,这些亚群表现出类似癌症干细胞的特性。这类干样细胞分裂较少,体积更小且更圆,且比主体细胞形成更紧密的簇。团队还将肿瘤细胞与星形胶质细胞一同培养——这些星状细胞帮助维持健康的脑组织。这样的混合培养更接近真实的肿瘤环境,在那里癌细胞不断与周围细胞“对话”。 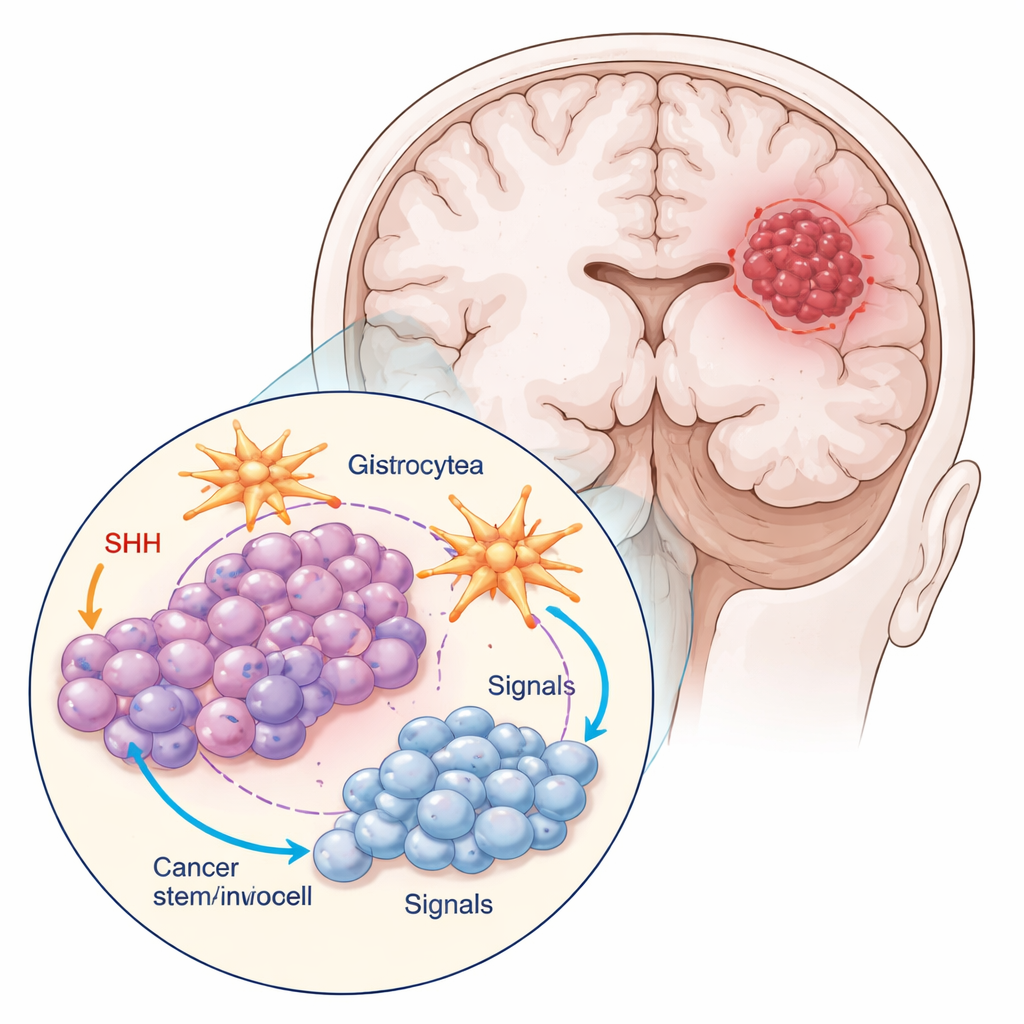
阻断肿瘤重新利用的发展信号
许多胶质母细胞瘤,尤其是其中的干样细胞,劫持了一个称为Sonic Hedgehog(SHH)的分子通讯通路,正常情况下该通路在脑发育过程中发挥作用。团队使用环蒿素(一种阻断SHH关键组分的化合物)来观察肿瘤主体细胞和癌症干细胞的反应。他们测量了与SHH相关的基因和蛋白活性、细胞周期进程速度以及细胞程序性死亡(凋亡)的频率。环蒿素对SHH信号的改变强烈依赖于细胞类型和是否存在星形胶质细胞。单独培养时,癌症干细胞产生的SHH信号最多,但当它们与星形胶质细胞共培养并暴露于药物时,这种分泌减少,表明周围的脑细胞可以抑制肿瘤的自我支持化学信号。
邻里环境如何改变增殖与死亡
除SHH本身外,研究团队还追踪了其他调控细胞继续分裂、暂停或开始分化的基因网络。在简单的肿瘤单培养中,阻断SHH使主体肿瘤细胞倾向于在分裂的后期阶段(G2/M期)停滞,而干样细胞则更倾向于在更早的静止或进入阶段(G0/G1期)累积。加入星形胶质细胞后,这些模式发生了变化:原本更静止的癌症干细胞转而出现G2/M阻滞,暗示在混合环境中作用的是另一套“刹车”机制。研究者还观察到与细胞命运和组织塑形相关的信号通路——例如WNT、BMP和TGF-β——在有无星形胶质细胞时,在主体细胞和干样细胞中的调控不同,这意味着微环境可以将细胞倾向于持续的干样行为或更分化、侵袭性较低的状态。
触发最具抵抗性的细胞走向死亡
研究进一步考察了细胞进行凋亡的难易程度。遗传学读数和DNA损伤感应检测(TUNEL实验)显示,环蒿素更偏向激活由CASP8驱动的“外源性”细胞死亡通路,尤其在癌症干细胞群体中表现明显。有趣的是,在单独培养的肿瘤细胞中,阻断SHH后总体细胞死亡有时反而减少,表明这些细胞可能激活备用的生存策略。相反,当干样细胞与星形胶质细胞共培养时,环蒿素增加了凋亡标志,表明周围的脑细胞在SHH信号被阻断后可以使这些本来顽固的细胞更易受损。 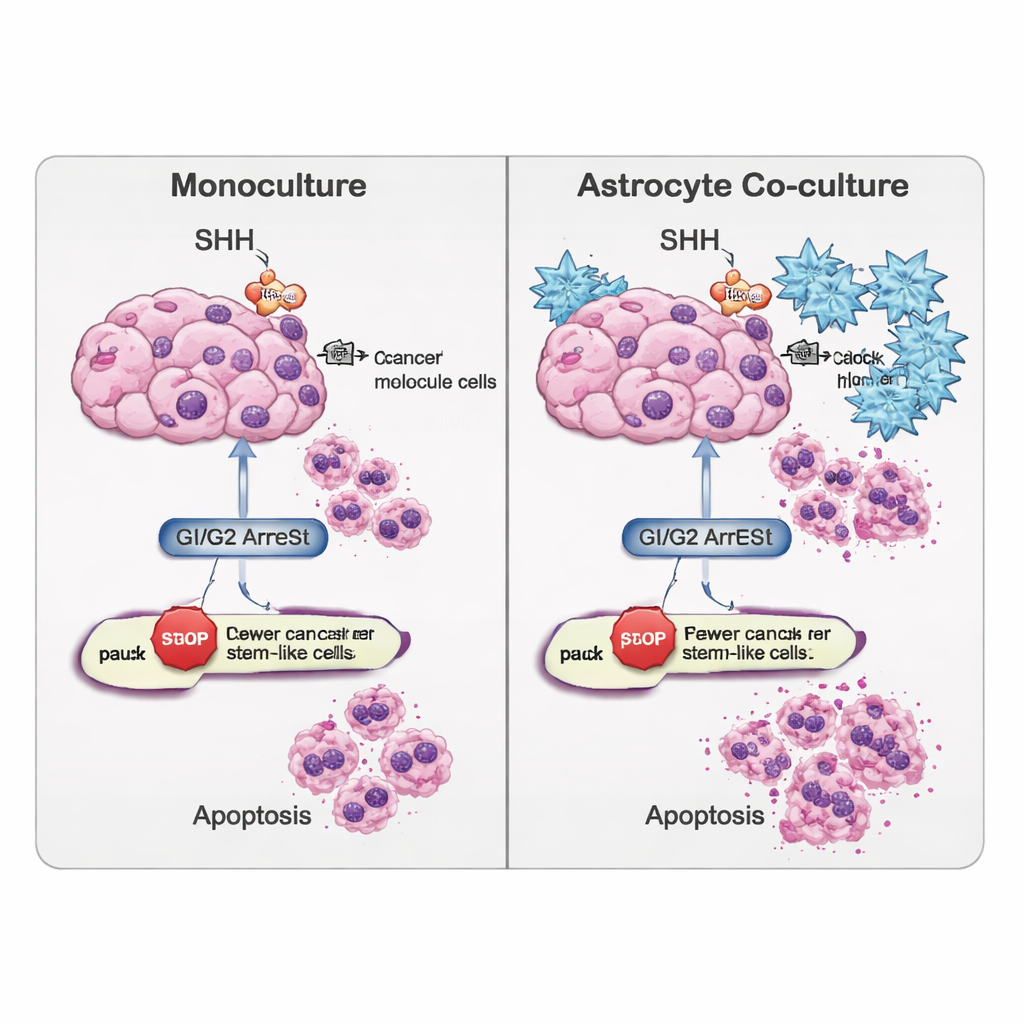
这对未来脑癌治疗意味着什么
对非专业读者来说,关键要点是:如果忽略肿瘤的“邻里”,仅针对单一生长信号来治疗胶质母细胞瘤是不够的。这项工作表明,与肿瘤共处的正常细胞——星形胶质细胞——能深刻改变肿瘤主体细胞和癌症干细胞对SHH通路抑制的响应。尤其是癌症干细胞,在有星形胶质细胞存在时更容易进入细胞周期停滞并走向一种细胞死亡形式。作者得出结论:针对SHH及相关通路的药物若要更有效,应在反映真实脑环境的条件下进行测试并最终使用,可能需要与攻击肿瘤备用生存通路的其他治疗联合使用。简言之,理解并利用肿瘤细胞与其邻居之间的“对话”可能为对抗这一难以战胜的癌症开辟更精确且更持久的策略。
引用: Kocaturk, D.C., Ozdil, B., Adali, Y. et al. SHH pathway inhibition and astrocyte co-culture induce distinct responses in glioblastoma and cancer stem cells. Sci Rep 16, 7712 (2026). https://doi.org/10.1038/s41598-026-38199-y
关键词: 胶质母细胞瘤, 癌症干细胞, Sonic Hedgehog通路, 肿瘤微环境, 星形胶质细胞