Clear Sky Science · zh
在Rd10小鼠中鉴定并验证与遗传性视网膜变性相关的新型铁死亡相关基因特征
为何眼细胞的死亡关系到我们每个人
视网膜色素变性是一组遗传性眼病,会逐步夺走患者的视力,通常先出现夜盲,最终可能导致完全失明。目前尚无治愈方法,现有的基因治疗只能惠及少数患者。本研究转向另一条思路:研究一种由铁和氧化损伤驱动的特殊细胞死亡方式——铁死亡,旨在发现可能在未来保护视网膜光感受细胞的新基因靶点——无论患者出生时携带何种突变。
从微观看致盲的眼病
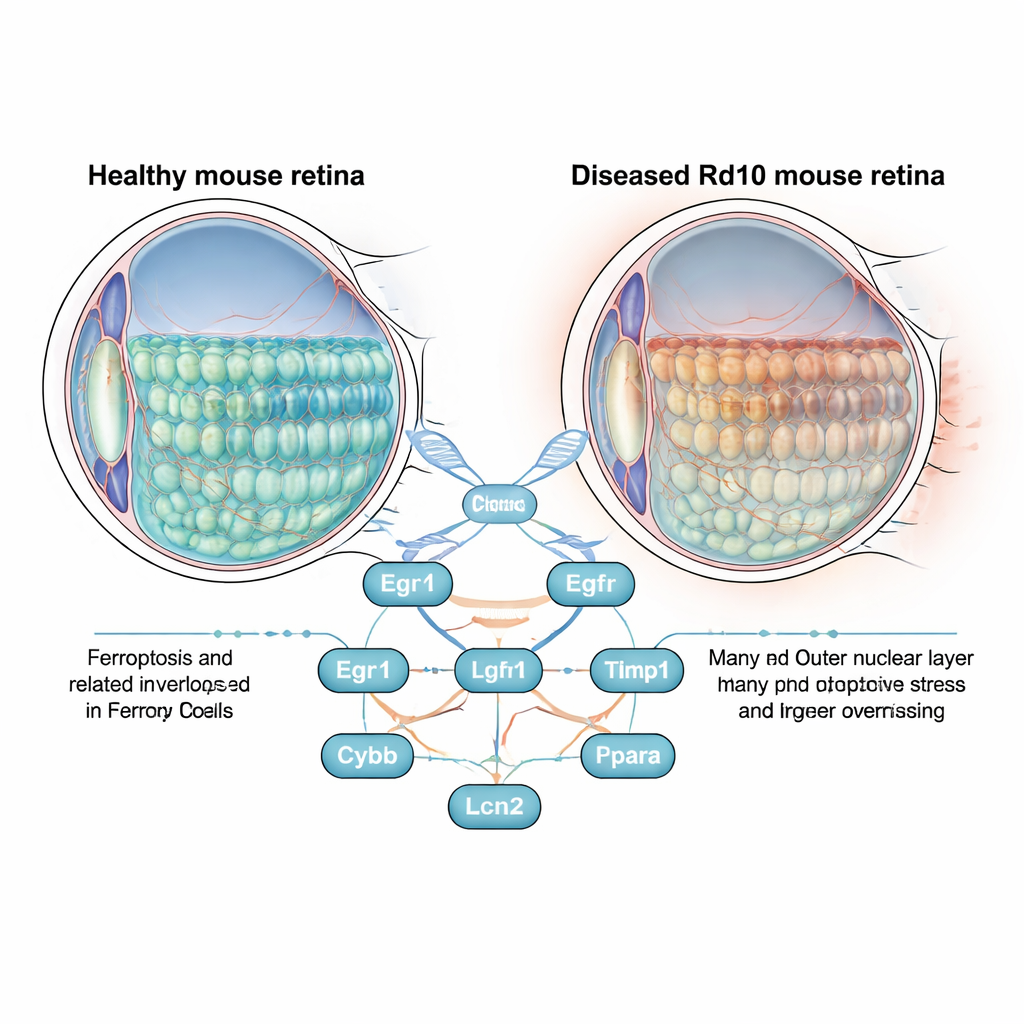
视网膜是位于眼后方的一层薄组织,包含杆状和锥状感光细胞,它们将光信号转换为电信号。在视网膜色素变性中,这些细胞会逐渐死亡,先导致夜间和侧向视力丧失,后影响中央视力。研究者常用携带与人类疾病高度相似突变的Rd10小鼠来研究这一过程。与其单纯关注致病基因,作者提出了更广泛的问题:随着视网膜退化,哪些与铁死亡相关的基因被上调或下调,它们是否在推动细胞丧失中起作用?
在海量数据中寻找关键基因
研究团队挖掘了来自健康与Rd10小鼠视网膜的大型公共基因表达数据集,本质上绘制了基因活动的全局“快照”。他们发现超过2000个基因发生变化,随后将这些基因与经过整理的铁死亡相关基因列表交叉比对,筛选出37个与铁驱动的氧化性细胞死亡相关的候选基因。生物信息学分析显示,这些基因在应对氧化应激、神经元死亡调控和脂质代谢等过程上聚集——这些都是铁死亡的特征,也是神经退行性过程中已知的应激反应。
突出的八个基因
为锁定最具影响力的候选基因,研究者构建了蛋白相互作用网络并应用多种排序算法。最终确定了八个“枢纽”基因:Egr1、Cd44、Egfr、Tlr4、Timp1、Cybb、Lcn2 和 Ppara。其中七个在病变视网膜中上调,而Ppara则下调。研究组在独立数据集中验证了这些模式,随后进一步考察了这些优势基因在眼内的位置分布。通过荧光染色和单细胞RNA测序,他们显示Egr1在杆状和锥状感光细胞中显著上升,而Cd44在跨越视网膜的支持性胶质细胞——穆勒细胞中明显升高。这提示受压的感光细胞与其支持细胞可能通过与铁死亡相关的通路相互作用——且这种相互作用可能是有害的。
对未来治疗的意义
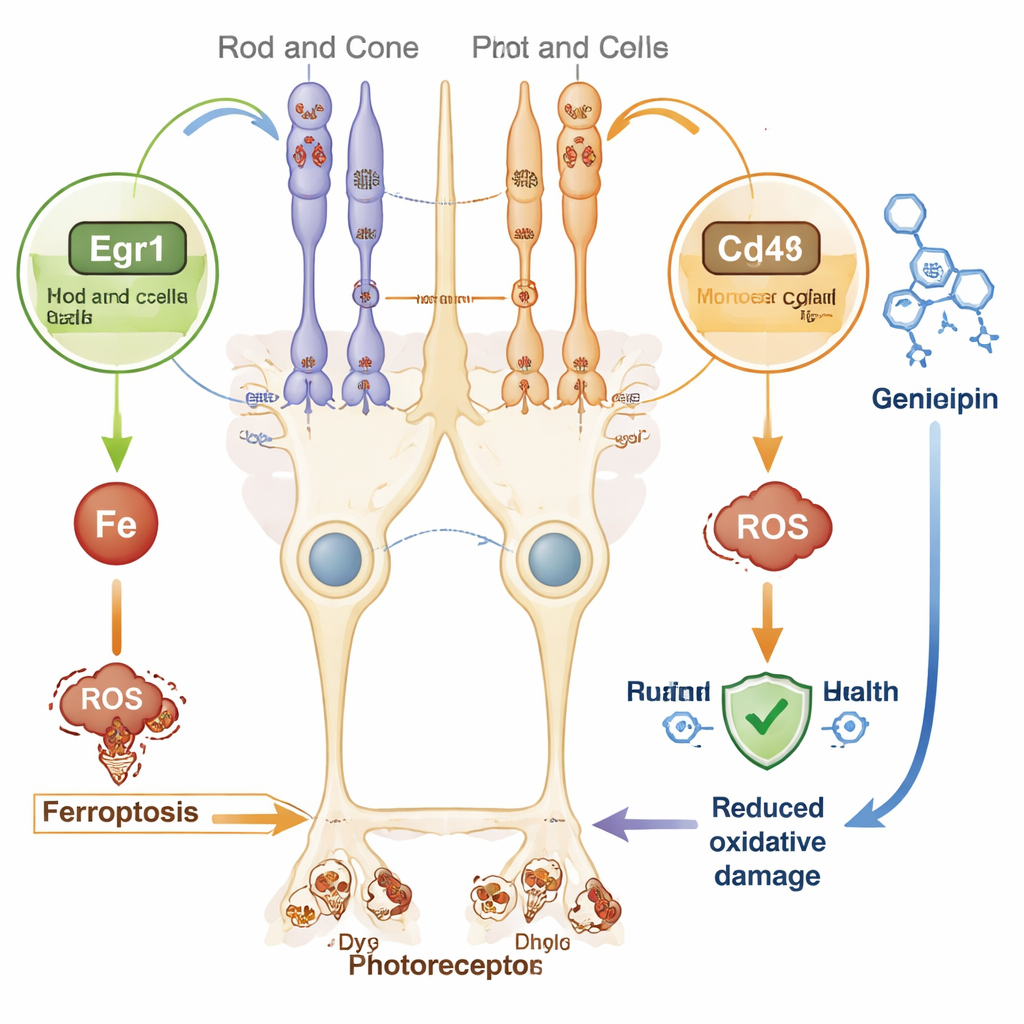
由于针对每一种突变定制的基因治疗复杂且费用高昂,广谱策略更具吸引力。新鉴定的基因特征提示了若干此类途径。例如,Egr1是对氧化应激反应的快速开关,在其他器官中可促进铁死亡。Cd44作为穆勒细胞表面的分子,在不同组织中被证明会加剧铁过载和细胞死亡。与此同时,负责脂质代谢和能量利用的Ppara下调,可能使视网膜细胞更易受损。通过针对这些共享的应激通路,或许可以在多种致病基因背景下减缓视网膜退化。
可能有助于保护视力的药物
利用药物——基因相互作用数据库,作者筛查了能够影响Egr1或Cd44的化合物。若干现有分子被检出,包括天然化合物剑叶栀子内酯(Genipin),在帕金森病、神经退行性疾病和糖尿病性视网膜病变模型中显示了通过抑制氧化应激和炎症而具有保护作用的证据。虽然这些候选药物尚未在该视网膜色素变性小鼠模型中进行测试,但它们为未来旨在保护感光细胞免受铁死亡的实验室与动物研究提供了有希望的起点。
面向非专业读者的要点
这项工作表明,由铁驱动的氧化性细胞死亡与经典遗传性失明模型中观察到的基因活动变化密切相关。通过筛选出八个关键基因,尤其在感光细胞中应激响应上升的Egr1和在穆勒细胞中显著升高的Cd44,研究为不依赖修复单一突变的潜在疗法绘制了新路径。如果后续实验证实通过针对这些靶点抑制铁死亡可以维持视网膜细胞存活,那么这可能为一系列面临进行性视力丧失的患者带来广泛受益的治疗方案打开大门。
引用: Qiu, X., Fu, XW., Lei, XL. et al. Identification and validation of a novel ferroptosis-related gene signature associated with inherited retinal degeneration in Rd10 mice. Sci Rep 16, 6992 (2026). https://doi.org/10.1038/s41598-026-38193-4
关键词: 视网膜色素变性, 铁死亡, 感光细胞, 视网膜变性, Egr1 Cd44