Clear Sky Science · zh
生物相容的三维层级花状铁掺杂银纳米结构作为体外和体内药物递送平台
为何微小金属花对癌症治疗重要
化疗药物可以成为对抗癌症的强大武器,但它们常常像地毯式轰炸一样在全身扩散,既损害肿瘤也伤及健康组织。本研究探讨了一种截然不同的方法:构建由银与铁组成的微小花状颗粒,用以携带已被确立的抗癌药物甲氨蝶呤,并在需要之处更精确地释放。通过调控它们的形状、表面化学和对酸性的响应,研究人员旨在使治疗更有效并减少对机体其他部分的伤害。
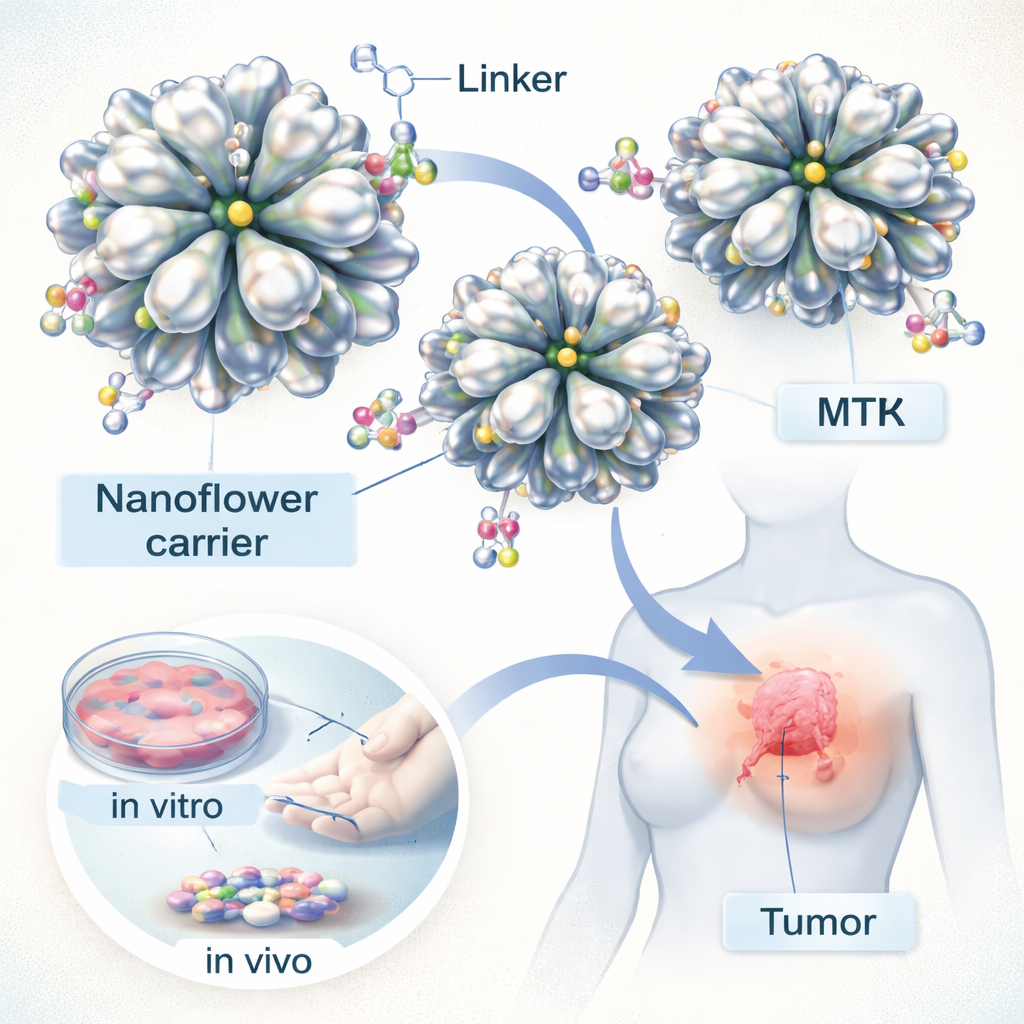
由金属构成的微小花朵
团队设计了由银轻度掺杂铁的三维“纳米花”。在显微镜下,这些颗粒确实像花朵,拥有许多薄而重叠的“花瓣”。这种复杂的形貌赋予它们很大的比表面积,非常适合承载药物分子。研究人员通过一种简单的水相化学反应制备纳米花,调节丙二酸和铁盐等成分,使金属原子生长为分支状、花瓣状的结构而非致密球体。成像与结构学测试证实,这些颗粒具有期望的粗糙分层表面,且铁在银中均匀分布。
将金属花转变为药物载体
为了将这些金属花变成药物运输载体,科学家们首先在其表面包覆了一种小有机分子,充当双头钩子。一端天然地结合银,另一端可与甲氨蝶呤连接。通过常规的偶联化学,他们在药物与纳米花表面之间形成了稳定的键合。这一策略实现了高药物负载——大部分供应的甲氨蝶呤可以附着到载体上。关键在于,药物与载体之间的键对酸性敏感:在肿瘤和癌细胞内常见的弱酸性环境下,该键更容易断开,而在健康血液的近中性pH下则更为稳定。
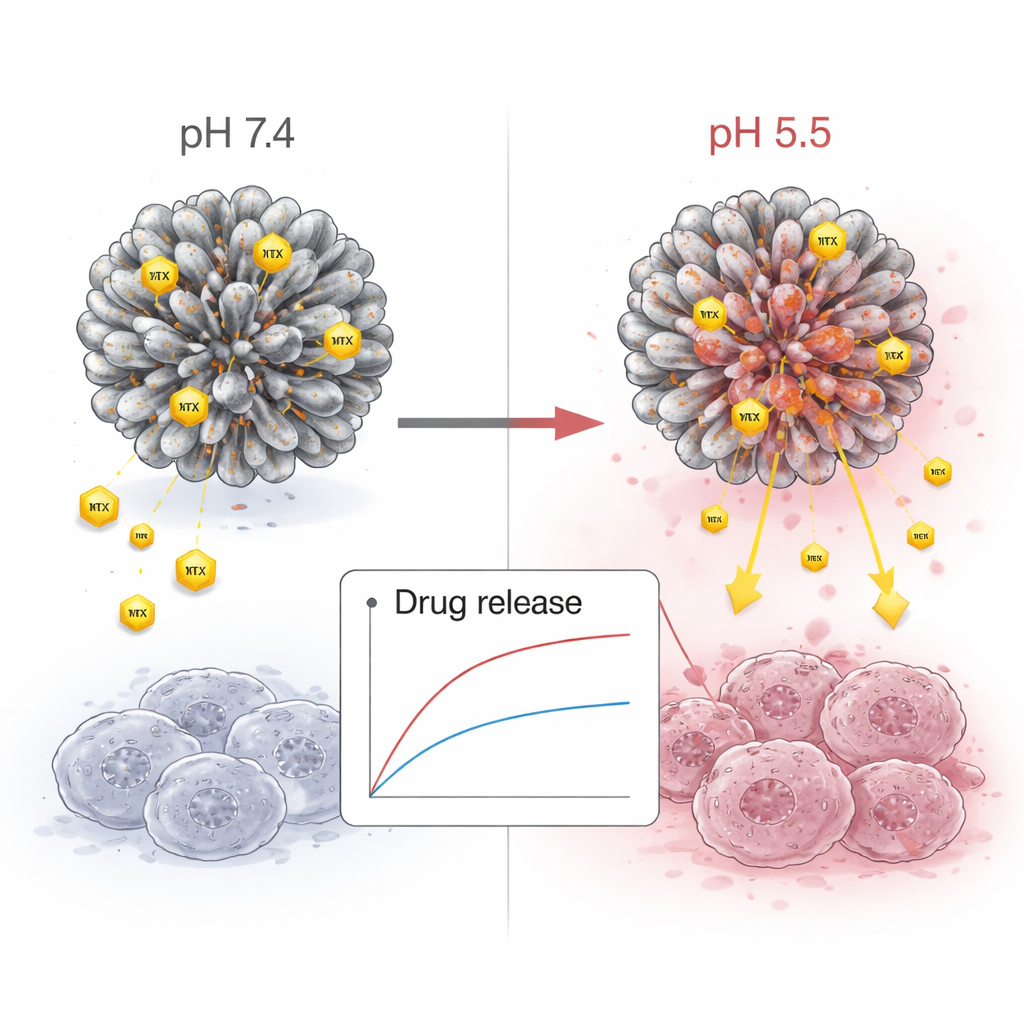
在酸性肿瘤环境中的智能释放
团队随后测试了在不同酸度下随时间释放的药物量。在正常血液pH下,纳米花缓慢释放甲氨蝶呤,这有助于限制对健康组织的损害。在类似乳腺癌细胞内的更酸性条件下,释放显著加快,在几天内释放出更多药物。这意味着同一颗粒在循环中可以保持“静默”,但一旦进入肿瘤更严苛的化学环境就变得“活跃”。这种对pH敏感的行为是现代“智能”药物递送系统的关键目标之一。
对细胞、血液与肿瘤的影响
在培养皿中测试时,负载甲氨蝶呤的纳米花对正常成纤维细胞表现温和,而对乳腺癌细胞则更具毒性,提示具有一定选择性。接触纳米花的癌细胞显示出程序性细胞死亡的迹象,并主要在复制DNA的生长周期阶段被阻滞,这与甲氨蝶呤已知的作用模式相符。荧光成像显示这些颗粒可以进入细胞并接近其遗传物质。纳米花在血液测试中也表现良好:在大多数浓度下对红细胞造成的损伤很小,而负载药物的版本尤其安全。在小鼠乳腺癌模型中,X射线微CT扫描和组织学研究显示这些颗粒倾向于在肿瘤中积聚,并在两周内帮助缩小肿瘤体积,同时在其他器官中的蓄积有限。
这对未来治疗可能意味着什么
总体而言,该研究表明这些铁掺杂银纳米花可以作为一种有前景的平台,更精确且更温和地递送甲氨蝶呤。通过结合高药物负载、酸触发释放以及在血液和组织中的合理安全性,它们解决了化疗长期存在的若干问题:选择性不足、严重副作用和药物快速洗脱。尽管仍需更多工作来充分了解它们在体内的长期行为并将其适配用于人体,但这些微小的金属花展示了一个可能的未来:将抗癌药物直接运送到肿瘤并以更可控、更有针对性的方式释放,从而可能使已有药物更安全、更有效。
引用: Almosawy, W., Landarani-Isfahani, A., Moghadam, M. et al. Biocompatible 3D hierarchical flower-like iron-doped silver nanostructures as a platform for in vitro and in vivo drug delivery. Sci Rep 16, 7044 (2026). https://doi.org/10.1038/s41598-026-38175-6
关键词: 纳米医学, 药物递送, 甲氨蝶呤, 乳腺癌, 银纳米颗粒