Clear Sky Science · zh
奥比妥珠单抗通过鞘磷脂依赖性抑制TRPML2引发溶酶体不稳定
为何这个抗体故事重要
对许多患有B细胞淋巴瘤的人来说,现代抗体药物已将曾经几乎必死的诊断转变为可治疗的疾病。然而,并非所有抗体都一样:有些抗体比其他抗体更强且更可靠地杀死癌细胞。本文通过聚焦细胞内一个出人意料的“内鬼”——细胞自身的回收中心溶酶体,以及其膜上脂质与离子通道的微妙平衡,来解释为何一种药物奥比妥珠单抗在直接杀伤淋巴瘤细胞方面优于其前任利妥昔单抗。
从表面靶点到内部自毁
利妥昔单抗和奥比妥珠单抗都识别B细胞表面的同一靶点——名为CD20的蛋白。但作者表明,奥比妥珠单抗被细胞摄取得更快、更有效。一旦与癌细胞表面的CD20结合,抗体–受体复合体通过胞吞过程被内吞并转运到酸性隔室,包括溶酶体。在那里,奥比妥珠单抗触发溶酶体膜通透性改变:本来坚固的溶酶体膜变得泄漏,消化酶如蛋白酶体(cathepsins)溢出到细胞内,引发细胞死亡通路。研究发现,这些隔室中盐和水分平衡的变化导致溶酶体肿胀,会大幅放大这种致命效应。
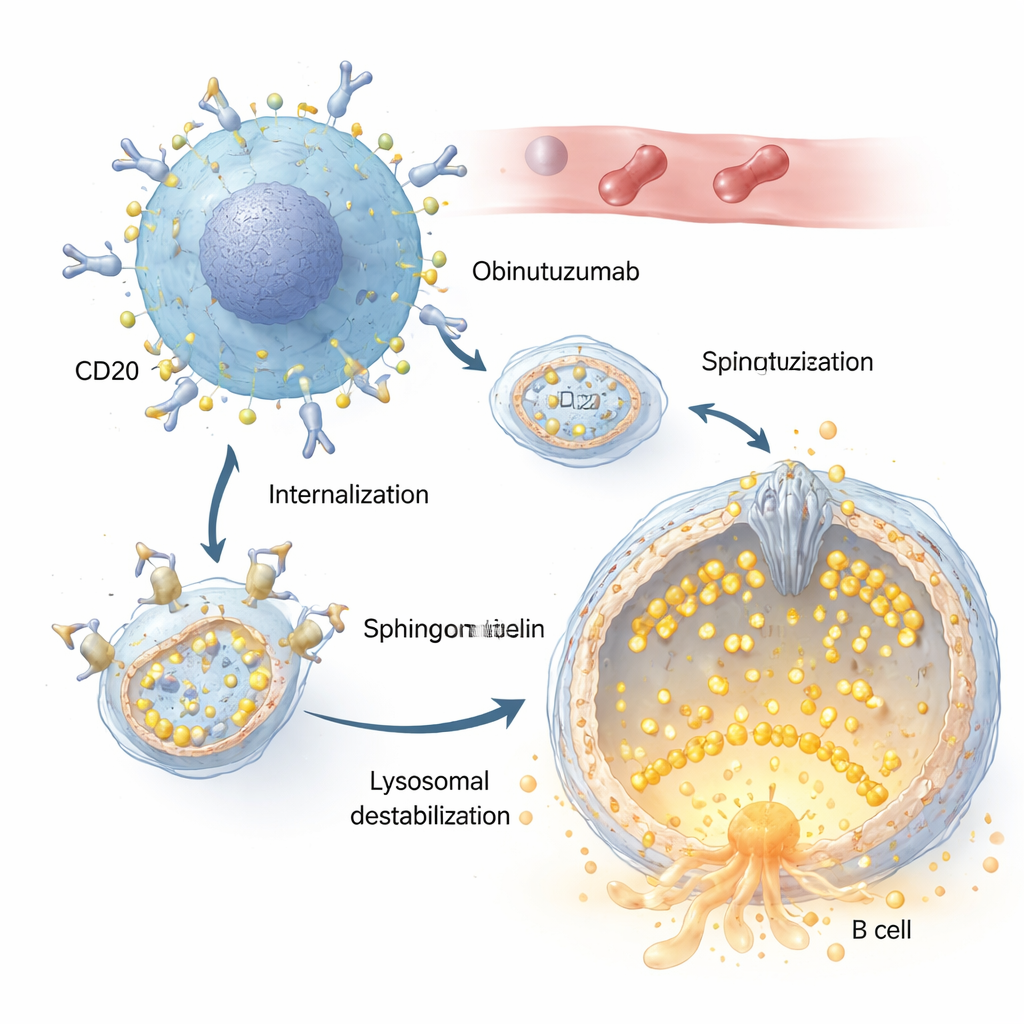
微小门控通道的作用
故事的核心是TRPML2,这是嵌入溶酶体膜的钙通道。在正常情况下,TRPML2通过释放钙帮助溶酶体应对机械和渗透应力,支持膜修复、运输和体积调控。研究者使用荧光钙染料和工程化的TRPML2钙感受器,显示奥比妥珠单抗迅速关闭该通道:在处理几分钟内,原本能打开TRPML通道的药物不再引发钙爆发。降低TRPML2表达的基因学方法,或阻断TRPML活性的的小分子抑制剂,都会使淋巴瘤细胞对奥比妥珠单抗更脆弱,导致更多溶酶体泄漏和更高的直接细胞死亡率。
膜脂如何改变天平
研究接着探究抗体摄取与通道关闭之间的联系。注意力转向鞘磷脂,这是一种在细胞膜中丰富且已知会干扰TRPML通道的脂质。使用荧光鞘磷脂结合探针,作者发现含有奥比妥珠单抗的囊泡一旦进入酸性隔室就富含鞘磷脂,远高于含利妥昔单抗的囊泡。当用能切除鞘磷脂的酶—鞘磷脂酶处理细胞时,即便存在奥比妥珠单抗,TRPML2的释放钙活性也得以恢复。在这些情况下,溶酶体不易泄漏,死亡细胞更少,强烈表明累积的鞘磷脂使TRPML2失能并使溶酶体易于破裂。
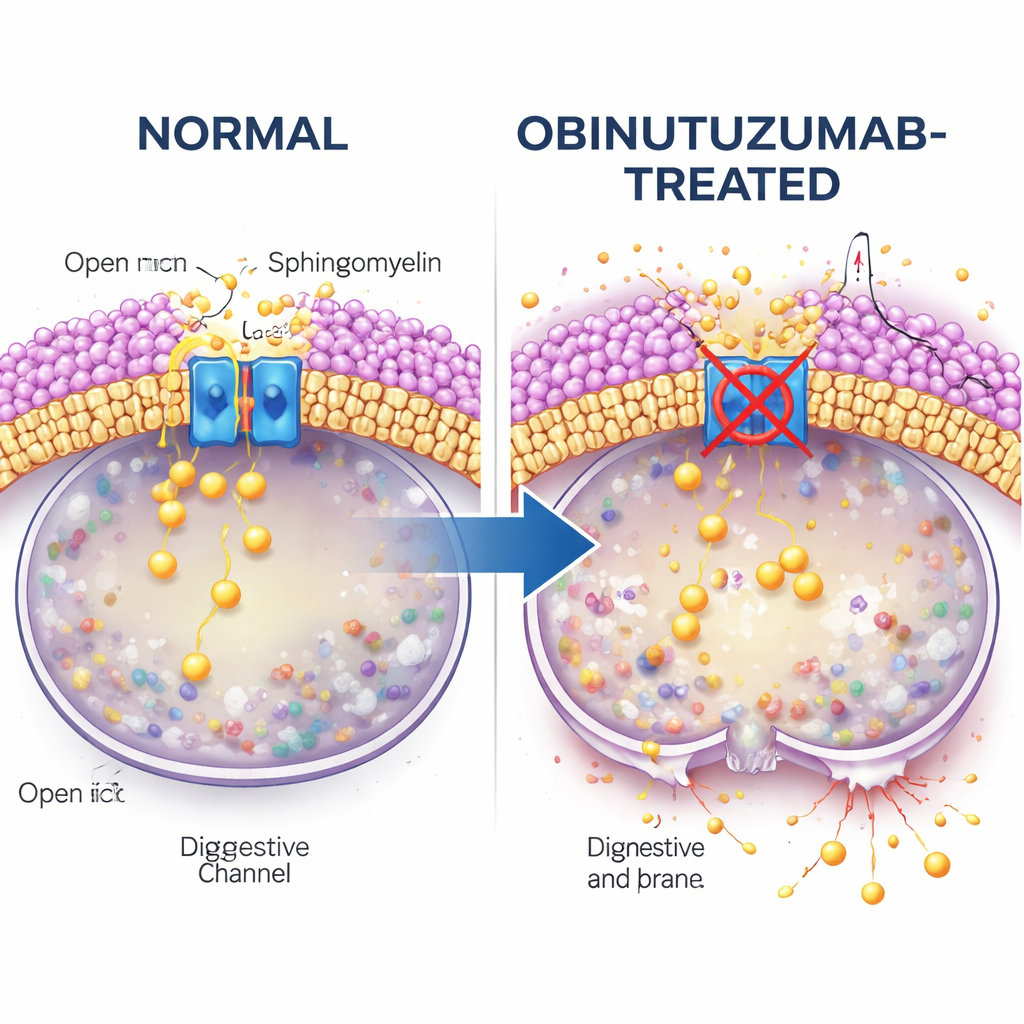
转运路线与胆固醇检查点
奥比妥珠单抗进入细胞的途径也很关键。电子显微镜和pH敏感的抗体标记显示,奥比妥珠单抗比利妥昔单抗更快地离开细胞表面并进入细胞内囊泡。当研究者干预特定的摄取途径时发现,阻断一种依赖胆固醇的胞吞形式(用一种叫filipin的化合物)能阻止奥比妥珠单抗关闭TRPML2,并部分减少溶酶体损伤与细胞死亡。其他胞吞抑制剂并没有这种保护效果。这指向一种富含胆固醇和鞘磷脂的专门通路,该通路将奥比妥珠单抗运送到溶酶体,从而促成TRPML2抑制和随后的膜不稳定。
这对未来癌症治疗意味着什么
简而言之,这项工作表明奥比妥珠单抗之所以能如此高效地杀死B细胞淋巴瘤,是因为它将肿瘤细胞的溶酶体推入一种脆弱状态。通过将抗体–CD20复合体驱动进入富含鞘磷脂的隔室,药物间接关闭了保护性钙通道TRPML2。一旦这种防护消失,溶酶体在应力下更容易破裂,释放腐蚀性酶,从内部拆解癌细胞。理解这一脂质—离子通道轴不仅解释了奥比妥珠单抗为何优于利妥昔单抗;还提示了若干策略以增强抗体治疗,例如将其与改变鞘氨醇类脂质的药物或促进TRPML2活性的药物联合,以精细调控肿瘤细胞溶酶体的自毁时机和程度。
引用: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
关键词: 奥比妥珠单抗, B细胞淋巴瘤, 溶酶体, 鞘磷脂, TRPML2