Clear Sky Science · zh
基于微小RNA谱的骨骼肌肌管来源细胞外囊泡功能特性:与间充质干细胞来源细胞外囊泡的比较分析
小包裹中的肌肉信息
我们的肌肉不仅仅推动运动——它们不断向全身发送分子“短信”。本研究探讨了肌肉细胞释放的微小颗粒与广泛用于未来疗法的干细胞释放的类似颗粒相比如何。通过解读这些颗粒所携带的遗传信号,作者提出了一个务实的问题:在何种疾病类型中,肌源性颗粒可能优于干细胞来源的颗粒?
穿行全身的微小信使
所有细胞都会释放被称为细胞外囊泡(EVs)的微观泡状体。这些是由脂质包裹的纳米级包裹,载有分子货物。微小RNA是一类关键货物——它们是短小的RNA片段,能帮助上调或下调基因,进而塑造细胞行为。骨骼肌作为驱动运动的组织,实际上是体内最大的分泌器官,尤其在通过非侵入性刺激(如超声)时会释放大量EVs。相比之下,间充质干细胞已是临床试验中的主力,其EVs正在被测试用于组织修复和抑制炎症。
解读货物的遗传代码
研究者并未直接在动物或人体中测试EVs,而是重新分析了现有测序数据集,这些数据记录了小鼠骨骼肌肌管(实验室培养的肌纤维)和骨髓来源间充质干细胞的EVs中存在哪些微小RNA。肌源性EVs有少数占主导地位的微小RNA,例如miR-206-3p和miR-378a-3p,占其货物总量的60%以上;而干细胞EVs则携带更为均衡的混合物,包括广泛作用的let-7家族。由于每种微小RNA可以影响许多靶基因,且多种微小RNA可以会聚到同一路径,团队构建了计算方法来理解整体谱系——而非单一分子——如何重塑细胞程序。
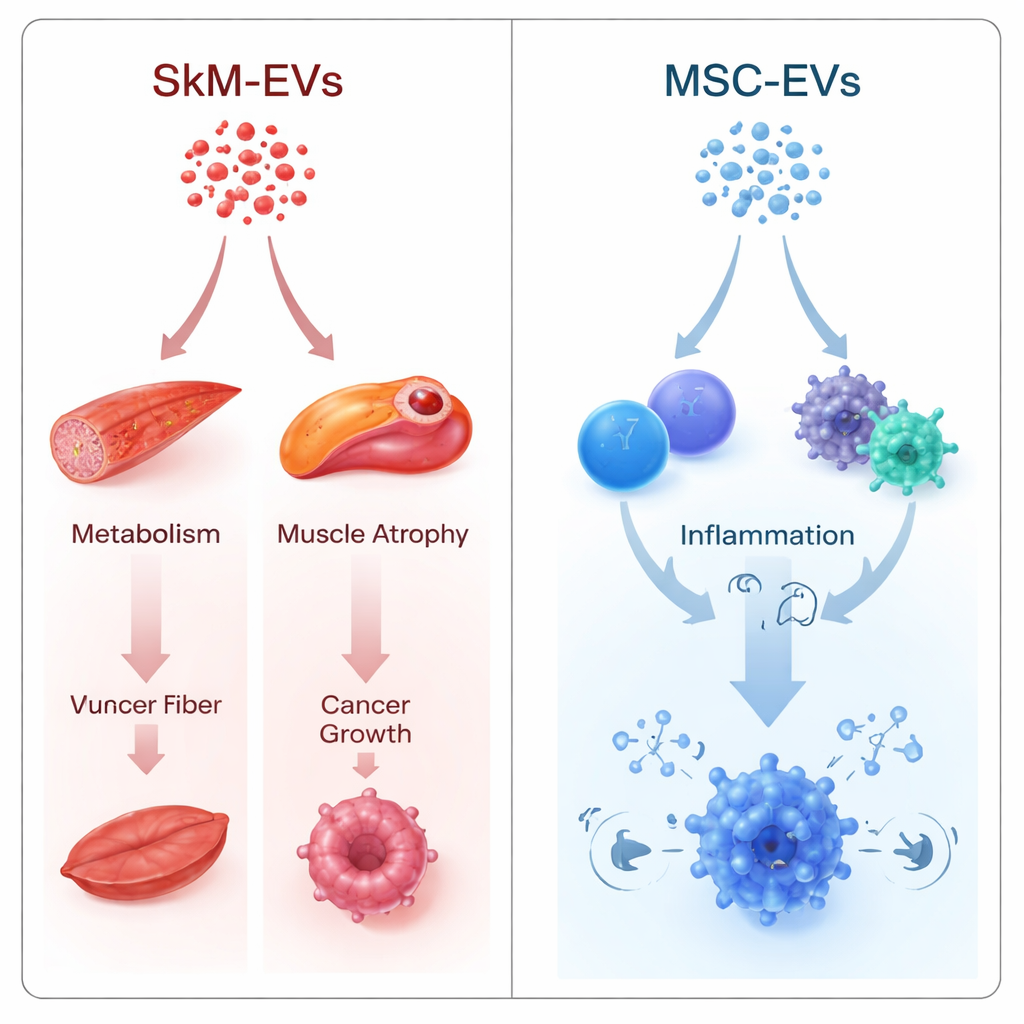
与肌肉、代谢和癌症相关的通路
作者采用了两种互补策略。一种是将肌肉和干细胞EVs进行直接比较,找出它们微小RNA的差异;另一种则分别处理每种EV类型,将其微小RNA谱转换为基因层面的“影响评分”,以估算货物可能多大程度上抑制特定通路。尽管方法不同,两个方法都指向相同的方向。肌源性EVs被预测倾向于抑制与肌肉萎缩(FoxO和TGF-β信号)、血糖控制与能量平衡(FoxO、mTOR、AMPK)以及肿瘤生长通路(ErbB信号和被标注为“癌症相关微小RNA”的一组)相关的通路。许多最具影响力的靶点是肝脏中糖异生的核心调控因子、驱动肌肉萎缩的关键分子和促进癌症的核心基因。
干细胞囊泡与免疫系统
干细胞EVs呈现出不同的图景。其微小RNA货物被预测更强烈地作用于免疫相关通路:NF-κB信号、细胞因子–受体相互作用、B细胞和T细胞受体信号以及Th17细胞分化等。这些通路是机体感知感染、开启与关闭炎症以及塑造免疫细胞身份的核心。这种偏向与越来越多的实验证据一致——表明干细胞EVs可以广泛调节免疫反应,并正在针对需要抑制炎症的疾病(如自身免疫和炎症性疾病)进行测试。
从计算预测到未来治疗
总体而言,这项工作提示肌源性EVs可能天然适合用于涉及肌肉消耗、代谢紊乱或不受控制的细胞生长的病症,而干细胞EVs可能更适合免疫失调驱动的疾病。结果完全来自对现有数据的计算分析,尚不能证明对患者有益,也未考虑EVs的其他货物如蛋白质或脂质。不过,通过将复杂的微小RNA谱转换为通路层面的“指纹”,该研究为将EV来源与疾病类型相匹配提供了路线图,并有助于优先确定哪些组合最值得在实验室乃至临床中进一步测试。
引用: Kawamoto, Y., Yamaguchi, A., Ma, X. et al. Functional properties of skeletal myotube-derived extracellular vesicles based on microRNA profiles: a comparative analysis with mesenchymal stem cell-derived extracellular vesicles. Sci Rep 16, 7436 (2026). https://doi.org/10.1038/s41598-026-38076-8
关键词: 细胞外囊泡, 骨骼肌, 微小RNA, 间充质干细胞, 细胞信号通路