Clear Sky Science · zh
脐带MSC来源的外泌体通过调节中性粒细胞对Th17/Treg平衡的影响改善干眼病发病机制
为什么干燥、刺痛的眼睛不仅仅是小烦恼
数以百万计的人,尤其是老年女性和长时间使用屏幕的人,饱受眼睛干燥、灼热或异物感之苦。我们常常求助于人工泪液,但这类产品只能短暂缓解,不足以抑制潜在的炎症。此项研究探讨一种来自脐带干细胞、无细胞的新疗法,研究者希望它不仅能缓解症状,还能纠正推动干眼病的免疫失衡。
重新审视驱动干眼的原因
现在认为,干眼病是一种眼表面的慢性免疫性疾病,而不仅仅是“泪液不足”。在干眼患者中,免疫细胞的平衡被打破:促炎的辅助性T细胞17(Th17)增多,而起到维持免疫稳态的调节性T细胞(Treg)减少。这种失衡,加上泪液分泌异常,导致泪膜不稳定并损伤角膜透明表面。常规治疗如人工泪液、激素或免疫抑制性眼药水可以缓解症状,但常伴随副作用,并不能直接重置这种免疫失衡。
来自干细胞的微小“包裹”作为药物
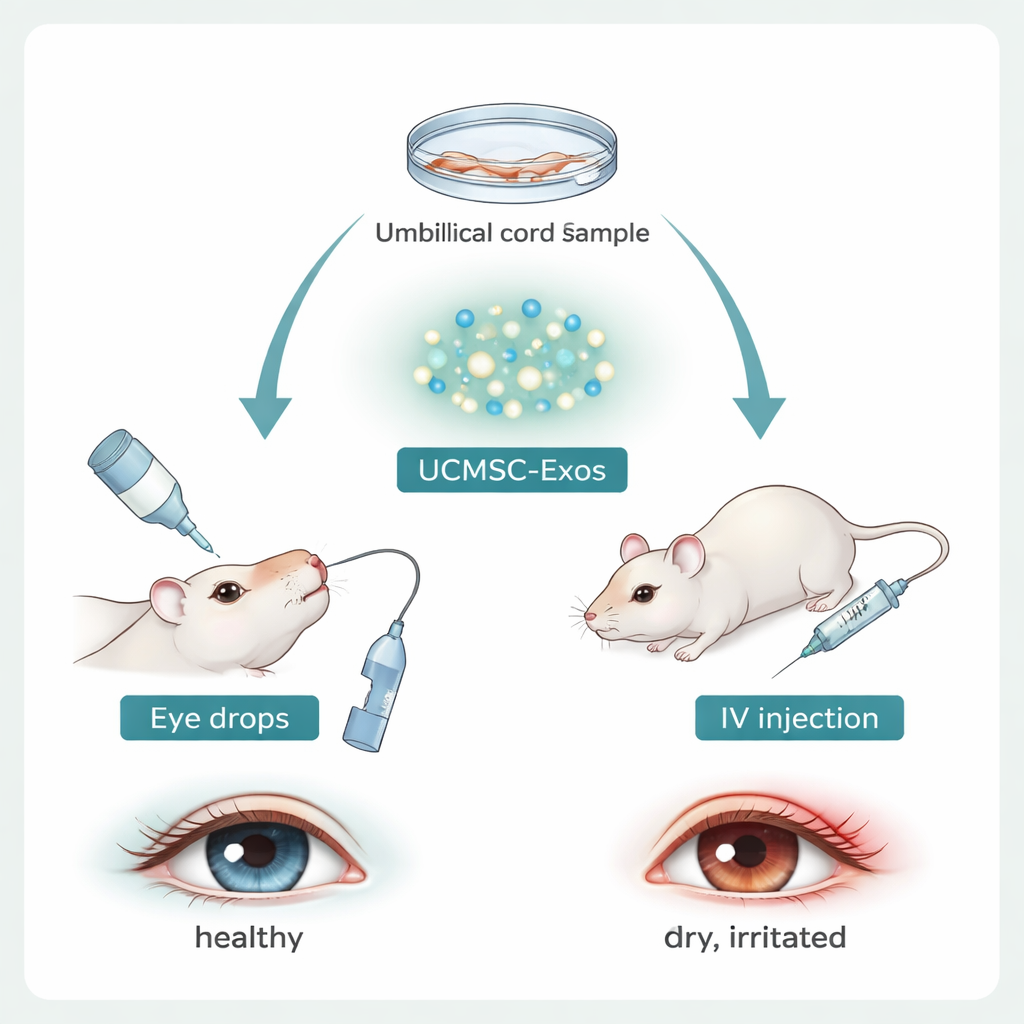
研究者对间充质干细胞感兴趣,是因为它们能抑制炎症,但使用完整细胞存在安全和伦理方面的顾虑。该研究团队转而关注外泌体——脐带间充质干细胞自然释放的纳米级囊泡。外泌体携带来自母细胞的蛋白和遗传物质,并能穿过眼表的一些屏障。科学家在实验室中纯化了这些囊泡,确认了其大小和特征性标志,并在体外测试它们是否能促进角膜细胞“迁移”以封闭伤口。暴露于外泌体的角膜细胞在划痕样缺损模型中更快闭合,提示这些颗粒可直接有助于表面修复。
在干眼小鼠模型中测试疗法
为了评估外泌体在生物体内的效果,研究者使用了将小鼠暴露于干燥环境并用药物抑制泪腺的模型,模拟人类干眼。年轻与年长小鼠均出现典型表现:角膜荧光染色增加,提示表面损伤,泪液分泌减少。与此同时,角膜边缘出现异常聚集的中性粒细胞(先发免疫细胞),邻近的淋巴结中促炎的Th17细胞增多、抑制性的Treg减少。这一模式确认该模型复制了患者所见的免疫紊乱。
外泌体如何平息免疫风暴
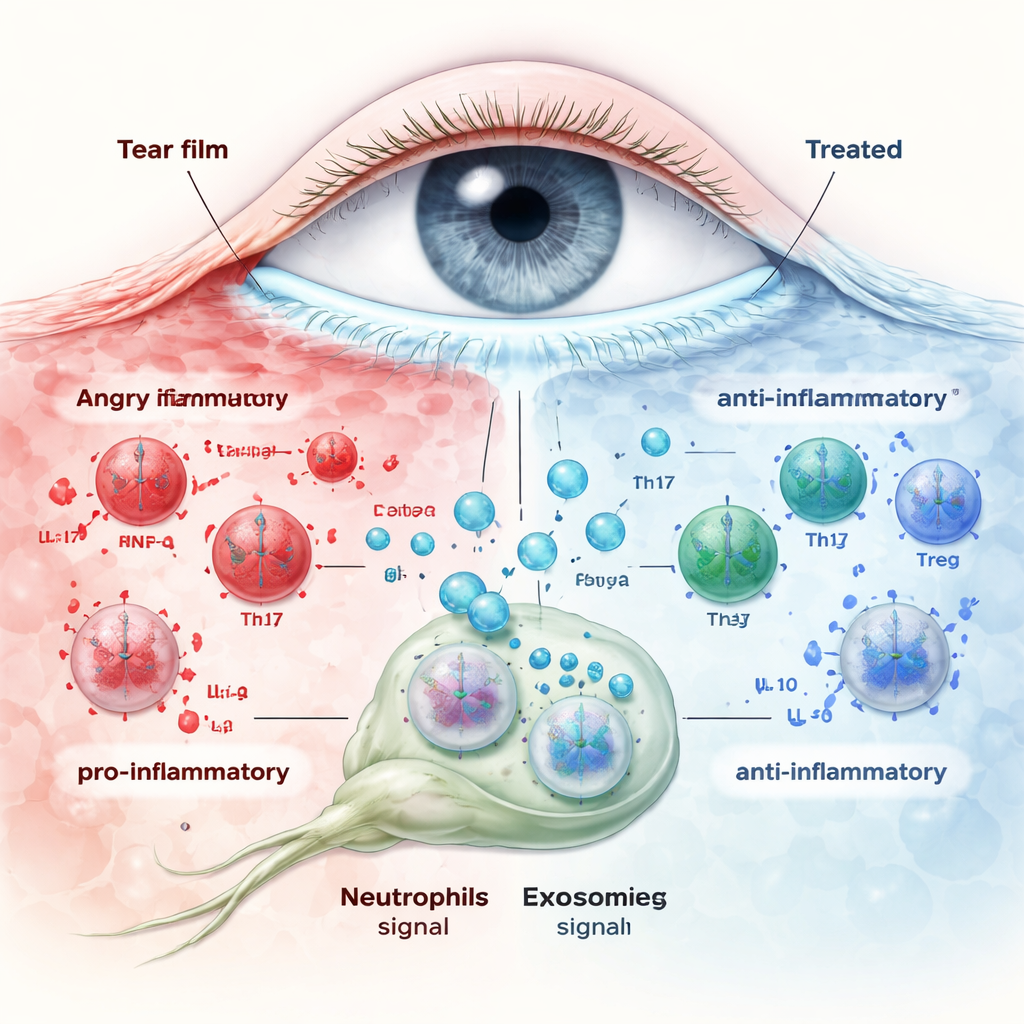
研究团队随后以眼药水或一次静脉注射的方式向干眼小鼠给予脐带外泌体。两种给药途径都改善了角膜健康和泪液分泌,且在年轻动物和静脉注射时效果更明显。角膜的基因表达从报警信号向正常组织修复方向转变。重要的是,外泌体治疗恢复了角膜周围的中性粒细胞数量,并改变了这些细胞的“表述”。在未治疗的干眼中,中性粒细胞释放诸如IL‑1β和IL‑17等促炎因子,同时减少如IL‑10、TGF‑β和Arg‑1等抑炎因子。外泌体逆转了这种模式,增加了抗炎信号、降低了促炎信号——无论是在引流眼部的淋巴结中的中性粒细胞,还是在角膜本身。随着这些信号的变化,淋巴结中的Th17/Treg平衡逐步恢复正常,将先天免疫细胞(中性粒细胞)的行为与适应性T细胞的重置联系起来。
这对未来治疗意味着什么
简言之,这项工作表明来自脐带干细胞的微小颗粒既能帮助受损的眼表愈合,也能教导免疫系统平息炎症。与其单纯补充湿润,这些外泌体似乎促使中性粒细胞释放更多“维稳”分子、减少促炎分子,从而恢复有害与保护性T细胞之间的平衡。疗效在年轻动物和经静脉给药时更强,但局部滴眼也显示出希望。由于外泌体避免了活体干细胞的许多安全问题且可在可控条件下生产,它们有望在未来为干眼患者提供一种更有针对性、持久的治疗,解决不适的根本原因,而非仅仅缓解干燥感。
引用: Gong, Y., Ding, Y., Yang, J. et al. UCMSC-derived exosomes ameliorate dry eye disease pathogenesis by modulating neutrophils on Th17/Treg balance. Sci Rep 16, 7350 (2026). https://doi.org/10.1038/s41598-026-38010-y
关键词: 干眼病, 眼部炎症, 外泌体疗法, 间充质干细胞, 免疫平衡