Clear Sky Science · zh
早期慢性应激改变了斑马鱼肠道的微生物和转录谱
为什么小鱼的早期应激与我们相关
生命头几周的应激经历可能在健康上留下持续数十年的痕迹,但这些影响在体内如何发生仍在探索中。在这项研究中,研究者使用斑马鱼——这类小而透明的鱼是研究人类生物学的有力模型——来探讨早期慢性应激对肠道、肠道内微生物及未来生育力的影响。通过跨越数代追踪受应激的鱼群,研究显示早期应激可以在时间上产生涟漪效应,重塑肠道生态、基因活性,甚至影响卵子与后代的存活概率。
一个多代的应激实验
为探究这些长期效应,团队从鱼类出壳后一周左右开始,直到一个月大期间,每天两次对幼鱼施加反复的轻度挑战。应激源模仿不可预测的环境:短暂的频闪灯、水流扰动或用网轻轻追赶,这些刺激在随机时间发生,使鱼无法适应。这个程序不仅应用于一组鱼,而是在四代连续世代中实施,形成有或没有家族早期应激史的谱系。在成年后,科学家测量这些鱼产生的卵数与后代存活数,并采集肠道样本以同时检查微生物群落和数千个基因的表达活动。 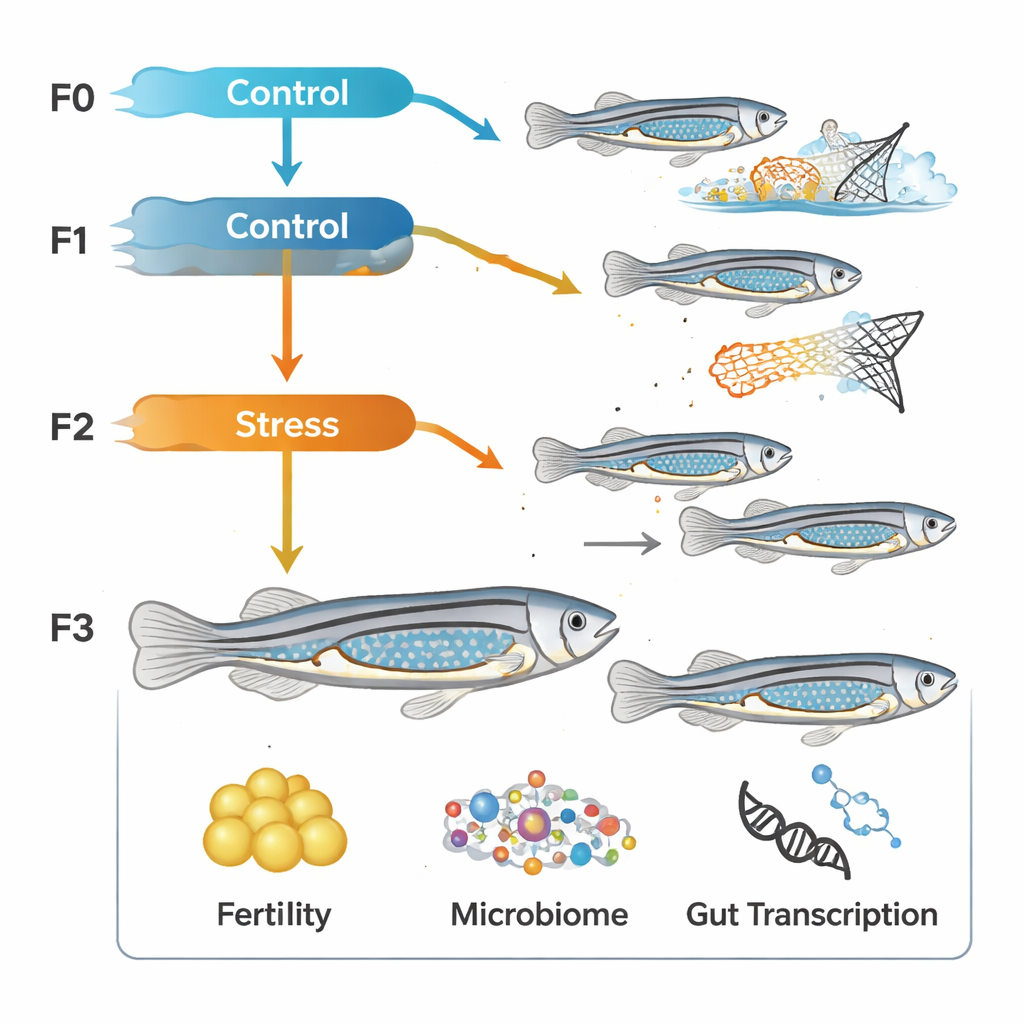
较少的健康卵与更低的存活率
第一个显著结果出现在生殖方面。早期经历应激的成年鱼比未受应激的同胞产出明显更多的死亡或异常卵。即便研究者从外观健康的胚胎开始,来自受应激谱系的后代在胚胎到幼体的转变期间存活较少,许多个体未能活到成年。到存活的鱼达到16个月时,受应激组的总体存活率约为对照组的三分之一,且群体性别分布偏向雌性。这些模式表明,早期应激可以悄然削弱生育力和存活率,其影响在应激期结束很久之后才显现。
肠道微生物向机会性物种倾斜
鉴于肠道微生物组已知会影响大脑与生殖健康,研究团队进一步探问应激如何重塑斑马鱼肠道的细菌群落。通过对混合肠内容物进行DNA测序,他们发现无论是在个体一生中经历应激,还是跨代传递应激史的鱼,其微生物群落都与未受应激的对照明显不同。尽管每个肠道内的总体多样性变化不大,物种组合却发生了显著转变。对照组鱼更倾向于携带更多的假单胞菌(Pseudomonas),而受应激及其谱系的鱼则显示弧菌属(Vibrio)、气单胞菌属(Aeromonas)和希瓦氏菌属(Shewanella)的扩增。这些微生物在水中常见,可在鱼体内无害共存,但也被称为“机会性病原体”,在防御受损时会借机为害。受应激谱系中观察到的独特微生物特征表明,早期逆境可以将肠道生态倾向于更易感染的状态,并在一定程度上跨代持续存在。
应激使肠道基因与免疫防御处于预激状态
为了解宿主组织自身如何响应,研究者检查了早期受应激幼鱼肠道中哪些基因被开启或关闭。通过对整体肠道的RNA测序,他们鉴定出800多个表达水平发生变化的基因。许多被应激上调的基因参与免疫防御,尤其是干扰素触发的通路——这类分子警报有助于细胞对抗病毒和其他入侵者。相比之下,与脂肪代谢、T细胞信号传导和神经细胞发育相关的若干基因则被下调。网络分析突出了抗病毒与抗菌基因家族,提示受应激鱼的肠道处于高度防御状态,可能是在对变化的微生物群落作出反应,或直接对压力激素的反应。 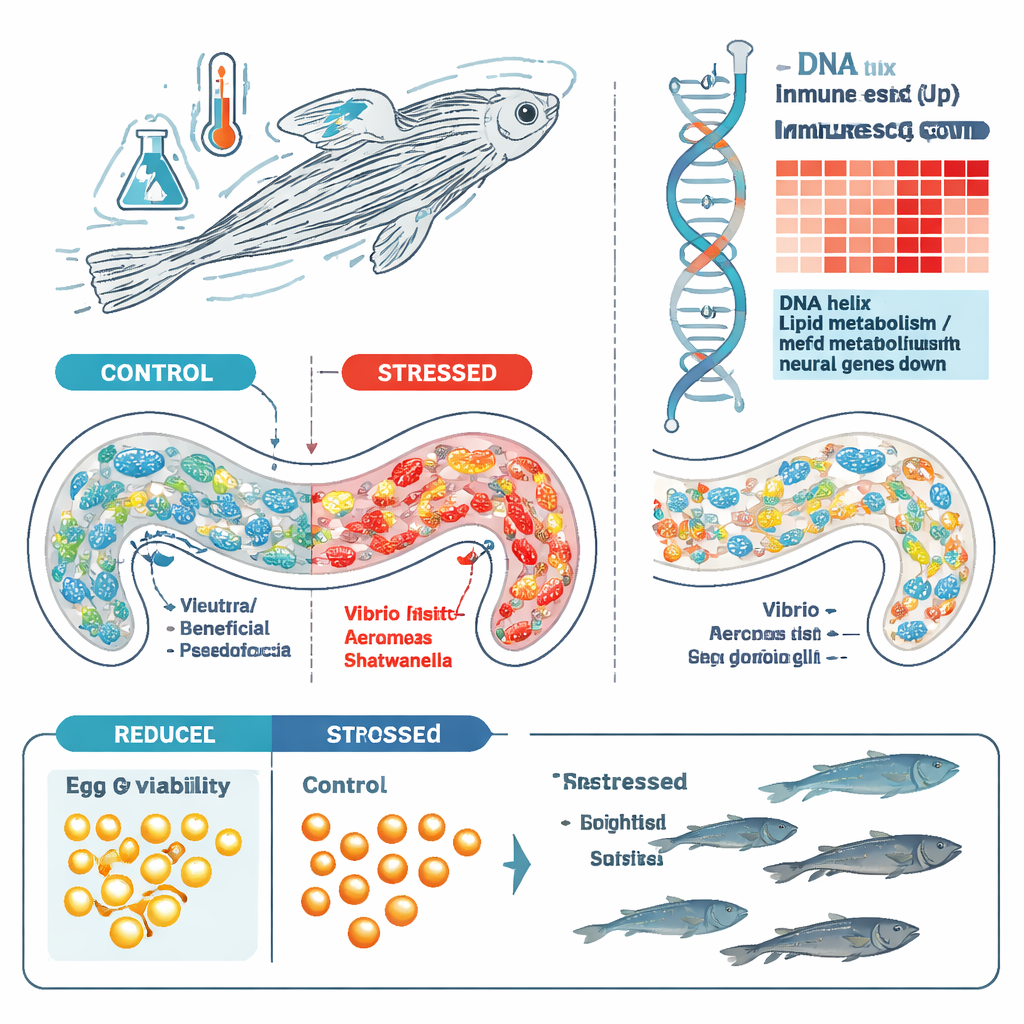
这对健康与未来研究的意义
综合来看,这些发现描绘出早期生活应激作为一种全身性的“程序化”因素,能够降低卵子质量与存活率,同时将肠道微生物推动向更具风险的物种,并将肠道基因表达重新接线为长期警觉状态。尽管这项工作在斑马鱼中完成,但应激激素、免疫防御与肠道微生物的基础生物学在包括人类在内的脊椎动物间是共享的。该研究增强了这样一种观点:肠-脑-性腺轴——连结心理状态、消化、微生物与生殖——是童年逆境影响终生健康的关键通路。它也将斑马鱼定位为一个有力的体系,便于未来开展可超越相关性的实验,精确检验早期应激、微生物与免疫通路如何相互作用以影响生育力、韧性与疾病风险。
引用: Norloff, E., Coker, K., Tusneem, S. et al. Chronic early life stress alters the microbial and transcriptional profile of the zebrafish gut. Sci Rep 16, 6949 (2026). https://doi.org/10.1038/s41598-026-37978-x
关键词: 早期生活应激, 斑马鱼, 肠道微生物组, 生育力, 黏膜免疫