Clear Sky Science · zh
从人类胚胎干细胞生成TCRγδ+ T细胞
为免疫系统配备新武器
癌症治疗越来越多地利用机体自身免疫系统来追踪并消灭肿瘤。其中一种特别有前景的免疫细胞称为γδ T细胞,它们能在无需识别患者具体组织类型的情况下杀死癌细胞——这使其成为“现成可用”治疗的有力候选者。但在成人血液中此类细胞稀少,且要大规模扩增它们十分困难。这项研究描述了一种从人类胚胎干细胞出发在体外培养γδ T细胞的方法,可能为更易获得的癌症免疫疗法打开大门。
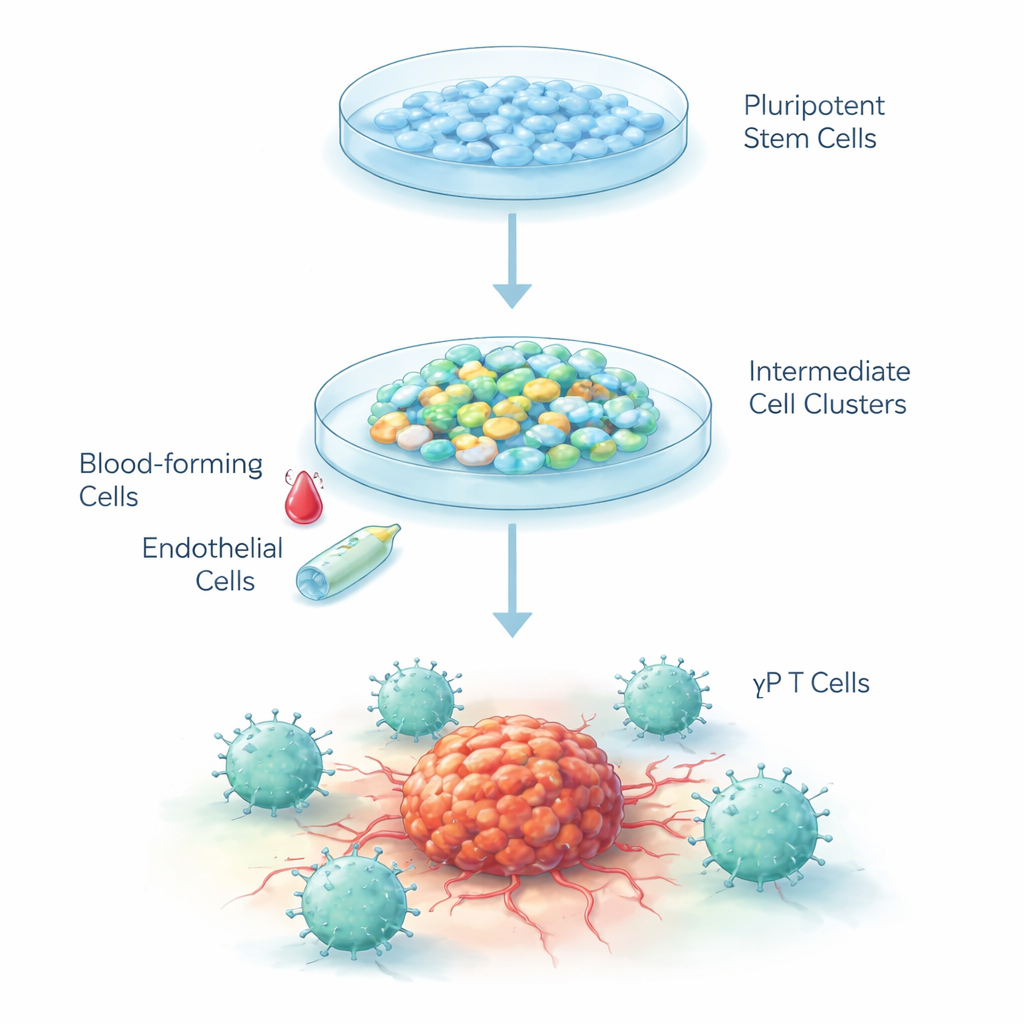
将“空白”细胞塑造成抗癌战士
人类胚胎干细胞是“空白”细胞,理论上可以分化成机体几乎任何组织。研究人员设计了一套逐步配方,诱导这些细胞沿着胚胎中血液和免疫系统最初形成时所走的相同路径发育。他们采用了三阶段过程:首先引导干细胞朝向早期类似血管的细胞,然后转向未成熟的造血细胞,最后分化为γδ 型T细胞。细胞以三维簇状在特殊液体培养基中生长,并在低氧条件下培养以模拟胚胎发育环境,随后在成熟过程中恢复到常氧水平。
构建免疫细胞流水线
在第一阶段,化学信号促使干细胞分化为间胚层——产生血液和血管的早期层。六天内,每个细胞簇中近40%的细胞显示出“造血内皮细胞”的标志,这是一类可产生血细胞的过渡性细胞。在第二阶段,更换生长因子促使这些类内皮细胞发生转换,形成游离的造血祖细胞。超过99%的这些悬浮细胞携带一个关键的早期造血标志,约90%表达另一个血细胞标志,表明这是一个纯度极高、具有继续分化为免疫细胞潜力的细胞群。
到达γδ T细胞阶段
在最后阶段,研究团队提供了已知可促进T细胞发育的信号,包括一种激活Notch的蛋白,模拟胸腺中通常存在的提示。经过25天,超过40%的细胞成熟为γδ T细胞,依据其特征性表面受体和“双阴性”表型(缺乏大多数其他T细胞上常见的CD4和CD8标志)来鉴定。重要的是,产生的常规αβ T细胞很少,这表明该方案强烈偏向γδ谱系。随时间进行的基因分析显示,细胞按有序顺序开启和关闭基因组群,这与体内造血和T细胞形成的过程高度相似。
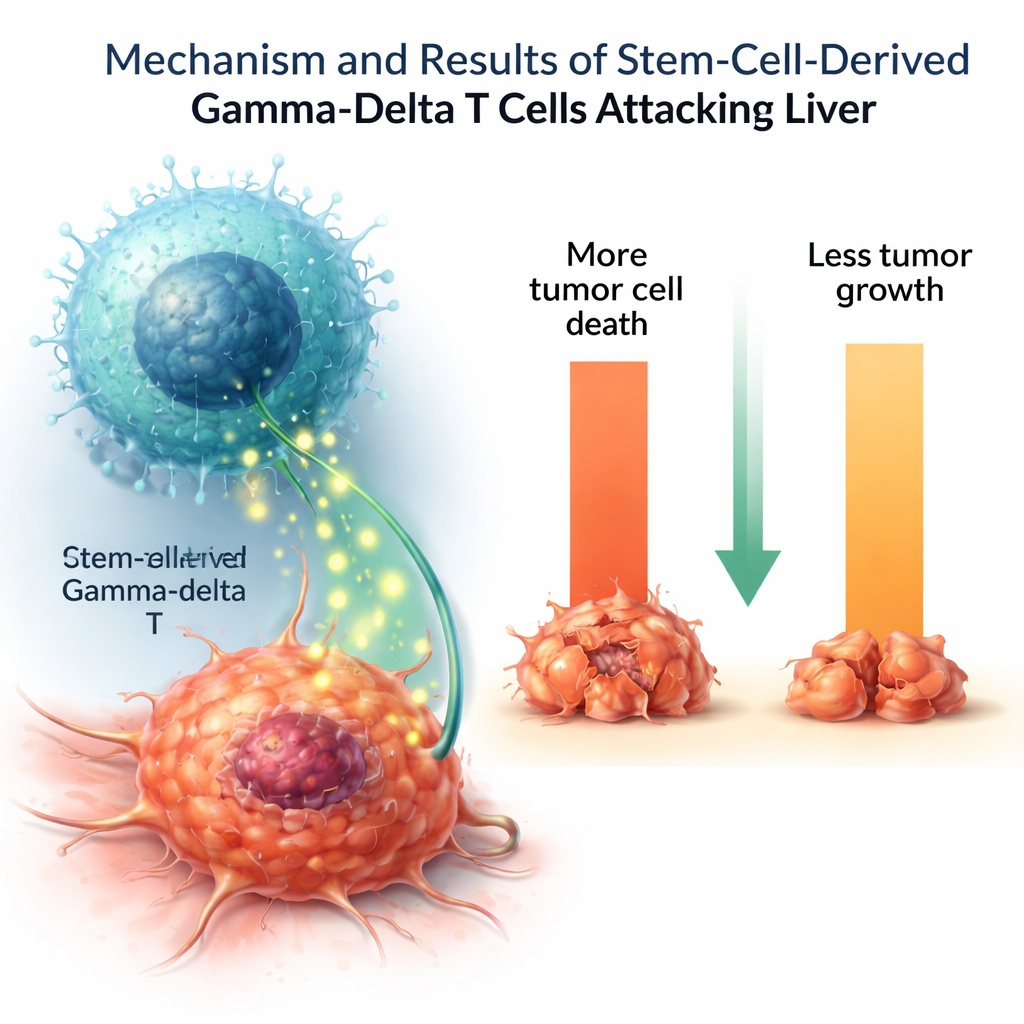
将实验室培养的细胞付诸检验
为检验这些体外生成的细胞是否具备真实的抗癌功能,研究人员将它们暴露于多种人类肿瘤细胞系。γδ T细胞能够杀死相当比例的肝癌细胞并减缓其增殖,而对健康对照细胞影响很小。在刺激下,它们分泌了诸如肿瘤坏死因子和白细胞介素‑2等重要免疫信使分子,这些分子有助于协调并放大免疫反应。一些其他杀伤分子的水平低于天然γδ T细胞,提示实验室培养的细胞可能尚未完全成熟或代表某一特定功能亚型。
这对未来癌症治疗的意义
通过在培养皿中重现简化版的早期造血发育——且未使用动物喂养细胞——科学家在不到一个月的时间内产生了大量γδ T细胞,比以往方法更快也更简便。尽管仍需进一步工作来净化最终细胞混合物、放大生产规模,并将配方调整为临床认可的无血清条件,但这一方法指向了可再生的标准化γδ T细胞来源。如果这些细胞在后续测试中被证明安全且有效,它们可能成为下一代“现成可用”免疫疗法对抗肿瘤(如肝脏肿瘤)的广泛可用构件。
引用: Zhang, X., Chen, C., Fu, Y. et al. Generation of TCRγδ + T cells from human embryonic stem cells. Sci Rep 16, 6762 (2026). https://doi.org/10.1038/s41598-026-37941-w
关键词: γδ T细胞, 癌症免疫疗法, 人类胚胎干细胞, 细胞分化, 肝癌