Clear Sky Science · zh
通过计算识别并机制学表征靶向 PDE6D 抑制素的天然产物结合物
将癌症常用的开关反过来对付它自己
从胰腺癌到结直肠癌和肺肿瘤,许多致命性癌症都依赖于一个被称为 RAS 的分子“开启开关”。当这个开关被卡在开启位置时,细胞会失控生长。几十年来,药物开发者一直难以直接关闭 RAS。本文探讨了一种不同策略:寻找能够悄然阻断 RAS 到达作用位点所需的辅助蛋白的天然化合物,从而在不直接针对 RAS 的情况下减弱其信号。 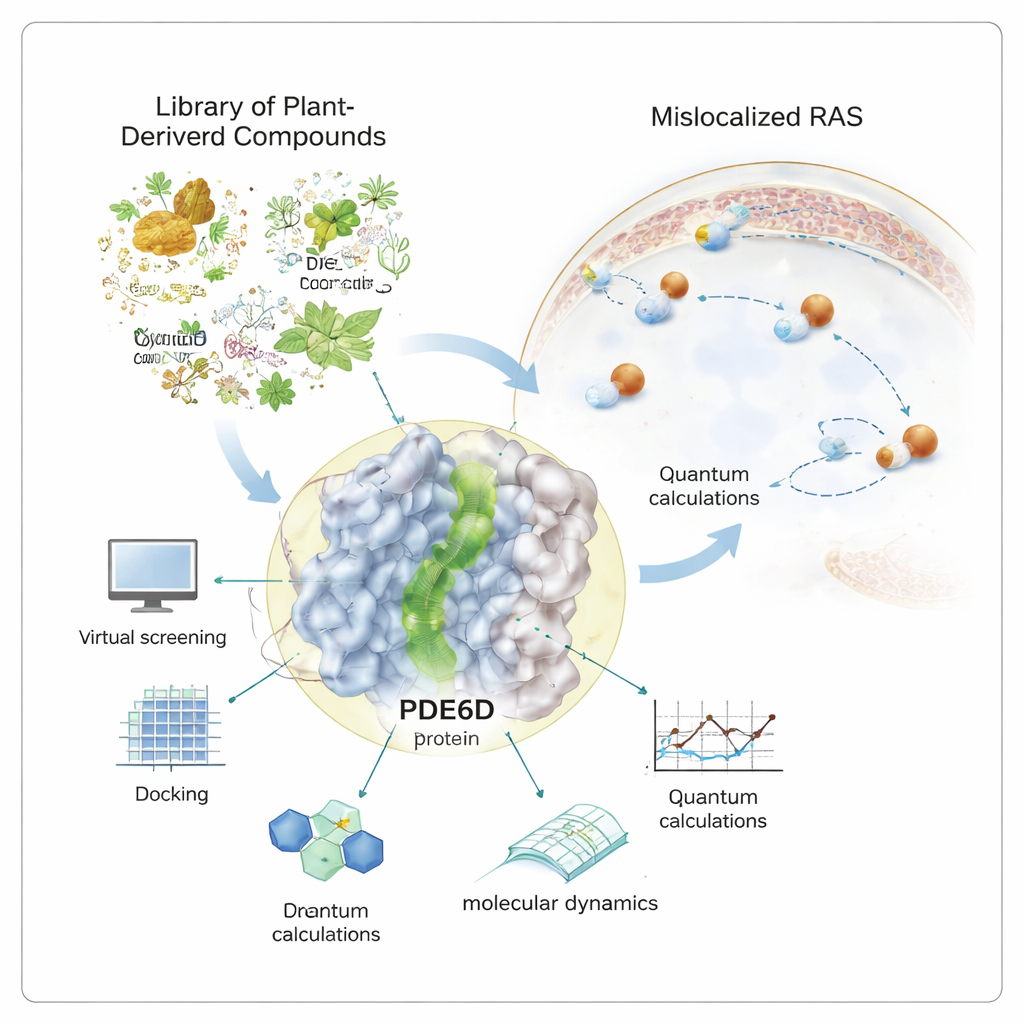
癌细胞中的隐秘帮手
RAS 蛋白必须位于细胞膜内表面才能传递促生长信号。为此,它们携带一段疏油的尾巴,使其能够锚定在膜上。一个名为 PDE6D 的伴护蛋白就像出租车一样,护住这段尾巴,使 RAS 能在细胞水性内环境中运输。PDE6D 有一条狭窄、内衬油质的隧道,可以抓住 RAS 的尾巴。如果这条隧道被堵塞,RAS 更可能到达错误的位置,从而削弱其驱动癌变的能力。因为现有许多针对 RAS 的药物只对一小部分突变有效,研究人员热衷于将 PDE6D 作为一个间接但更具广泛相关性的靶点进行探索。
用计算方法挖掘自然的化学库
作者没有仅依赖合成化学品,而是求助于一个经整理的、包含一千多种可购买天然产物的文库——这些分子最初来源于植物、微生物和其他生物体。利用强大的计算工具将该文库与 PDE6D 的三维结构进行筛选。在这种虚拟测试中,每个分子都被“对接”到隧道中,以评估其结合的契合度和亲和性。得分最高的候选分子随后用量子级别的计算进行更深入的考察,这些计算探测了每个分子中电子的分布,以及它们在蛋白口袋内参与稳定相互作用的能力。
在运动中对应试候选分子做压力测试
蛋白质和小分子在细胞内并非静止,因此研究超越了静态快照。使用长时程分子动力学模拟,追踪原子在半微秒时间尺度上的运动,研究者观察了每个有前景的天然化合物在 PDE6D 隧道内随时间的行为。两种候选分子(标记为 MolPort-039-052-621 和 MolPort-002-507-186)在隧道内保持嵌入并形成稳定的接触网络,而第三种分子则向隧道出口漂移并变得结合较弱。额外的分析描绘出 PDE6D 结构在结合后哪些区域变得更有弹性或更为平静,以及复合体如何探索其“能量景观”——本质上,哪些构象更为舒适且存在时间更长。 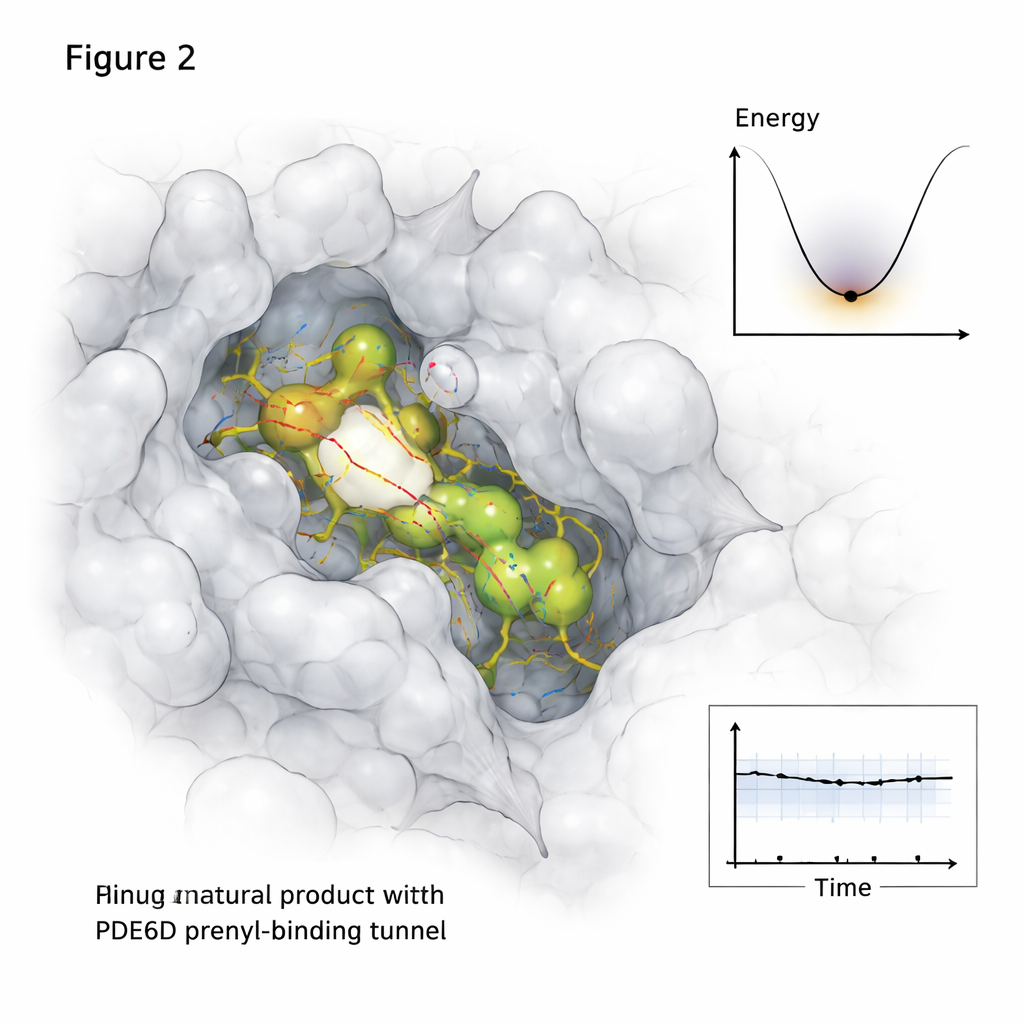
在结合强度与类药性之间的权衡
研究还使用在线预测工具评估这些天然化合物是否具备作为药物起点的现实潜力。所有三种顶级命中都具有与基本“类药性”一致的化学特征,但每种也带有警示。有些被预测具有较差的吸收或溶解性;另一些显示出潜在毒性信号,例如对心律或 DNA 的影响。这些问题意味着这些分子以现有形式不太可能成为现成药物。相反,它们更适合作为结构模板,供化学家改造,在保留适配隧道的关键特征的同时,去除有问题的部分。
对未来癌症治疗的意义
简言之,这项工作并未直接产出新型抗癌药,但它绘制了一条有前景的路线。通过结合多层次的计算方法——从快速对接到详细的模拟与量子计算——研究将庞大的天然分子集合缩小到一小群看起来适合堵塞 PDE6D 隧道的分子。如果未来的实验室研究证实这些化合物确实能在细胞内误导 RAS 并减缓 RAS 驱动肿瘤的生长,它们可能会激发一种新类别的治疗策略,针对癌症的“后勤”系统而非直接作用于其主要驱动因子。
引用: Alshahrani, M.M. Computational identification and mechanistic characterization of natural product binders targeting the PDE6D prenyl binding tunnel. Sci Rep 16, 6571 (2026). https://doi.org/10.1038/s41598-026-37939-4
关键词: RAS 信号传导, PDE6D 抑制剂, 天然产物, 计算药物发现, 癌症治疗