Clear Sky Science · zh
整细胞模型预测古菌 Methanococcus maripaludis 中的可替代蛋白组分配策略
为什么微小的产甲烷者很重要
Methanococcus maripaludis 是一种微小的古菌,能够将二氧化碳和甲酸等简单化学物质转化为甲烷——天然气的主要成分。理解这种微生物如何在细胞内部分配资源,尤其是蛋白质,可以揭示在能量受限条件下生命的一般规律,并为将其作为生物甲烷工厂或绿色化学平台的利用提供指导。
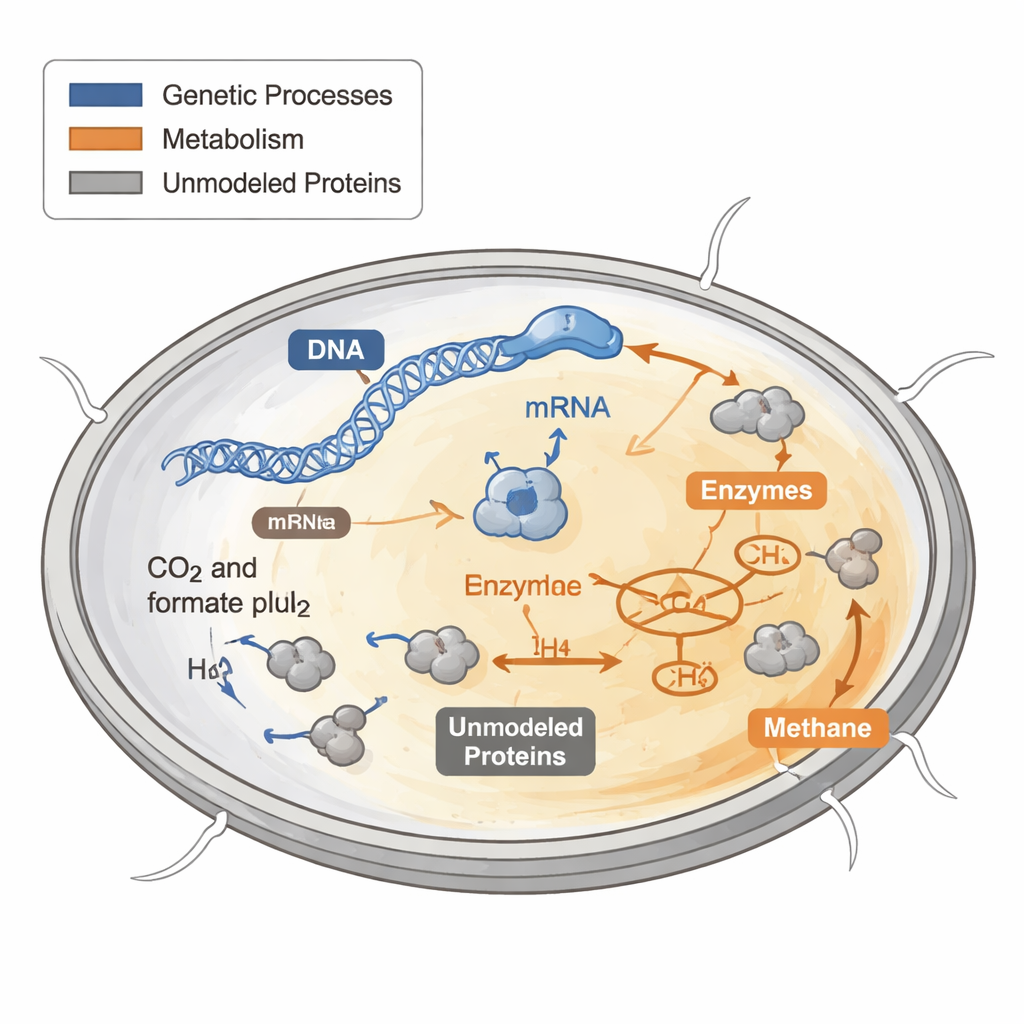
细胞如何花费它们的蛋白质“预算”
每个细胞都必须决定如何使用有限的蛋白质“预算”。有些蛋白质用于构建新的细胞部件,有些用于能量获取,另一些则负责家务性维护。早期的代谢计算模型将这些蛋白视为自由且无限的资源,这在预测恶劣或营养贫乏条件下的生长时表现不佳。在细菌和酵母中,实验证明生长快速的细胞会把更多的蛋白预算投在核糖体上——负责合成新蛋白的分子机器——而生长缓慢的细胞则将资源转向其他用途。
一株打破规则的古菌
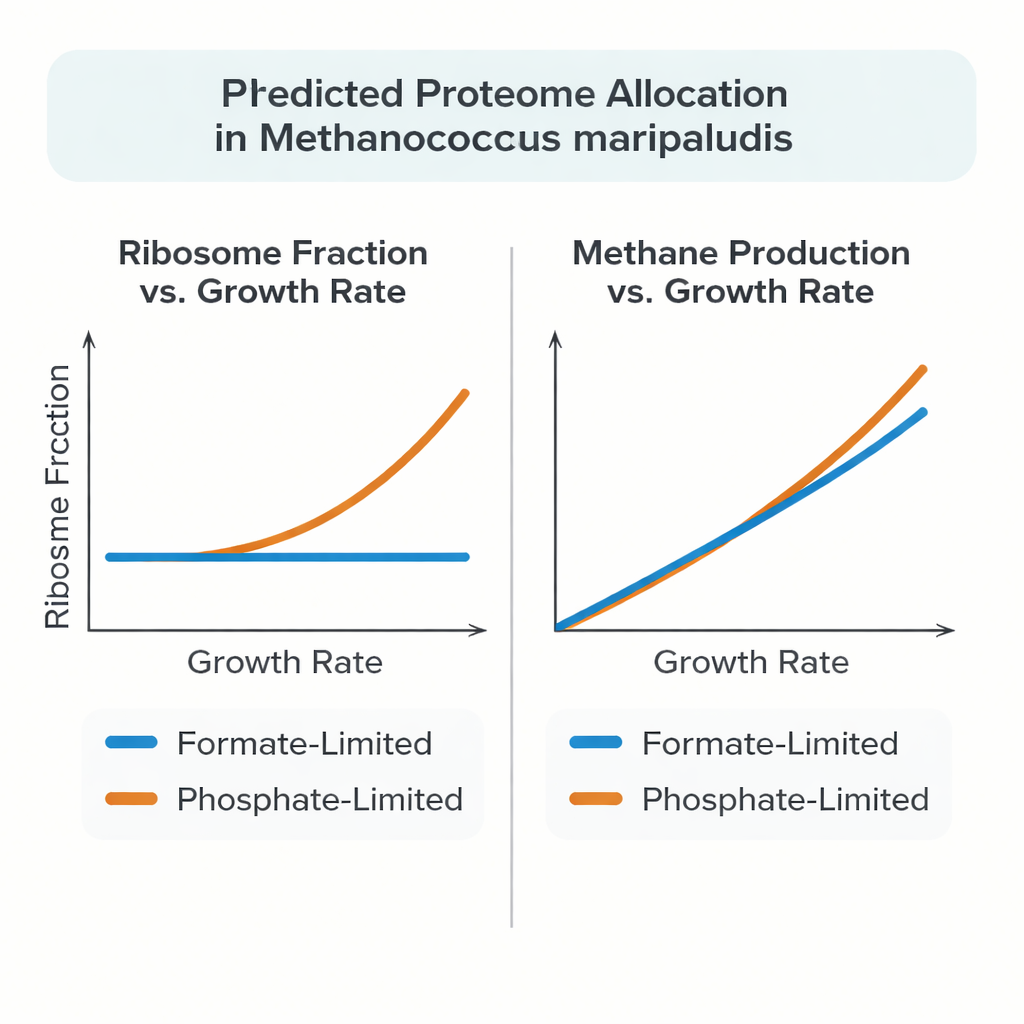
最近的实验证实 M. maripaludis 并不总是遵循这一模式。当它以甲酸同时作为碳源和能量来源生长时,随着生长变慢,其分配给核糖体的蛋白质比例几乎保持不变。然而在磷限制条件下,该古菌的表现更为传统:核糖体比例随着生长速率上升,类似于大肠杆菌和酵母。为了解释这一异常行为,作者构建了一个详细的整细胞风格模型,将代谢与制造及装配蛋白质和 RNA 的高代价过程相连接,而不是把蛋白质当作抽象的反应速率。
构建整细胞风格模型
研究人员以已有的 M. maripaludis 代谢图为出发点,叠加了数千条描述基因表达的反应:将 DNA 复制为 RNA、给转运 RNA 充电、组装核糖体和酶复合体,以及在细胞分裂过程中稀释这些组分。他们从生化数据库和文献中收集酶的速率上限,并估算未建模蛋白质(即未直接对应代谢图中反应的蛋白)在总蛋白质质量中的占比。然后他们施加了全局约束:限制蛋白质和 RNA 的总质量,将反应速率与可用酶量联系起来,并将蛋白质生产与核糖体产能挂钩。在这些约束下,模型必须选择如何把固定的蛋白质预算分配以支持生长。
模拟揭示了什么
在与高质量的恒定培养器实验对比时,模型准确再现了测得的蛋白质和 RNA 质量、甲烷产率以及在一系列缓慢生长速率下的生长产率。在甲酸限制条件下,模拟细胞在生长变化时自然地维持了几乎恒定的核糖体蛋白比例,与实验证据相呼应。在磷限制条件下,模型仅在允许核糖体在低生长速率时工作更快的情况下,才能匹配观察到的核糖体比例上升,这与测量到更多核糖体积极参与蛋白合成的结果一致。模型还提示,在 M. maripaludis 中相当一部分蛋白并非维持最小生长所必需,多余的碳和能量可以根据受限营养的不同被储存或转向其他大分子,例如糖原或游离氨基酸。
探测突变体和生长极限
因为该模型明确考虑了每条代谢途径的蛋白质成本,它不仅能预测基因突变体是否能生长,还能预测它们相对于野生型的生长能力。作者模拟了缺失不同氢处理酶的菌株,并在多种生长条件下(包括有无氢气和一氧化碳)将预测的适应度与实验室测量进行比较。在许多情况下,模型能捕捉突变体能否生长并给出相对生长速率的合理估计,优于早期只能给出是/否答案的模型。相同的框架还被用来估算不同底物组合下批式培养条件的最大可能生长速率。
对科学与技术的意义
通俗地说,这项研究表明 M. maripaludis 在分配其蛋白质劳动力时采用了一种替代策略:在某些条件下,随着生长放缓,它保持蛋白质代工厂占预算的稳定份额,而不是将其缩减进而降低产能。通过将这种行为嵌入到一个详细且以数据为驱动的模型中,这项工作提供了一个试验平台,用于探索能量受限微生物如何在生长、维护和储存之间取得平衡。对于应用研究来说,该模型为工程改造这种古菌以提高甲烷或其他产物的产量提供了路线图,帮助识别在蛋白质投入方面代价最高的酶和通路。更广泛地讲,它将强大的整细胞风格建模扩展到古菌领域,帮助弥合分子细节与涉及气候、能源和工业生物技术的微生物群落大尺度行为之间的鸿沟。
引用: Kasem, G.S., Soliman, T.H.A., Mousa, M.A.A. et al. Whole-cell modeling predicts alternative proteome allocation strategies in the archaeon Methanococcus maripaludis. Sci Rep 16, 7386 (2026). https://doi.org/10.1038/s41598-026-37887-z
关键词: Methanococcus maripaludis, 蛋白组分配, 整细胞建模, 产甲烷作用, 古菌代谢