Clear Sky Science · zh
白细胞介素‑7通过Notch1/TGF-β通路诱导上皮‑间质转化以促进非小细胞肺癌的肿瘤生长与转移
为什么一种信号蛋白在肺癌中很重要
肺癌仍然是全球最致命的癌症之一,主要因为常在肿瘤已转移后才被发现。本研究聚焦于一种天然存在的免疫信使——白细胞介素‑7(IL‑7),提出了一个紧迫的问题:在非小细胞肺癌(NSCLC)中,IL‑7是帮助机体对抗肿瘤,还是在实际上促进肿瘤生长与扩散?通过追踪IL‑7对患者标本、细胞培养和小鼠模型中肺癌细胞的影响,研究人员揭示了一条似乎推动肿瘤朝着更强生长、扩散和治疗抵抗方向发展的通路。
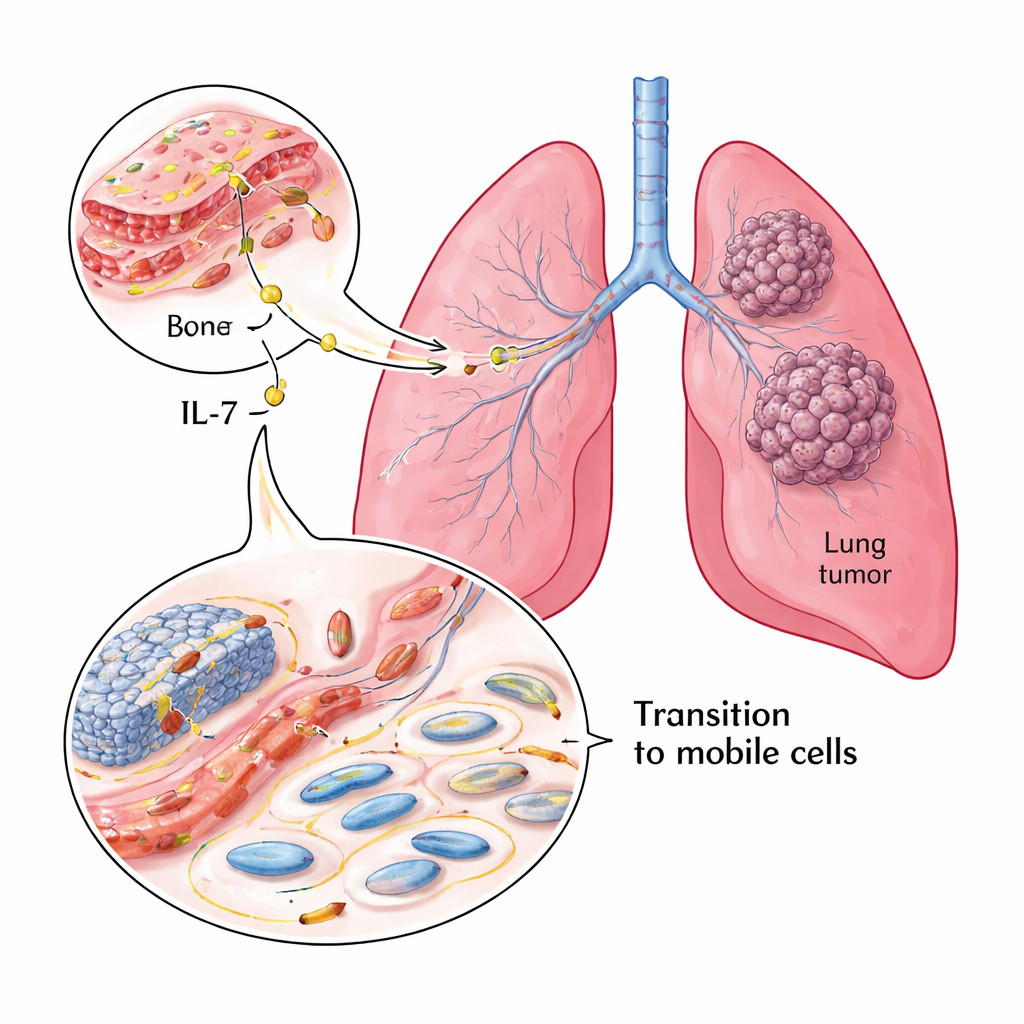
仔细观察肺肿瘤与患者结局
研究团队首先检查了119例NSCLC患者的肿瘤样本。通过对固定组织的染色,他们测定了IL‑7、其受体(IL‑7R)以及两个描述癌细胞“固定”或“移动”状态的关键标志物的水平。E‑cadherin与紧密连接且不易移动的细胞相关,而Vimentin则与更具可塑性、侵袭性的细胞相关。大多数肿瘤显示IL‑7和IL‑7R水平较高。当IL‑7和IL‑7R丰富时,E‑cadherin往往较低而Vimentin升高——这是一种不利的模式。肿瘤保留较多E‑cadherin的患者生存期更长,而IL‑7R高表达的患者则预后更差,使得IL‑7R成为一个强有力的结局预测因子。
癌细胞如何从“停留”转为“脱离”
为了超越相关性,研究人员在体外培养的肺癌细胞上测试了IL‑7的直接作用。当两种NSCLC细胞系暴露于IL‑7时,细胞形态由紧密的鹅卵石状外观转向更为延长、可自由移动的形态。细胞内蛋白水平也相应变化:E‑cadherin下降,而代表“移动性”表型的标志物如N‑cadherin、Vimentin和Snail1上升。细胞的肌动蛋白骨架(帮助细胞爬行)也更为突出并形成突起。阻断IL‑7受体可逆转这些效应,表明IL‑7通过肺癌细胞表面的受体驱动这种被称为上皮‑间质转化(EMT)的形态转变。
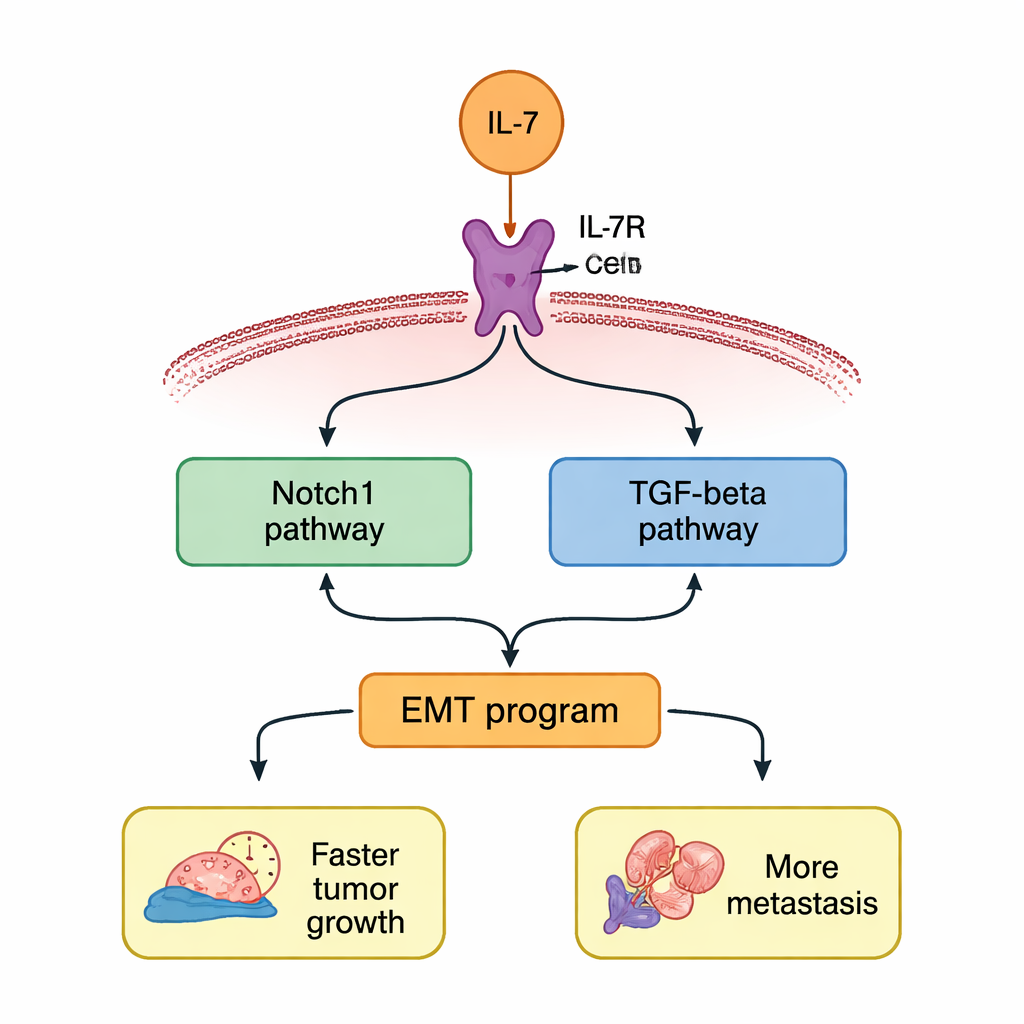
放大危险性的两条相互关联通路
随后研究探讨IL‑7如何在细胞内传递这些指令。作者重点关注两条在侵袭性癌症中常见的信号通路:Notch1和TGF‑β。IL‑7处理后,这两条通路在基因和蛋白水平上均在肺癌细胞中上调。如果阻断IL‑7R,这些上调就会消失。当研究者用特定药物抑制Notch1或TGF‑β时,两条通路同时被抑制,提示存在一种正反馈环路——每条通路都助长对方的维持。切断任一条通路都部分关闭了EMT程序,并减少了IL‑7对细胞增殖、迁移与侵袭的推动作用。
从培养皿到活体肺组织的验证
为检验这些实验室发现是否在活体中成立,团队使用了小鼠模型。在一组实验中,将肺癌细胞皮下移植。接受IL‑7的小鼠相比对照组出现更大、更重的肿瘤。这些动物的肿瘤组织显示E‑cadherin降低,Vimentin和Snail1升高,且Notch1与TGF‑β活性增强。当小鼠同时接受Notch1或TGF‑β的抑制剂时,肿瘤生长和这些侵袭性标志显著降低。在另一个模型中,研究者通过尾静脉注射将癌细胞注入血液循环。IL‑7处理的小鼠最终出现更多肺转移灶且肺脏更重,而阻断通路的药物再次抑制了这种扩散。
这对未来肺癌治疗意味着什么
综合来看,这项工作描绘了IL‑7在NSCLC中并非简单的免疫助力者,而是一把双刃剑。在这一情境下,IL‑7似乎促使肿瘤细胞松开相互连接,采纳更具移动性的身份并迁移到新位点,这一过程通过以Notch1和TGF‑β为核心的相互强化的网络实现。对患者而言,这些发现表明肿瘤中高表达的IL‑7R可能预示更差的预后,且有针对性地设计抑制IL‑7/IL‑7R或其下游通路的治疗策略,可能有助于减缓肿瘤生长与转移。尽管还需更多研究来绘制确切的分子联系并检验人体安全性,但该研究指出了一组有望将局势转向有利于抗癌的新靶点。
引用: Shao, Y., Cheng, H., Ni, W. et al. Interleukin-7 induces EMT to promote tumor growth and metastasis in NSCLC via Notch1/TGF-β pathway. Sci Rep 16, 7326 (2026). https://doi.org/10.1038/s41598-026-37876-2
关键词: 非小细胞肺癌, 白细胞介素‑7, 上皮‑间质转化, Notch1通路, TGF‑β信号