Clear Sky Science · zh
SARS-CoV-2 核衣壳蛋白与可溶性补体调节蛋白形成能结合到病毒颗粒的复合体
这个隐蔽病毒伎俩为何重要
我们大多数人都听说过冠状病毒的“刺突”蛋白,因为它是疫苗的主要靶点。但病毒内部还有另一种蛋白,称为核衣壳蛋白或 N 蛋白,事实证明它远不只是结构性包装。这项研究显示,N 蛋白可以抓住血液中关键的人体免疫调节因子并将它们带到病毒表面。通过这种方式,SARS-CoV-2 可能部分关闭我们最早的防御系统之一——补体系统——帮助病毒存活,并可能促成严重 COVID-19 的出现。
更仔细地看病毒内部的蛋白
N 蛋白是病毒基因组的“包裹者”,有助于包装和稳定其 RNA。临床上在 COVID-19 患者的血液中检测到高水平的 N 蛋白,尤其是重症病例,早期研究也表明它可以引发炎性信号。作者们想知道 N 是否也会干扰补体——这是一网络状的血液蛋白系统,会标记入侵者以便清除并能在微生物膜上打孔。许多病毒已经进化出巧妙的方式借用或模仿体内的补体调节因子以避免被攻击。研究团队提出了三个问题:N 是否能与刺突蛋白及病毒本身结合,是否能与血液中的人类补体调节蛋白结合,以及能否将这些调节蛋白带到病毒表面?
N 与刺突如何在病毒上相遇
研究者使用多种蛋白结合测试,显示 N 蛋白可以直接粘附刺突蛋白,无论刺突是在实验室制备的还是呈现在真实的 SARS-CoV-2 颗粒上。他们在不同实验配置中确认了这一相互作用并测量了其强度,发现亲和力与许多抗体相当。通过将刺突蛋白切分为片段并识别仍能与 N 保持结合的部分,他们将可能的接触区主要映射到刺突的 N 端结构域——该区域已知是抗体结合和某些宿主分子对接的热点。这表明 N 能在实际病毒颗粒上与刺突形成稳固、具有生物学意义的桥接。
劫持体内的安全开关
补体系统受可溶性“刹车”——称为补体调节蛋白——严格控制,这些蛋白保护我们的细胞免受自体攻击。团队关注了四种此类蛋白——C1 抑制因子、C4 结合蛋白、因子 H 和维甲素(vitronectin)——因为它们在补体级联的不同阶段发挥作用。在血清基础测试和纯化蛋白测定中,N 蛋白与这四种调节蛋白均可结合,而在相同条件下刺突蛋白并未与它们结合。这意味着 N 可以在血浆中形成 N–CRP 复合体。关键是,当先将 N 与人血清混合然后暴露于病毒颗粒时,研究者检测到这些调节蛋白附着在病毒上——但仅在存在 N 时才出现。使用的 N 越多,出现在病毒上的补体调节蛋白越多,指向一种剂量依赖的募集机制。 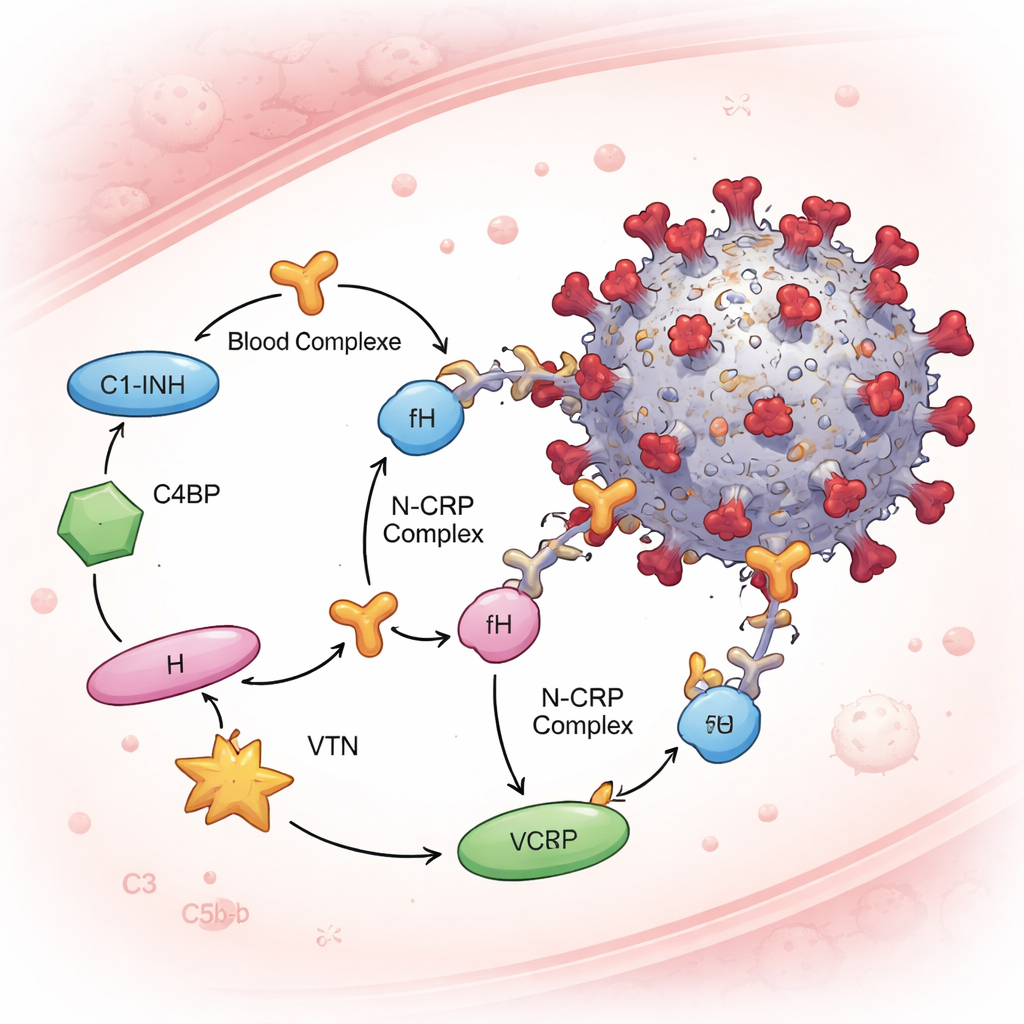
削弱补体的最终攻击步骤
补体系统的终极武器是膜攻击复合体(MAC),它形成环状结构,在细胞或病毒包膜上打孔。作者测试了 N 是否会改变 SARS-CoV-2 上 MAC 的形成。他们将纯化的病毒与有人血清(一部分加入 N,另一部分不加入)共同孵育,然后测量有多少 MAC 的 C5b-9 复合体沉积在病毒上。没有 N 时,病毒积累了 C5b-9,显示补体在起作用;而在存在 N 时,MAC 的沉积按浓度呈下降趋势:N 越多,病毒表面的 C5b-9 越少。这与这样一种观点相符:N 通过在病毒表面装饰补体调节蛋白,使其免于被打穿。 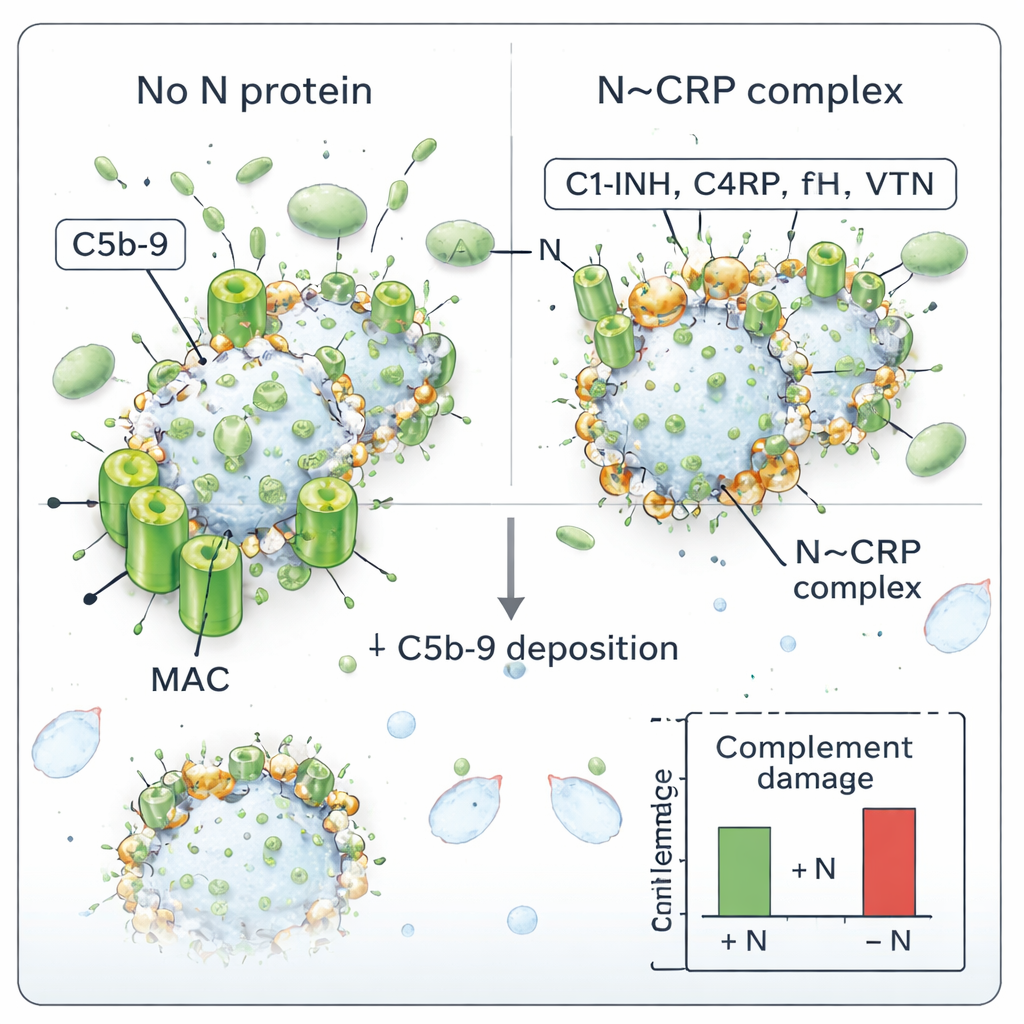
对患者和未来疗法的意义
对非专业读者而言,结论是 SARS-CoV-2 并不只依赖其著名的刺突蛋白来智胜免疫系统。其内部的 N 蛋白可以逸出到血液中,抓住体内的补体“刹车”,并将它们带回病毒表面。在那里,它们可能帮助病毒躲避先天免疫的强大分支并减少直接的补体介导损伤。这可能促成持久感染并加剧在重症 COVID-19 中观察到的复杂补体紊乱。尽管这些实验是在受控的实验室条件下进行的,但它们强调了 N–补体相互作用作为一个潜在的新靶点:阻断 N 与这些调节蛋白结合或恢复平衡的补体活性等疗法,未来或许能帮助将战局重新倾向于免疫系统一方。
引用: Víglaský, J., Bhide, K., Talpasova, L. et al. SARS-CoV-2 nucleocapsid protein forms complexes with soluble complement regulatory proteins that can bind to the virion. Sci Rep 16, 6599 (2026). https://doi.org/10.1038/s41598-026-37866-4
关键词: SARS-CoV-2 核衣壳蛋白, 补体系统, 免疫逃逸, 补体调节蛋白, COVID-19 严重程度