Clear Sky Science · zh
负载姜黄素的银-胺功能化二氧化硅纳米粒子混合体系的抗癌活性
把厨房香料变成更聪明的抗癌武器
姜黄,那种常见于咖喱中的亮黄色香料,含有姜黄素——一种长期以来因其健康益处(包括抗癌活性)而备受关注的天然化合物。但单独的姜黄素在水中溶解性差、在体内易被分解,且难以以有效剂量到达肿瘤部位。本研究描述了一种将姜黄素封装到微小工程化颗粒中的新方法,使其更稳定、更能靶向肿瘤并对癌细胞更具杀伤力,同时尽量减少对健康组织的损害。
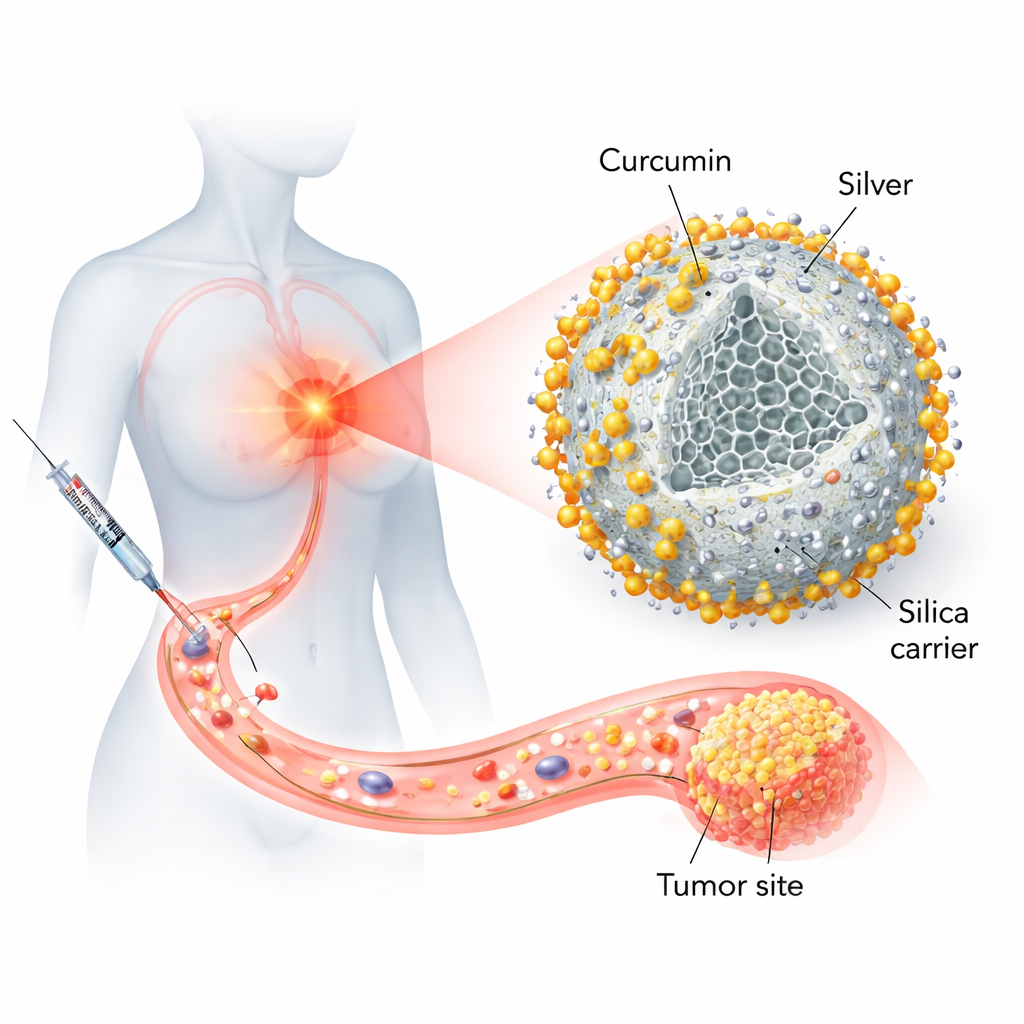
为何有前景的天然药物需要更好的载体
姜黄素可干扰癌细胞赖以生长和存活的多种过程。然而,当人们口服姜黄素时,大部分并不能到达肿瘤:它易聚集而非溶解、在血液中被迅速清除,且无法安全地大剂量注射。现有的递送系统——例如脂质颗粒或聚合物胶囊——在一定程度上有所改进,但通常载药量有限、可能不稳定或制造工艺复杂。与此同时,银纳米粒子已知可通过在细胞内产生活性分子来损伤细菌和癌细胞,但它们也可能不稳定且有时具有毒性。研究者因此着手将这两种成分——姜黄素和银——结合到一个精心设计的二氧化硅“壳”中,以稳定两者并在最需要的部位释放药物。
用“沙子”、银和姜黄素构建微小载体
研究团队首先制备了二氧化硅纳米粒子——由与沙子相同基本材料构成的纳米级球体——采用溶液法形成均匀、多孔颗粒。随后他们在表面引入胺基,这些化学“钩子”能改善银离子和姜黄素的结合。银被引入并牢固结合到这些胺基上,形成银-二氧化硅的混合框架。最后,从醇溶液中将从姜黄根部提取的姜黄素装载到该结构中。所得颗粒称为 CUR@Ag-AFS,在保持固态与均匀性的同时,达到相对较高的药物负载。一系列实验室表征确认颗粒为球形,硅、氧、氮、碳和银等元素存在,并且姜黄素以更无序、更稳定的形式嵌入,而非易碎的晶体。
设计为在肿瘤内释放更多药物
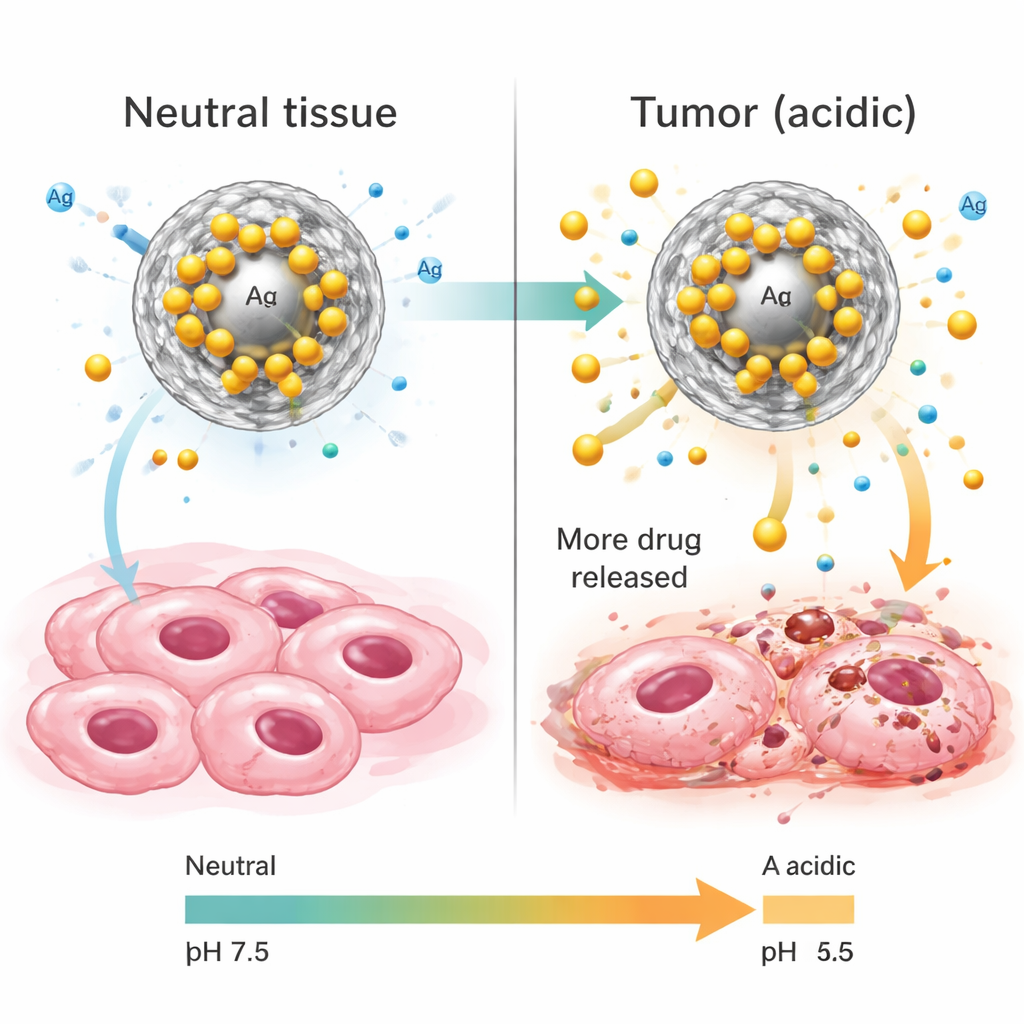
为测试新载体在不同环境下的行为,研究者将其置于模拟正常血液与组织(近中性pH)以及肿瘤和癌细胞胞室中更酸性的环境的流体中。24小时内,颗粒缓慢且稳定地释放姜黄素,但显示出明显的pH依赖性:在类似肿瘤细胞内部的酸性条件下释放量最大——超过90%的载药被释放——而在中性条件下释放明显较少。对释放数据的数学分析表明,姜黄素主要通过二氧化硅的孔道扩散出来,酸性环境削弱了姜黄素与颗粒表面之间的吸附作用。换言之,该系统被调校为在健康组织中相对“沉默”,而在癌变部位变得更活跃,从而在保持局部强效作用的同时可能减少副作用。
将这些颗粒用于对抗癌细胞的测试
随后团队将人体乳腺癌细胞(MCF-7)暴露于不同配方:纯二氧化硅、带胺基的二氧化硅、含银的二氧化硅、游离姜黄素和复合的 CUR@Ag-AFS 粒子。通过一种反映代谢活性的标准显色检测测量处理后的细胞存活率。在所有纳米粒子体系中,姜黄素—银—二氧化硅混合体对杀灭癌细胞最为有效,仅次于作为阳性对照的常规化疗药物多柔比星。与游离姜黄素或单独含银的颗粒相比,该混合颗粒在明显更低的浓度下就能达到相同的癌细胞杀伤效果,表明存在协同作用。重要的是,作为基底的二氧化硅框架本身表现出相对较低的毒性,表明大部分抗癌效力来自姜黄素—银的组合以及其递送方式。
这对未来癌症护理可能意味着什么
通俗地说,研究者构建了一种由二氧化硅制成的智能微观“海绵”,它吸附姜黄素和银,保护它们在循环过程中的稳定性,并在到达肿瘤的酸性环境后更快释放。这一设计既增强了姜黄素的杀癌能力,又有助于更直接地瞄准病变细胞,同时二氧化硅结构提供了稳定性和可控性。尽管这项工作仍停留在实验室和细胞培养阶段——尚未在动物或患者身上验证——但它指向了一个可能的未来:将像姜黄素这样的天然化合物与精心设计的纳米材料配对,可能有助于开发更具靶向性、更持久且对机体负担更小的癌症治疗方案。
引用: Shafqat, S.S., Wakeel, M., Zubair, M. et al. Anticancer activity of curcumin loaded hybrid system of silver-amine functionalized silica nanoparticles. Sci Rep 16, 7026 (2026). https://doi.org/10.1038/s41598-026-37829-9
关键词: 姜黄素纳米粒子, 靶向癌症治疗, 银纳米载体, pH响应药物递送, 乳腺癌细胞