Clear Sky Science · zh
基于多任务学习的阿尔茨海默病复杂性状预测的建模与应用
这项研究对家庭和患者为什么重要
阿尔茨海默病是我们这个时代最令人恐惧的诊断之一,但医生仍然难以预测谁会快速恶化、谁会保持多年的稳定,以及哪些早期迹象真正重要。本研究提出了一个简单但有力的问题:如果我们把多项与阿尔茨海默相关的测试结果和脑部影像一并考虑,并将它们与个体的遗传信息结合,现代人工智能能否学出有助于更准确预测疾病进程的模式?
同一种疾病的多种面貌
阿尔茨海默并不仅仅表现为记忆丧失。患者在认知测试表现、日常生活能力以及脑部影像表现上存在差异。这些不同的测量——例如常用的记忆与认知量表、关于日常功能的问卷以及反映脑代谢或淀粉样蛋白沉积的PET扫描——已知部分受遗传影响。重要的是,它们也共享部分相同的遗传根源。传统的预测方法通常一次只关注一个测量值,从而忽视了这些性状相互关联的有用事实。作者认为,正如能看到完整病情而非单一检测的医生一样,模型也应当从多个相关性状中共同学习。
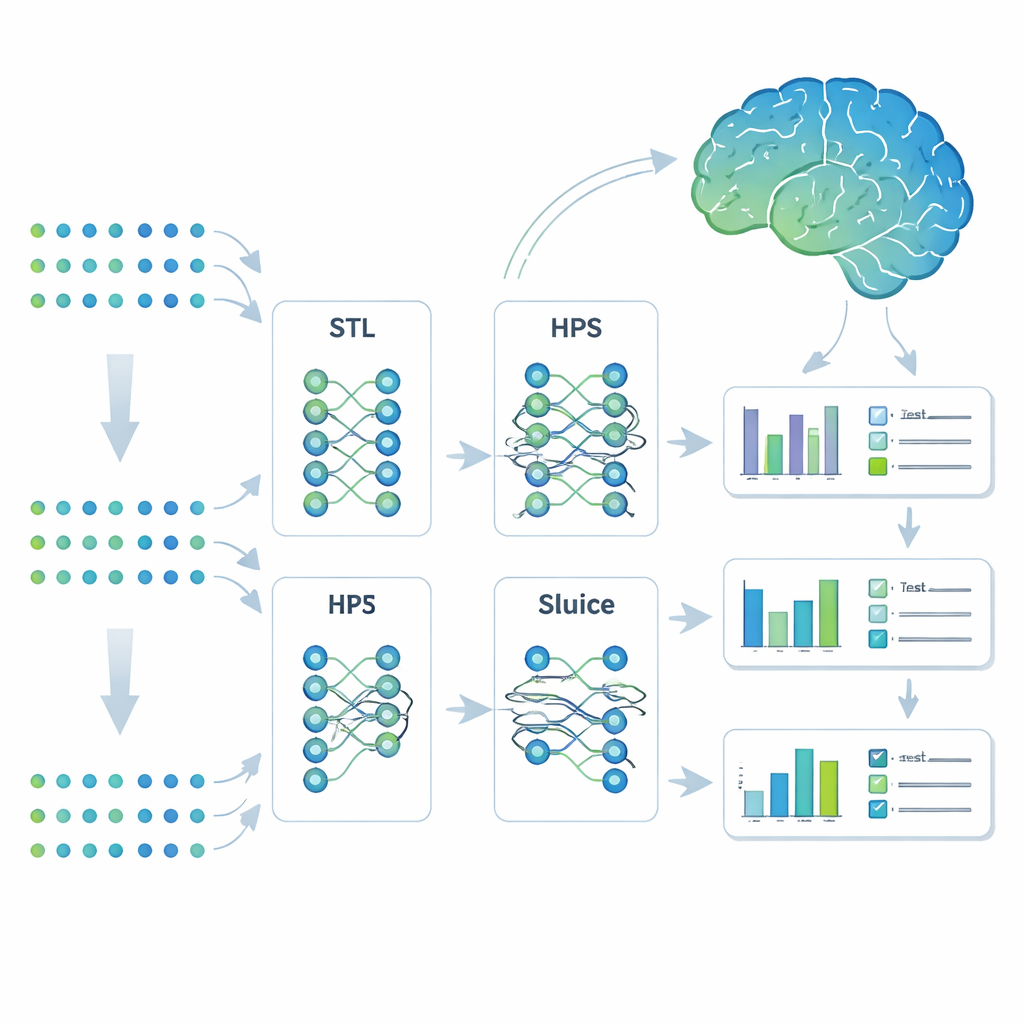
教一个模型去做多项相关任务
研究人员采用了一种称为多任务学习的机器学习策略。他们没有为每个结果构建独立模型,而是训练了一个系统同时预测七项与阿尔茨海默相关的性状。他们比较了四种方法:完全独立的模型(单任务学习)、只在末端才分开的简单共享模型(硬参数共享)、可将任务分为子组的更灵活的分支式设计,以及一种高度可调的结构——Sluice Network(可微调每层共享信息量)。四种模型使用相同的遗传输入;差别在于它们如何在性状之间共享所学到的信息。
在模拟基因组中检验想法
在将任何模型应用于真实患者之前,团队基于来自阿尔茨海默病神经影像倡议(ADNI)的真实遗传模式构建了可控的详细模拟数据集。他们创建了多种情景:所有性状共享相同遗传原因、性状形成部分重叠的群组、以及每个性状有不同的遗传原因。他们还改变了遗传信号的强度和添加噪声的量,以模拟人类数据的杂乱现实。在几乎所有条件下,Sluice Network 给出了最准确的预测,并在性状相关性较弱时仍保持稳定。更简单的共享模型在性状共享大量遗传因素时表现良好,但在共享较少时效果下降;而完全独立的模型虽然稳定,但整体准确性较低。
真实数据与基因分组的威力
随后,作者将这些模型应用于来自463名个体的真实ADNI数据,使用近3,800个来自此前与阿尔茨海默相关的56个基因的遗传标记。在这里他们加入了一个受生物学启发的改进:不是直接输入成千上万的单个位点标记,而是先按基因对标记进行分组,让网络为每个基因学习一个紧凑的“汇总”信号,再用这些基因级别的信号去预测七项结果。基因水平的聚合提升了大多数模型的性能,尤其是对Sluice Network的提升显著 —— 它与真实结果的平均相关性大约翻倍。收益在PET影像测量以及某些认知和功能评分上最为明显,这表明将微弱的遗传效应在基因层面合并,比把它们视为孤立标记更容易检测到。
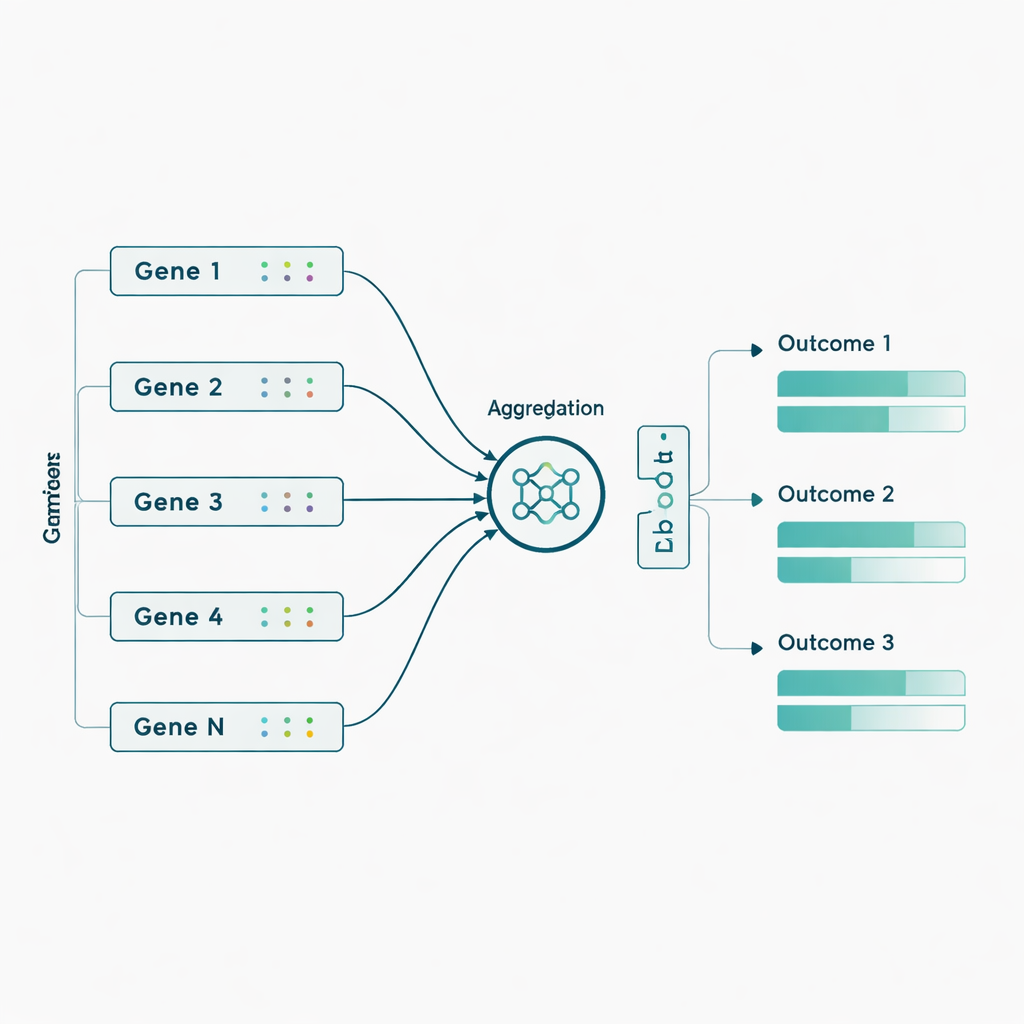
这对未来预测与护理意味着什么
对非专业读者而言,结论是更聪明、更灵活的人工智能模型能够通过同时从多项相关结果中学习并尊重基因这一生物学组织方式,从相同的遗传与临床数据中挤出更多见解。尽管目前的提升仍然有限,远未达到临床检测的水平,但这种方法指向了更可靠的个体风险估计、进展追踪以及潜在的监测或干预个性化工具。在像阿尔茨海默这样的复杂疾病中,许多微小的遗传效应相互作用,跨性状共享信息并聚合弱信号的方法,可能比传统的逐一性状评分提供更清晰、更有信息量的视角。
引用: Zhou, W., Xue, Z., Liang, J. et al. Modeling and application of alzheimer’s disease complex trait prediction based on multi-task learning. Sci Rep 16, 7749 (2026). https://doi.org/10.1038/s41598-026-37820-4
关键词: 阿尔茨海默病遗传学, 多任务学习, 深度学习预测, 神经影像生物标志物, 基因水平聚合