Clear Sky Science · zh
荧光分子探针 Cy7-SYL3C 在 EpCAM 阳性结直肠癌小鼠模型中的生物分布与靶向性初步评估
这对癌症检测为何重要
结直肠癌是全球致死率较高的癌症之一,部分原因在于许多肿瘤被发现得较晚。目前的主要筛查工具为结肠镜检查,虽然有效但具有侵入性且不适,因而不少人回避。该研究探索了一种新型“智能示踪剂”——会发光的探针,未来有望帮助医生用光学手段而不是手术刀或长管镜更早、更清晰地发现肠道肿瘤。
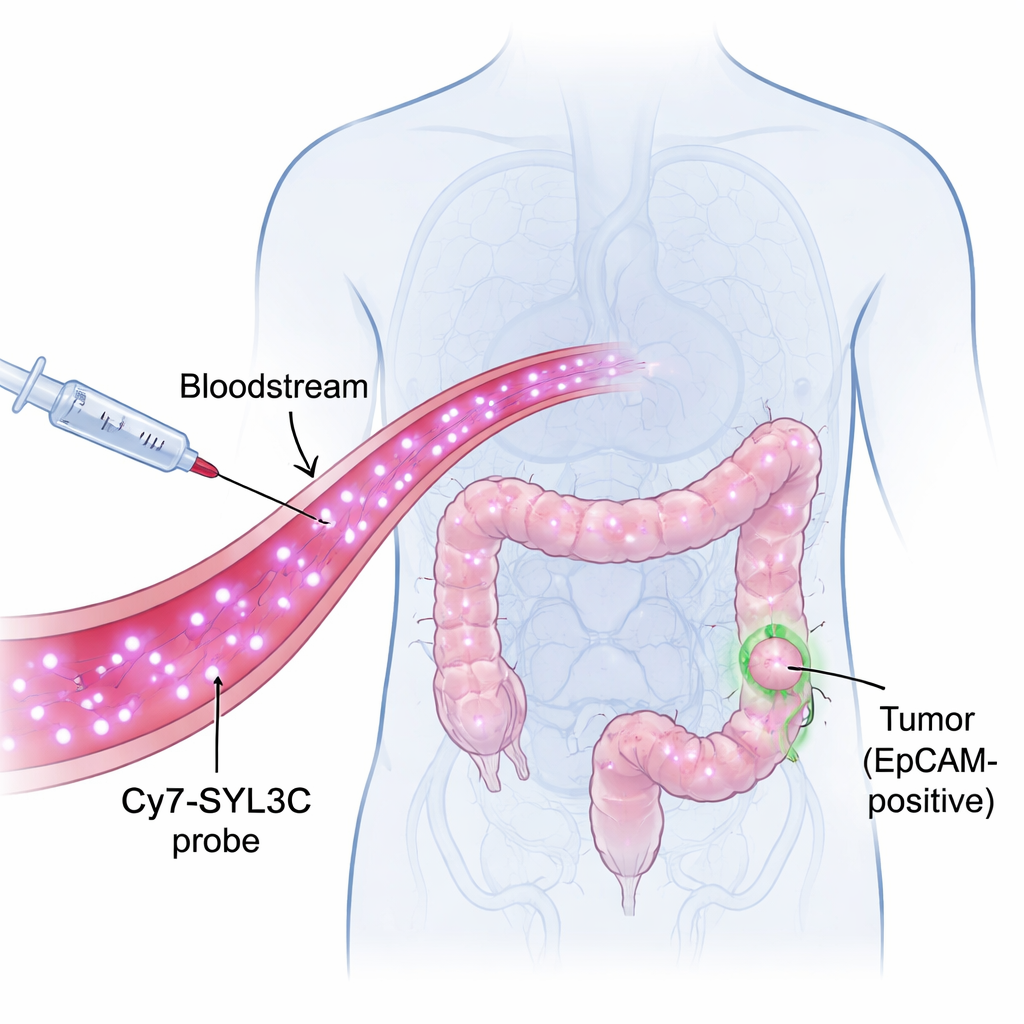
识别肿瘤细胞的发光标签
研究者将注意力集中在一种名为 EpCAM 的分子上,它存在于许多结直肠癌细胞表面,而在健康组织中较少见。他们构建了名为 Cy7-SYL3C 的探针:将近红外染料(Cy7)连接到一种短 DNA 链——适配体(SYL3C),该适配体能够像钥匙开锁般识别 EpCAM。近红外光肉眼不可见,但可穿透数毫米组织,使相机能够从体内捕捉到高对比度的信号。思路很直接:把 Cy7-SYL3C 注入血液,让它寻找富含 EpCAM 的肿瘤细胞,然后用专用相机使这些细胞在暗色背景中发光。
在实验室检测安全性与稳定性
在活体动物试验之前,团队先评估了探针的稳定性和安全性。他们将 Cy7-SYL3C 与小鼠和牛的血清混合,发现大部分探针在至少八小时内保持完整,足够用于医疗操作期间的成像。随后,他们用不同浓度的探针处理人结直肠癌细胞和正常结肠细胞,细胞生长基本未见变化;当探针与红细胞混合时,也未导致红细胞破裂。这些测试表明 Cy7-SYL3C 在化学上较为稳定且对细胞温和——这是任何可能用于患者的成像剂所需的关键特性。
探针在体内的分布路径
接着,科学家们使用小动物成像系统追踪了 Cy7-SYL3C 在健康小鼠体内的去向。注射后不久,最强的信号出现在肝脏和肾脏,这两个器官负责从血液中过滤和清除物质。肝脏信号在大约一小时达到峰值后逐渐减弱,而肾脏的荧光持续更久,表明尿液是该探针的主要排泄路径。两天后,仅剩少量初始信号,且对主要器官的显微检查未见明显组织损伤。这意味着在短期研究中,探针清除较快且未对重要器官造成可见伤害。
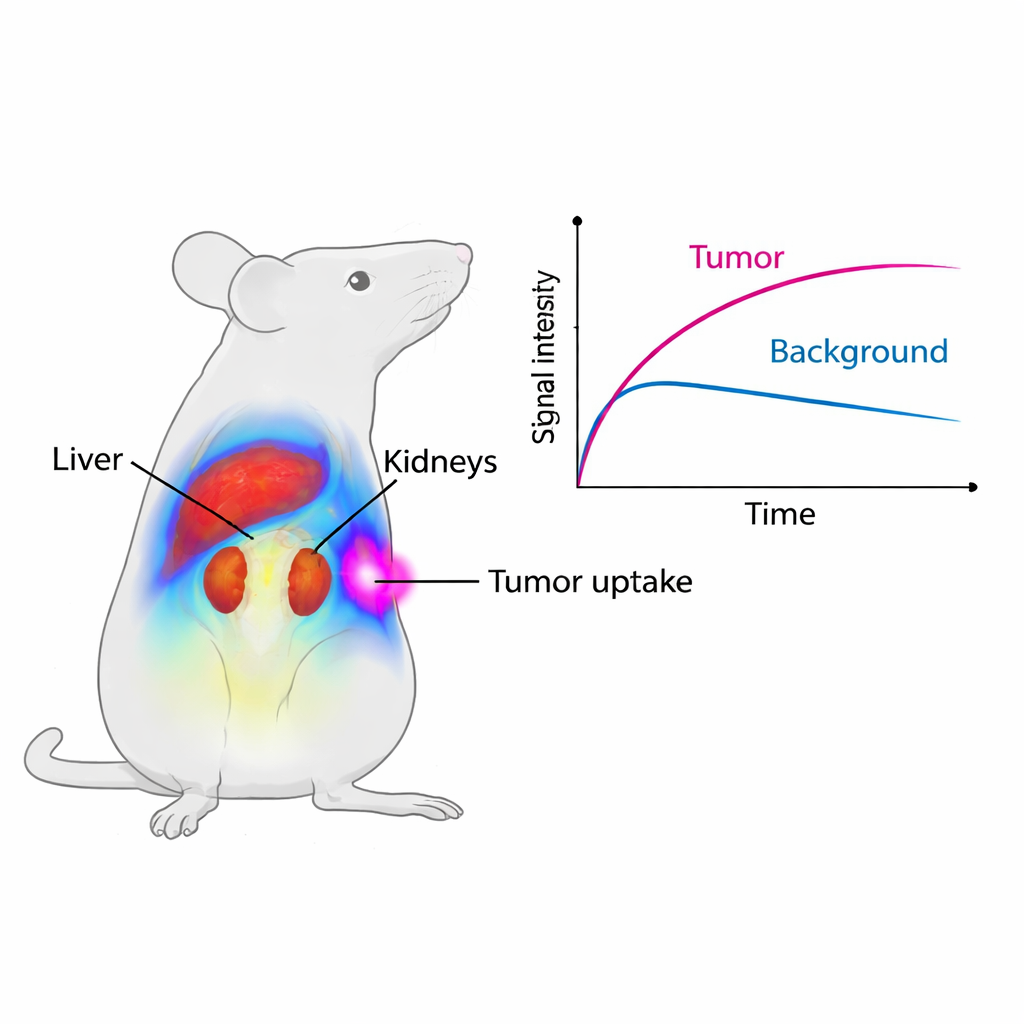
聚焦结直肠肿瘤
为验证 Cy7-SYL3C 是否确实靶向癌症,研究团队使用植入了产生 EpCAM 的人类结直肠肿瘤的小鼠模型。注射后仅五分钟,肿瘤就在成像系统上开始发光。在最初四小时内,肿瘤的平均信号强度几乎是那些用过量未标记 SYL3C 进行“预阻断”小鼠的两倍——预阻断会临时占据 EpCAM 位点,阻止带荧光的探针结合。肿瘤信号与邻近肌肉的比值在八小时左右达到峰值,说明在一个有用的成像时间窗内,肿瘤明显比周围组织更亮。显微镜级的详细研究证实,荧光探针与肿瘤细胞上的 EpCAM 染色重叠,而在正常器官中则几乎没有或没有 EpCAM 表达。
这将如何指导未来的手术与诊断
对非专业读者而言,主要结论是 Cy7-SYL3C 表现得像一种智能染料:能寻找结直肠癌细胞,随后主要通过肾脏被洗脱。它似乎稳定、对细胞温和,且能够快速且持续数小时使肿瘤发光,这可能帮助外科医生实时更清晰地看到肿瘤边界,或帮助放射科医生在微创操作中识别可疑部位。尽管这些结果来自早期小鼠实验,且要用于人体之前仍需更多工作,本研究为一类基于光学的示踪剂奠定了重要基础,有望使结直肠癌的检测和手术更精确、创伤更小。
引用: Li, Y., Li, M., Li, P. et al. Preliminary assessment of biodistribution and targeting of the fluorescent molecular probe Cy7-SYL3C in an EpCAM-positive colorectal cancer mouse model. Sci Rep 16, 6589 (2026). https://doi.org/10.1038/s41598-026-37787-2
关键词: 结直肠癌成像, 近红外荧光, EpCAM 靶向, 适配体探针, 肿瘤手术引导