Clear Sky Science · zh
SIRT3通过调控IDH2乙酰化抑制肾癌进展
这项肾癌研究的重要性
肾癌,尤其是一种称为肾细胞癌的类型,发病率在增加,而且一旦发生转移通常难以治疗。本研究深入观察癌细胞内部,研究其能量工厂线粒体中微小变化如何助长肿瘤生长——以及一种天然植物化合物厚朴酚可能如何减缓这一过程。对读者而言,它展示了理解细胞“家务管理”如何为现有药物之外开辟新的治疗选择。
肾细胞内的一个隐形刹车
我们的细胞不断管理能量产生和有害副产物。在健康肾细胞中,一种名为SIRT3的蛋白在细胞线粒体内类似维护主管,保持其他蛋白处于良好状态。作者分析了大型公开癌症数据库和患者组织样本,发现肾肿瘤中SIRT3水平持续低于邻近正常组织。SIRT3最低的肿瘤表现出与更快生长和更强迁移能力相关的基因模式,这表明当这个细胞级的刹车丧失时,癌细胞会变得更具侵袭性。
癌细胞如何扭曲能量平衡
为检验SIRT3缺失是否真能驱动癌性行为,研究人员在体外培养的肾癌细胞系中降低了SIRT3表达。SIRT3减少的细胞增殖更快并形成更多克隆,表明其存活和生长能力增强。当这些改造细胞移植到小鼠体内时,形成的肿瘤比对照细胞产生的肿瘤更大、更重。这些实验共同表明,SIRT3在肾癌中不仅是缺失的——其存在时确实抑制肿瘤生长。
一个关键酶与细胞内“生锈”问题
研究组随后聚焦于另一种线粒体蛋白IDH2,IDH2有助于生成NADPH——这种分子为清除活性氧(ROS,类似细胞“生锈”的有害化学物)提供能量。IDH2的功能可被一种称为乙酰基的小化学标签改变,而SIRT3以去除此类标签而闻名。在肾癌细胞中,SIRT3与IDH2发生物理结合,并在特定位点(K413)去除乙酰化标记。当SIRT3被减少时,该乙酰标记积累,IDH2效率下降,NADPH水平降低,ROS水平上升。线粒体膜电位部分丧失,显示功能受损。通过使用模拟乙酰化或去乙酰化状态的工程化IDH2变体,作者证明了乙酰化形式可以覆盖SIRT3的抑制生长作用,将这一细胞刹车直接关联到这一处化学开关。
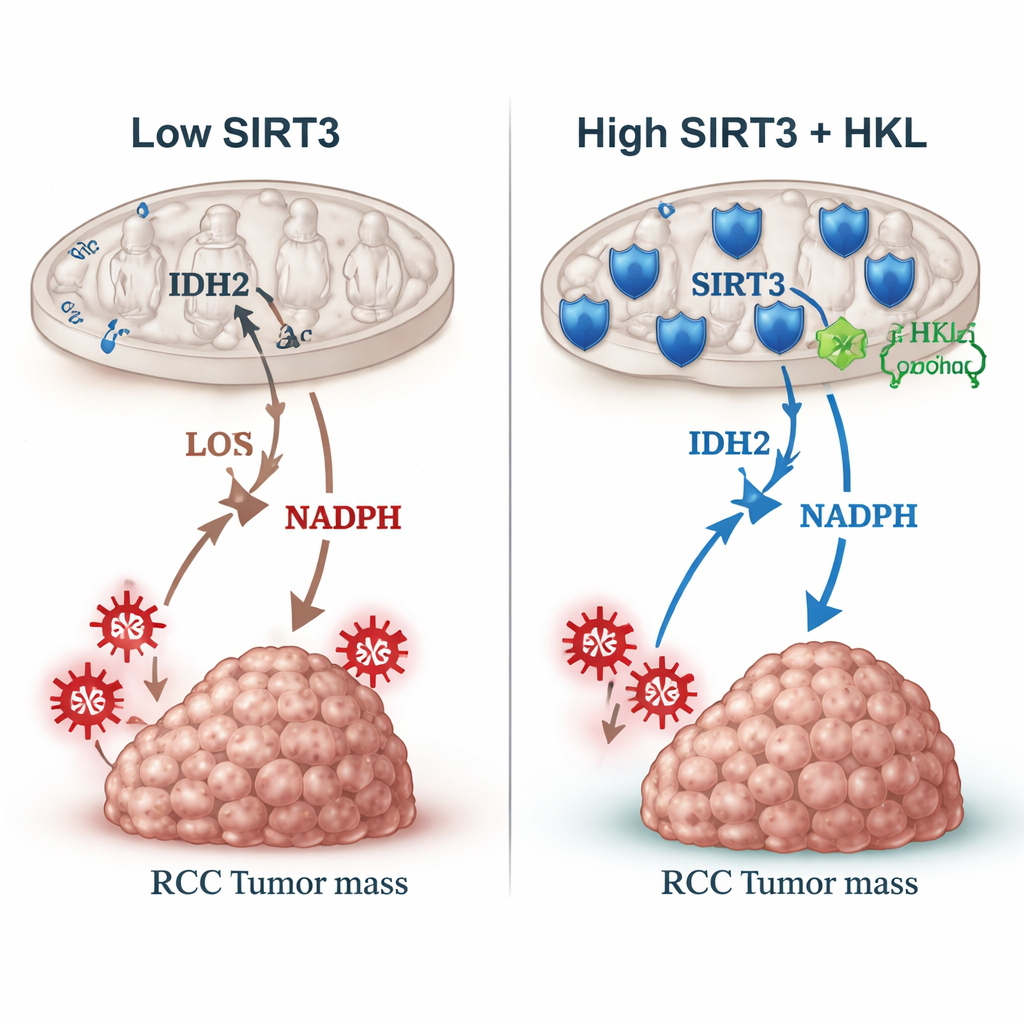
用植物化合物重新启动刹车
鉴于SIRT3具有保护作用,作者探问是否可以用药物将其增强。他们测试了厚朴酚,这是一种来自木兰科树皮的天然分子,已知影响多条癌症通路。在一个精心选择、不直接导致细胞灭活的剂量下,厚朴酚随时间在肾癌细胞中提高了SIRT3水平,并伴随相关调控因子(p-AMPK和PGC-1α)的上调。随着SIRT3水平上升,IDH2失去乙酰标签,ROS下降,细胞增殖与克隆形成减慢。当厚朴酚与标准肾癌药物舒尼替尼联用时,两者对生长的抑制超过单用舒尼替尼,部分原因是厚朴酚减轻了舒尼替尼本身可能诱导的过量ROS。研究者使用经典抗氧化剂时也观察到类似效果,支持通过控制氧化应激能增强现有治疗的观点。
这对未来治疗的意义
对非专业读者而言,结论是这项研究识别出SIRT3作为肾癌中的一种天然肿瘤刹车,其作用通过对IDH2和线粒体内保护性与有害分子之间平衡的精细调控实现。当SIRT3水平低时,细胞内会积累促进损伤的ROS并获得生长优势。恢复SIRT3活性——可能通过厚朴酚或未来更精确的药物——有望减缓肿瘤生长并帮助现有疗法更有效。尽管厚朴酚本身仍面临包括吸收性和多靶点等障碍,这项工作指向了清晰的通路:SIRT3–IDH2–氧化还原轴,药物开发者现在可以针对这一代谢相关路径设计更智能的肾细胞癌治疗策略。
引用: Li, L., Tian, Y., Chen, S. et al. SIRT3 suppresses renal cancer progression by regulating IDH2 acetylation. Sci Rep 16, 7619 (2026). https://doi.org/10.1038/s41598-026-37783-6
关键词: 肾癌, SIRT3, 线粒体, 氧化应激, 厚朴酚