Clear Sky Science · zh
通过泊马利度胺与帕诺比司他协同靶向ARID2–MYC轴克服多发性骨髓瘤的先天IMiD耐药性
这项研究对患者的重要性
多发性骨髓瘤是一种发生在骨髓中产生抗体细胞的癌症,尽管可治疗性已有很大提高,但仍很少能治愈。许多患者最终对标准药物失去反应,医生的治疗选择因此减少。该研究探讨了为何将两类现有药物——所谓的IMiD类(如泊马利度胺)与影响染色质结构的组蛋白去乙酰化酶(HDAC)抑制剂(如帕诺比司他)联合使用,能够协同杀伤骨髓瘤细胞,即便肿瘤已对单用IMiD产生耐药性。理解这种分子层面的协作机制可为更优的联合治疗提供依据,使更多患者受益于现有药物。
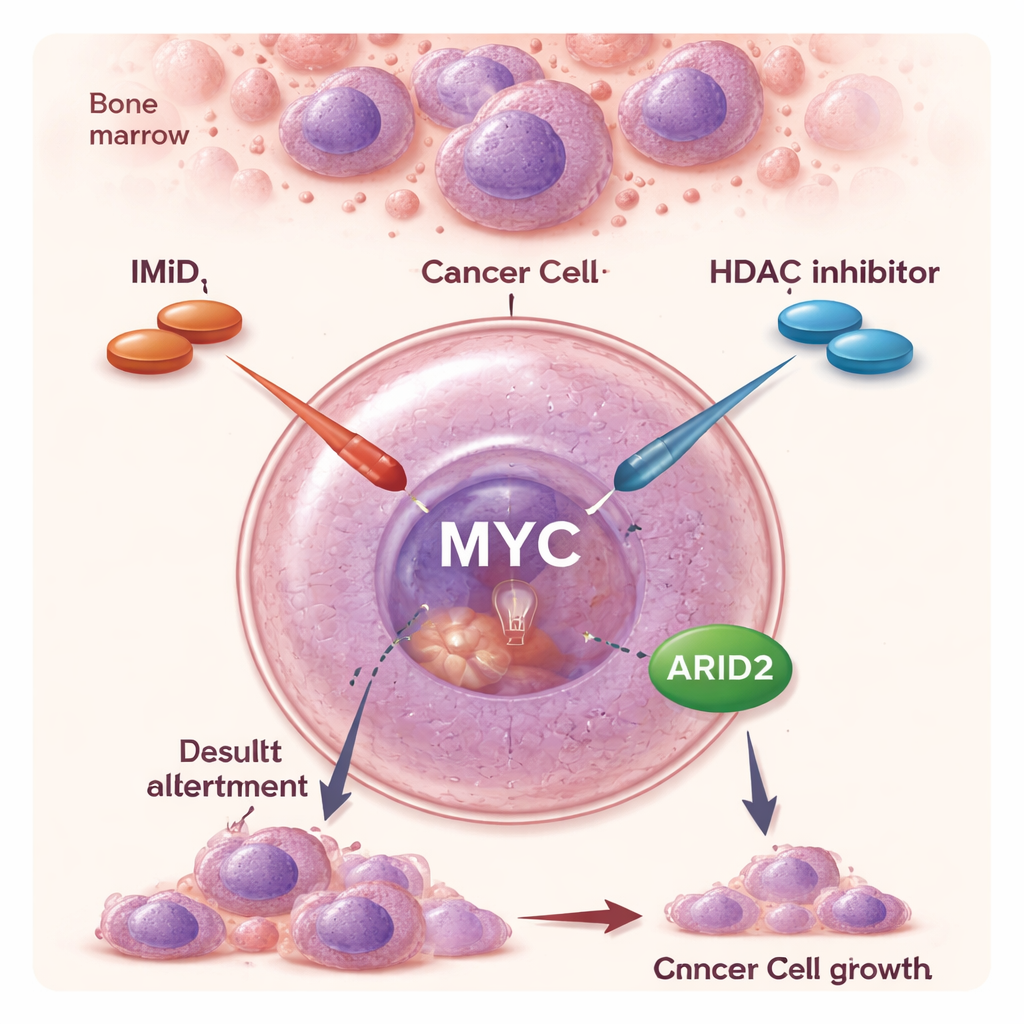
两类老药,一个新组合
过去二十年,IMiD和其它靶向药物显著延长了多发性骨髓瘤患者的生存期。IMiD的作用机制有别于简单地抑制某一蛋白:它们通过促使特定蛋白被标记降解,从细胞中清除这些蛋白,从而削弱骨髓瘤细胞依赖的关键信号。像帕诺比司他这样的HDAC抑制剂则以不同方式起效:它们放松DNA的紧密包装,广泛改变基因的开启或关闭。作为单药,HDAC抑制剂效果有限且可能带来副作用,但临床试验提示将其与IMiD联合能产生更强的抗癌反应,包括在那些对IMiD单药已不再敏感的患者中。然而,这种协同作用的分子基础一直不清楚。
共同的压力点:压低MYC
研究人员系统测试了多种IMiD与不同HDAC抑制剂在一系列骨髓瘤细胞系上的组合,并用标准评分体系衡量组合疗法较单药的增强效果。他们发现泊马利度胺加帕诺比司他在多数细胞模型中显示出特别强的协同效应,且该效应依赖于一个名为cereblon的蛋白——IMiD通过它将“靶标”蛋白引向降解。通过分析全基因表达,研究团队发现帕诺比司他及其它广谱HDAC抑制剂显著抑制MYC这一常被称为癌细胞“致癌引擎”的关键生长基因,而IMiD在同一节点上施加额外压力。当科学家强制使骨髓瘤细胞从一个对药物不敏感的来源持续表达MYC时,这对药物组合的强效几乎消失,表明抑制MYC是二者协同作用的核心。
通过替代途径攻破耐药
部分骨髓瘤细胞对IMiD固有耐药:尽管预期的早期靶标被降解,但MYC和其它生存信号并未得到有效沉默,细胞仍继续生长。在一个这样的耐药模型中,早期靶标到MYC的标准IMiD途径被“解耦”。研究团队探究是否存在替代路线将IMiD作用传递到MYC上。他们关注ARID2——SWI/SNF这一大型染色质重塑复合体的一个组成部分。先前研究表明,泊马利度胺能将ARID2标记降解,从而帮助降低MYC。在耐药细胞中,泊马利度胺单用仅能温和降低ARID2,部分原因是细胞对其作出增加ARID2产量的反馈反应。当加入帕诺比司他时,它抑制了ARID2基因本身,克服了该反馈回路。两药联用显著降低了ARID2蛋白继而降低MYC,即使在对IMiD耐药的细胞系中也能强烈诱导癌细胞死亡。
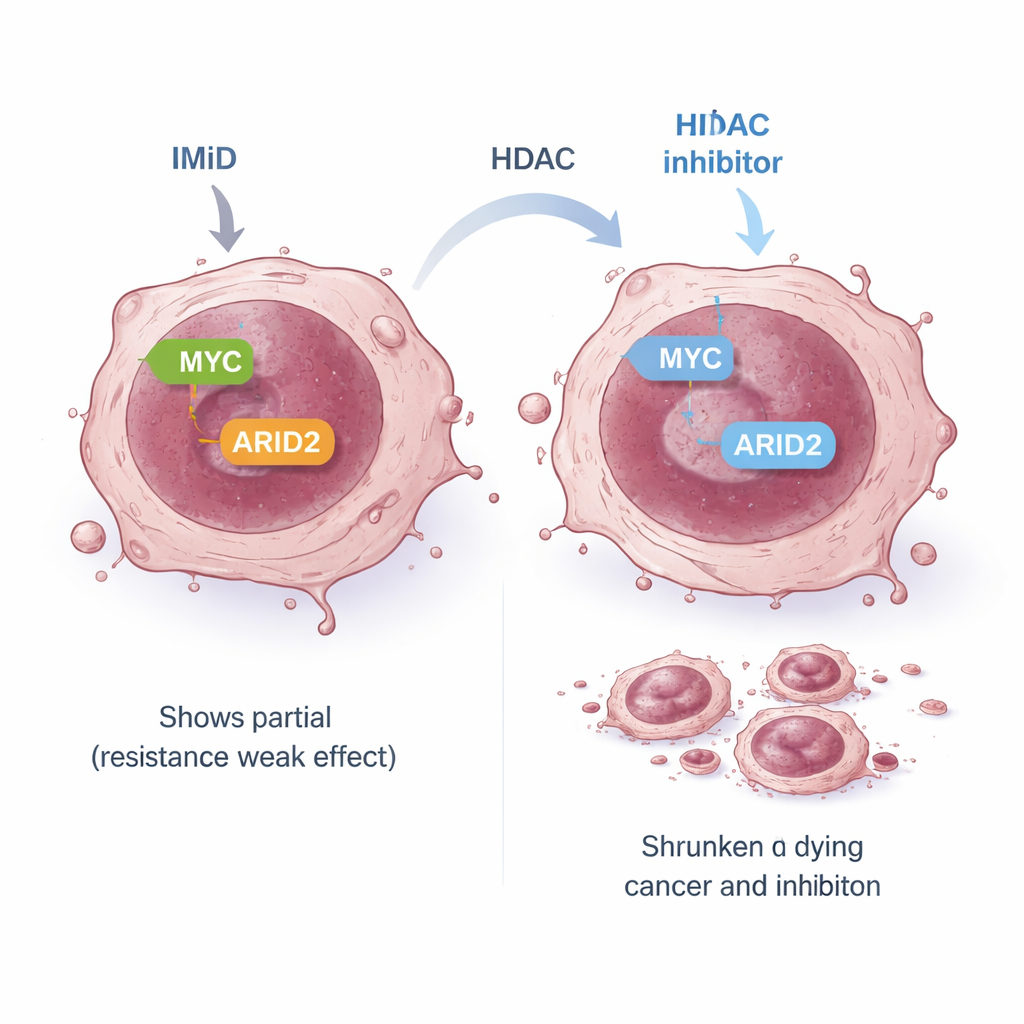
揭示癌细胞更广泛的薄弱环节
由于ARID2只是SWI/SNF复合体的一个成员,作者怀疑整个复合体是否是一个治疗薄弱点。他们发现HDAC抑制剂能降低多个SWI/SNF组分的水平,而一种旨在阻断该复合体核心发动机(BRG1/BRM)的小分子药物单用即可减缓骨髓瘤细胞生长并降低MYC。重要的是,这种SWI/SNF抑制剂也能与泊马利度胺和帕诺比司他产生协同作用,三药组合则将ARID2和MYC进一步压低,同时强烈抑制细胞增殖。通过探查具体参与的HDAC酶类,研究人员强调HDAC1是维持ARID2–MYC通路的关键因子,而其它HDAC似乎通过并行途径影响MYC。
这对未来骨髓瘤治疗意味着什么
对于非专业读者,核心信息是:骨髓瘤细胞似乎依赖于以MYC为中心的共享“生长控制枢纽”,并且通往该枢纽的道路不止一条。标准IMiD治疗主要打击其中一条道路;在某些耐药癌症中,那条道路被阻断,导致MYC保持活性。本研究表明,一条替代途径——通过ARID2和SWI/SNF复合体——仍然畅通,而将帕诺比司他与泊马利度胺联用可以关闭这条路。通过刻意组合从多个方向施压MYC的药物,临床上可能克服某些先天性耐药形式,同时有望降低单药剂量。尽管仍需更多的临床前和临床研究,这些发现为为难治性多发性骨髓瘤患者设计更智能、基于机制的联合方案提供了更清晰的蓝图。
引用: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
关键词: 多发性骨髓瘤, 药物耐药, 泊马利度胺, 帕诺比司他, MYC