Clear Sky Science · zh
胶质瘤的脂质代谢分类
为什么脑肿瘤中的脂质重要
被称为胶质瘤的脑肿瘤是最危险的癌症类型之一,但看似相同诊断的患者结局可以大相径庭。本研究提出了一个看似简单但意义深远的问题:肿瘤如何利用脂肪——机体的脂质——会如何影响其侵袭性、对治疗的反应,以及我们是否能在常规脑部影像上识别这些差异?通过追踪数百例肿瘤的脂质利用模式,作者发现了胶质瘤中隐藏的亚型,这些发现可能改变医生对预后预测和疗法设计的方式。
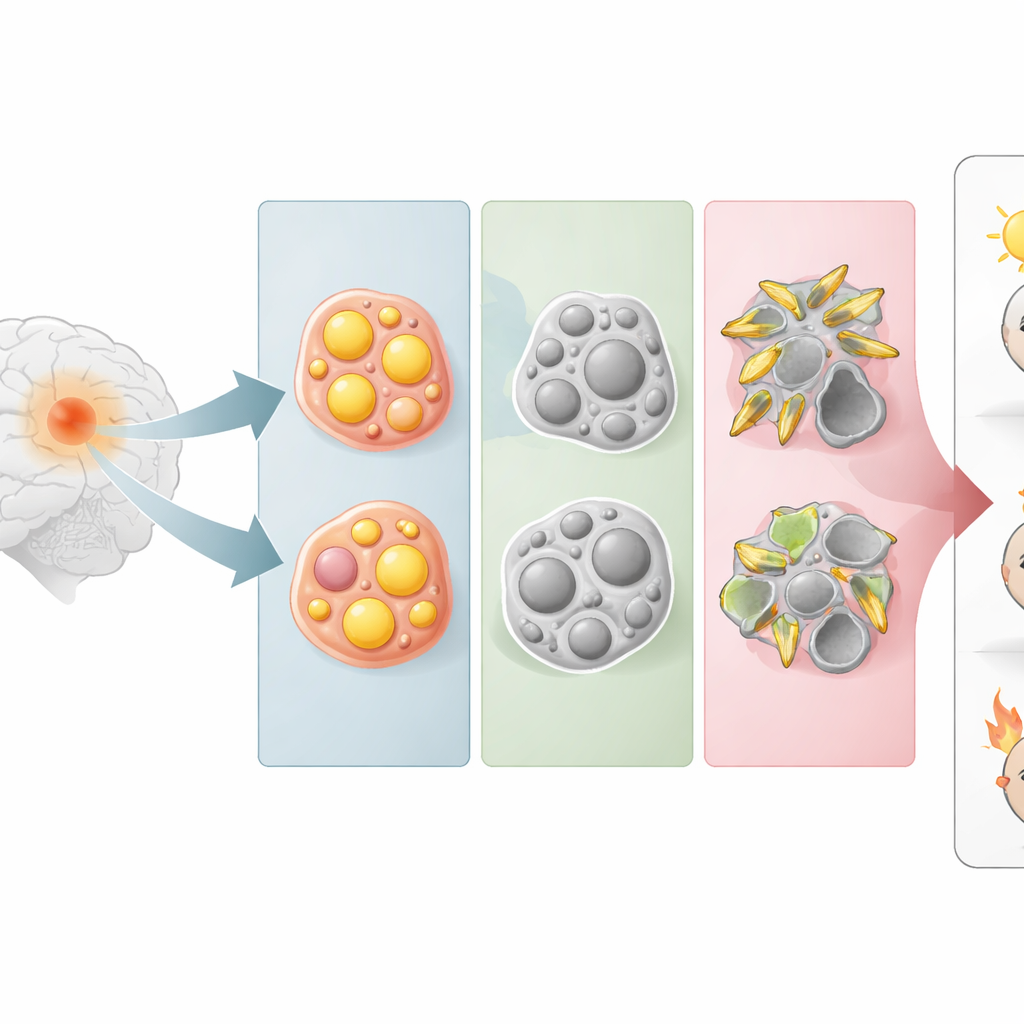
同一类脑肿瘤的三张隐秘面孔
研究者没有从显微镜下的细胞形态出发,而是按肿瘤激活五条主要脂质通路的强度进行分组,这些通路包括处理类固醇脂、甘油三酯和鞘脂(细胞膜的重要构件)等路径。利用来自大型公共肿瘤数据库的基因表达谱,他们发现胶质瘤自然分成三类:一类主要依赖类固醇代谢(ST型),一类偏向甘油三酯代谢(TC型),还有一类偏向鞘脂代谢(SP型)。这些代谢分型跨越了经典的肿瘤分类,揭示了在外观不同的胶质瘤中也存在具有相似脂质利用习性的细胞。
从代谢到患者预后
接着团队探讨了这三种脂质使用风格与真实世界结局的关联。属于ST型的患者总体存活时间最长,这类肿瘤更常为低级别并携带已知的有利基因改变。相反,SP型肿瘤通常为高级别的胶质母细胞瘤,缺乏保护性突变,并更多见于老年患者。即使在统计学上校正了肿瘤级别和关键基因标志后,属于SP型仍然能独立预测更差的预后,表明肿瘤处理鞘脂的方式捕捉到常规检测遗漏的危险维度。
脑内的敌对生态圈
深入分析肿瘤微环境——即癌周围的免疫细胞、血管和支持组织——发现SP型肿瘤展现出拥挤且冲突的免疫景观,既有攻击性免疫细胞也有抑制性细胞,并伴随强烈的信号抑制有效的抗肿瘤反应。与快速细胞生长、侵袭、新血管生成、瘢痕形成和炎症相关的通路在该亚型中更为活跃。用于估计肿瘤对放疗反应的指标显示,SP型胶质瘤对放疗最具耐受性,这与其较差的生存率相吻合。相比之下,ST型肿瘤在这些侵袭性特征上显得更“平静”。
从MRI影像读取肿瘤代谢
由于外科取样具有侵入性并非总可行,研究者尝试评估常规磁共振成像(MRI)是否能提示肿瘤的脂质行为。他们从两种常见的MRI序列中提取了两千多项细微的纹理与形状特征,并训练机器学习模型以区分SP型与其他肿瘤。该模型在医院训练集和独立的公共验证集中均表现良好,比随机猜测更常准确地区分出SP型肿瘤。这提示特别具有侵袭性的代谢指纹会在常规脑部影像上留下可检测的印记。
处于侵袭性网络中心的关键基因
为了从宏观通路找到具体靶点,团队寻找在脂质相关网络中处于核心地位、在SP型肿瘤中强烈过表达、与差生存相关并能区分SP型的基因。三种基因——GLA、GLB1和HSD3B7——符合所有标准。它们在SP型胶质瘤中均更为活跃,并共同构成了一个有力的诊断签名。作者重点关注HSD3B7,该基因在脑肿瘤中的作用此前鲜有研究。来自100例胶质瘤患者的组织染色显示,HSD3B7蛋白在更晚期、更恶性的肿瘤中表达更高,且肿瘤HSD3B7水平高的患者生存显著更短。
一个脂质基因如何重塑肿瘤生态系统
单细胞分析揭示,HSD3B7不仅在癌细胞中活跃,在数种免疫和支持细胞类型中也有表达。该基因高表达与促血管生成、慢性炎症和免疫逃逸的一系列信号相关联。某些保护性细胞类型之间的通讯减弱,而支持肿瘤生长的细胞内部自我强化回路增强。总体来看,这些模式表明HSD3B7活性升高有助于形成并维持一个有利于肿瘤生长和治疗耐受的敌对微环境。
对患者与未来护理的意义
在实践层面,这项工作表明胶质瘤可以根据脂质代谢有意义地划分为三种亚型,其中以鞘脂占优的SP型尤为危险且耐疗。这些差异不仅是学术上的:通过先进的影像分析可以从常规MRI读出,并可追溯到像HSD3B7这样的具体基因,后者可能成为未来的药物靶点。尽管仍需实验研究来检验阻断这些脂质通路是否能减缓肿瘤或提高放疗效果,该研究提供了一个新的代谢视角来观察脑癌,并推动该领域向更个体化、基于生物学的治疗决策迈进。
引用: Tu, S., Zhang, P., Chi, X. et al. Lipid metabolism classification of gliomas. Sci Rep 16, 8219 (2026). https://doi.org/10.1038/s41598-026-37697-3
关键词: 胶质瘤, 脂质代谢, 脑肿瘤影像, 放射组学, 肿瘤微环境