Clear Sky Science · zh
在候选基因中通过全转录组鉴定与牛分枝杆菌肠病相关的有害变异
隐匿在昂贵牛病背后的基因
牛分枝杆菌肠病,也称约翰氏病,悄然削弱着全球奶牛群的健康与产能,每年给养殖者带来数亿美元的损失,并引发对其与人类肠道疾病关联的担忧。本研究深入霍尔斯坦牛的遗传层面,提出一个简单却关键的问题:基因上的哪些差异可能让部分动物抵抗感染,而另一些则不幸受累?通过测读血液和肠道组织中的 RNA——基因的工作拷贝,研究者追踪到关键免疫基因中细微的 DNA 变化如何影响疾病走向。
为什么这种牛病很重要
分枝杆菌肠病由细菌 Mycobacterium avium 亚种 paratuberculosis(MAP)引起。牛通常在生命早期感染,但症状往往在多年后才出现。在隐匿和亚临床阶段,动物看起来健康,但可能低水平排菌并产生较少牛奶。在临床阶段,牛会出现慢性腹泻、严重消瘦和产奶量大幅下降。许多地区的群体感染率可超过50%,包括欧洲和北美的部分地区,造成经济和动物福利上的挑战。由于该细菌也可能作为环境触发因子与克罗恩病等人类炎症性疾病相关,人们日益呼吁改善在牛群中的控制策略。
解读工作中的基因组
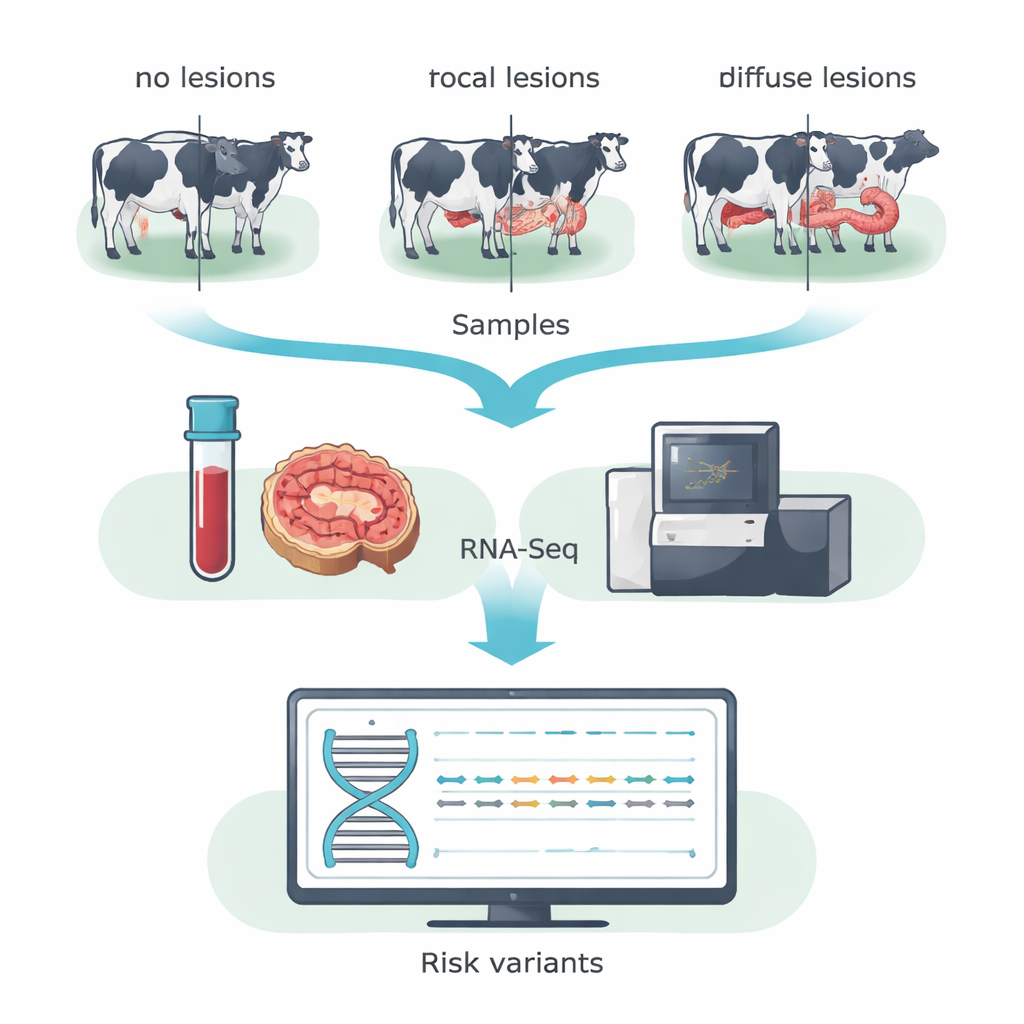
研究团队没有扫描整个 DNA 序列,而是使用 RNA 测序(RNA-Seq)聚焦于动物体内实际活跃的基因。他们从西班牙一处奶牛群的 14 头霍尔斯坦牛采集了血液和回盲瓣(MAP 高度影响的肠道区域)样本。根据肠道组织的显微检查结果,牛被分为三类:无可检测病变的动物、出现小而局限(局灶性)病变的动物(典型的长期亚临床感染),以及出现严重、广泛(弥漫性)病变并与临床疾病相关的动物。通过在每组内合并血液和肠道的数据,研究者提高了检测在表达基因中单个碱基变化(即编码区 SNPs)的能力。
在关键免疫基因中发现有害变异
在数十万种变异中,研究团队将注意力集中在那些改变蛋白质序列并被预测为损害蛋白功能的变异——所谓的有害变异上。他们应用严格的过滤以确保高置信度,然后使用已有的预测工具标记出风险变异。这一筛选过程揭示了无病变牛独有的 31 个此类变异、局灶性病变牛独有的 15 个变异,以及弥漫性病变牛独有的 31 个变异。其中许多落在指导免疫细胞识别与清除感染、调控细胞凋亡与管理代谢的基因上。一个突出发现是 BOLA 基因家族,这是牛类的主要组织相容性复合体 II 类(MHC II),帮助免疫细胞将细菌片段呈递给 T 细胞。在三组牛中都发现了不同的潜在有害 BOLA 变异,提示特定的 BOLA 等位本可能使动物倾向于抵抗、受控感染或有害炎症。
从 DNA 变异到疾病通路
为理解这些基因变化在实际中的意义,研究者检查了每组富集的生物学通路。无病变牛显示在与抗原加工、囊泡运输和肠道免疫平衡相关的基因中存在差异变异,包括 BOLA、AP3B1 和 CHGA。这些变化可能促进免疫细胞内对细菌的高效消化和维持限制损伤的稳定肠道环境。在出现局灶性病变的牛中,有害变异集中在抑制程序性细胞死亡并调节细胞代谢的基因(如 ORMDL3 和 KANK2),这可能帮助宿主在长期亚临床阶段保持细菌数量较低。在出现弥漫性病变的牛中,受影响的基因指向过度活跃的免疫通路,例如 Th1/Th2 细胞分化和抗原呈递,以及胆汁运输和药物反应路径。在这里,BOLA 家族的改变可能促成强烈、偶尔自损的炎性反应,与许多人类自身免疫和炎症性疾病中观察到的模式相呼应。
为培育更具韧性的牛群提供线索
除了阐明不同遗传变异如何塑造对 MAP 的免疫反应外,该研究还将这些风险变异与已知的牛基因组中与健康性状相关的区域联系起来,包括对分枝杆菌肠病和其他感染的易感性。尽管这些结果仍需在更大规模的牛群中验证,且尚不能作为单独的诊断标记使用,但它们提供了一个有前景的候选变异与基因目录。简单来说,这项工作表明一些牛携带有助于默默控制感染的基因版本,而另一些则携带促使失控炎症和严重疾病的基因版本。未来,这类信息可支持选择性育种和基因检测,将牛群朝着更高的天然抗性方向转变,从而减少经济损失并降低对密集疾病控制措施的依赖。
引用: Badia-Bringué, G., Lam, S., Cánovas, Á. et al. Whole-transcriptome identification of deleterious variants in candidate genes linked to bovine paratuberculosis. Sci Rep 16, 6243 (2026). https://doi.org/10.1038/s41598-026-37675-9
关键词: 牛分枝杆菌肠病, 约翰氏病遗传学, 乳牛免疫, RNA 测序, 抗病育种