Clear Sky Science · zh
APOL1 血浆膜库抗拒快速蛋白降解
为什么一种肾脏蛋白的“消失行为”很重要
在近代非洲血统人群中,严重肾脏疾病的很大一部分已被追溯到单一基因 APOL1 的两个变体。然而,科学家仍难以解释该基因如何在不伤害大多数携带者的情况下损害肾细胞。本研究提出了一个看似简单但意义重大的问题:一旦 APOL1 蛋白在细胞内合成,它会存在多久,哪里最稳定?答案揭示了一个意想不到的二分特性——APOL1 在细胞内部迅速被破坏,但嵌入细胞外表面时却异常稳定,这一线索可能指引未来的治疗方向。
具有双重影响的风险基因
APOL1 基因有助于保护人类免受某些寄生虫的侵害,这一进化优势可能解释了其风险变体(称为 G1 和 G2)在非洲人群中普遍存在。不幸的是,遗传到两份这些变体的人面对被归类为 APOL1 介导肾病的显著升高风险。早期研究表明,当 APOL1 水平上升——通常是对炎症的反应时——蛋白可能变得有毒,尤其是在称为足细胞的脆弱肾过滤细胞中。但大多数研究侧重于是什么激活了 APOL1。相比之下,关于细胞如何将其关闭,例如通过分解该蛋白,知之甚少。
追踪细胞内易损的蛋白
为探索 APOL1 的稳定性,研究人员构建了产生荧光标记 APOL1 及其最接近的同族 APOL2 的人源细胞系。这使他们能够通过免疫印迹、显微镜和流式细胞仪观察在不同条件下每种蛋白的积累或消失情况。他们抑制了细胞的主要蛋白降解装置——蛋白酶体,并另行抑制新蛋白的合成。当蛋白酶体被抑制时,APOL1 水平迅速上升,表明其通常被快速降解。当新蛋白合成被停止时,APOL1 水平迅速下降。形成鲜明对比的是,APOL2 在任一处理下几乎没有变化,显示其为更稳定的蛋白。重要的是,APOL1 的高周转率在正常版本(G0)和肾脏风险版本(G1 与 G2)中相同,并且在几种天然存在、在膜中定位方式不同的 APOL1 形式中都成立。
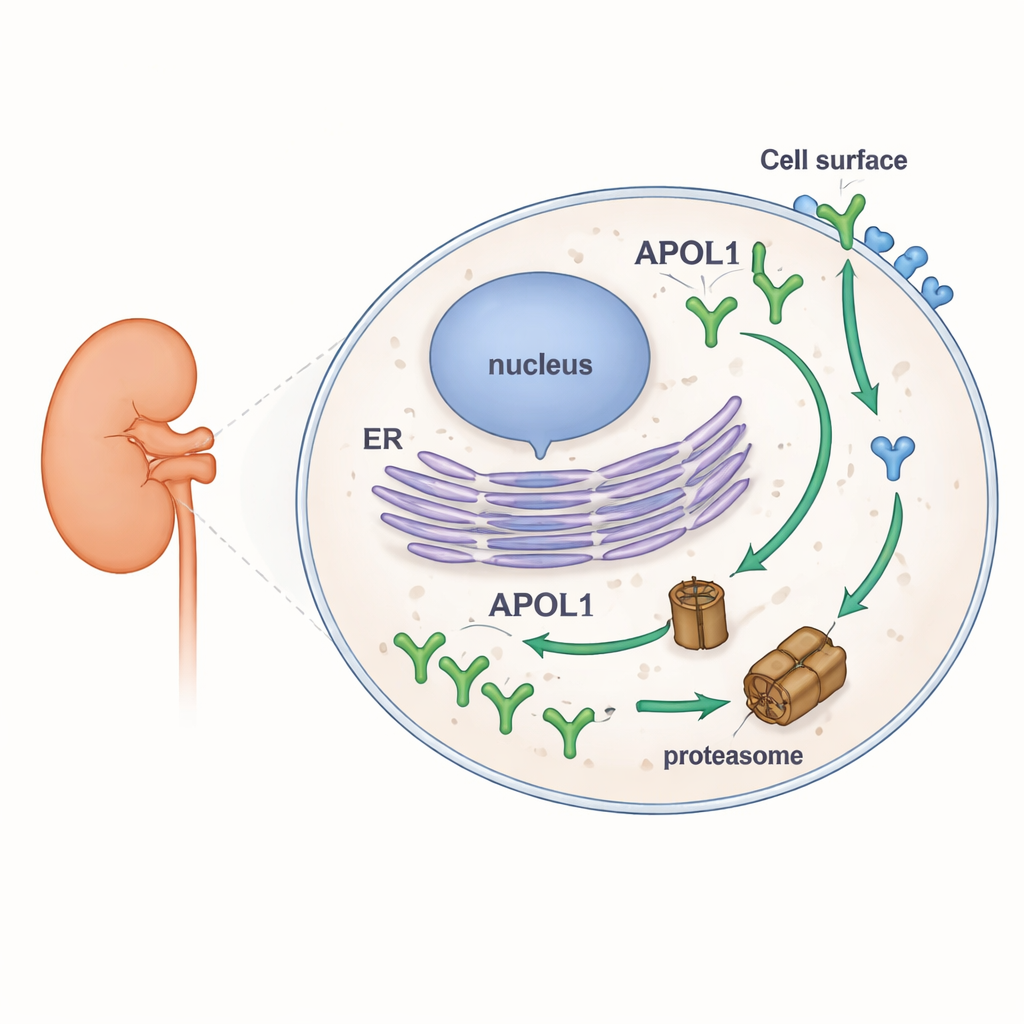
序列线索与两种“社区”的故事
深入蛋白结构,研究组使用计算工具扫描 APOL1 与 APOL2 中的松散无序片段,称为本征无序区。这类区域常作为蛋白酶体的“吃我”信号。他们在 APOL1 中鉴定出两个强候选区域,而 APOL2 中基本不存在这些区域。为测试 APOL1 独特的前端是否促成其脆弱性,他们构建了杂交体:一个缺失前 59 个氨基酸的截短 APOL1,以及一个携带该 APOL1 片段的 APOL2 嵌合体。将 APOL1 的 N 端片段加入 APOL2 后,APOL2 降解更快;而截短的 APOL1 仍然不稳定,提示 APOL1 中不止一处区域促使快速分解。总体而言,这些结果将 APOL1 异常的柔性片段与其快速周转联系起来,但并未将此行为专门归因于致病变体。
细胞表面的顽固蛋白
最引人注目的发现出现在作者区分细胞内 APOL1 与细胞表面 APOL1 时。使用只识别暴露于细胞外的 APOL1 片段的抗体,他们将表面水平与总量分别测量。细胞内的 APOL1 行为符合预期:当蛋白酶体被阻断时积累,当新合成被停止时迅速消失。然而,表面 APOL1 在任一条件下几乎没有变化。一旦 APOL1 分子到达质膜,它们就表现出高度抗拒快速降解。此外,尽管风险变体产生的 APOL1 总量低于正常版本,但它们的表面水平相似。这提示风险型与正常型 APOL1 在细胞内的清除速率相当,但被认为形成离子通道并驱动毒性的膜嵌入库在所有变体中都能得以保存。
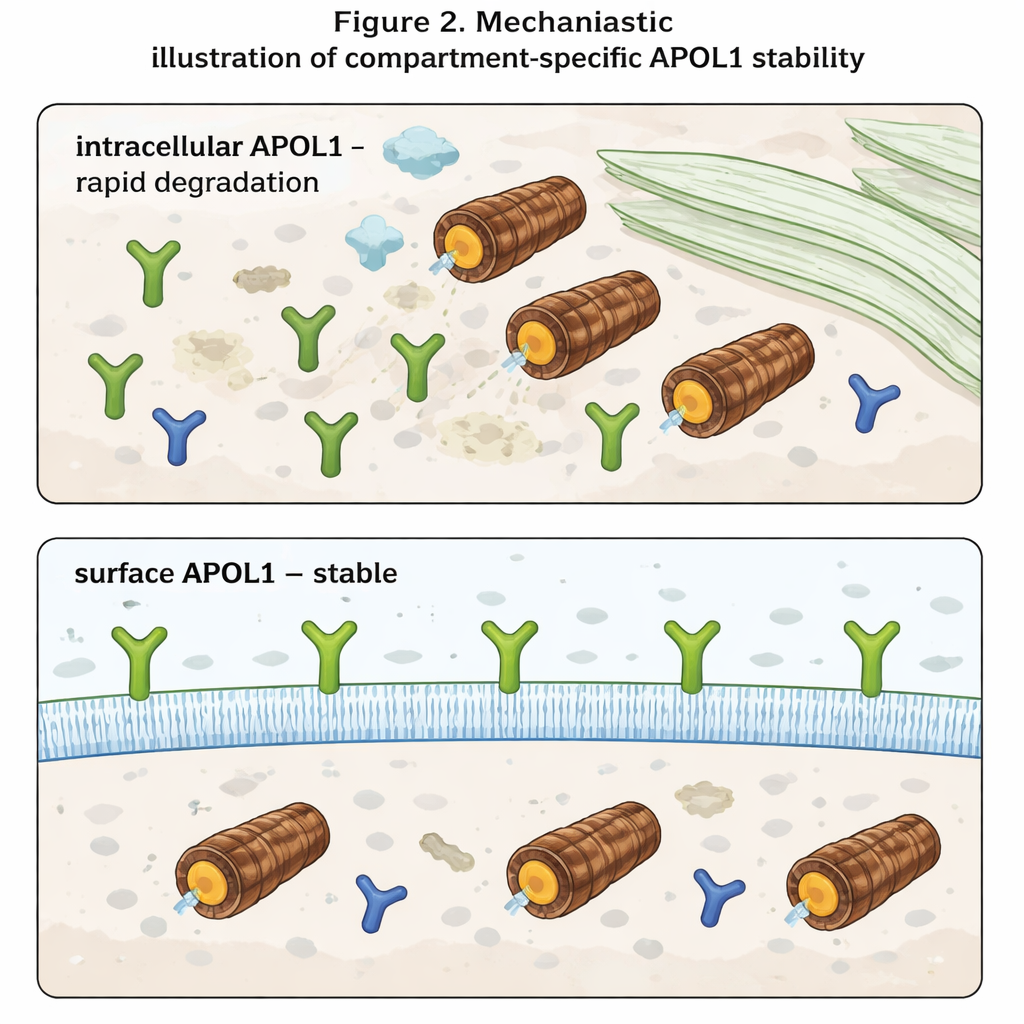
这对未来治疗的意义
对非专业读者而言,核心信息是 APOL1 的行为与其所在位置密切相关。在细胞内,它是短命蛋白,会被快速识别并降解;在细胞表面,它则变得长寿且相对受保护,即便细胞的降解机制发生改变。由于疾病似乎在 APOL1 于表面形成通道并扰乱钠、钾等离子平衡时产生,治疗策略或许应更关注到达并在质膜中停留的 APOL1 量,而非仅仅降低总量。减少 APOL1 运送到细胞表面的策略或选择性使表面库不稳定,理论上可以在不完全阻断该基因有益免疫功能的前提下,减轻肾损伤。
引用: Höffken, V., Alvermann, L., Niggemeier, D. et al. APOL1 plasma membrane pools resist rapid protein degradation. Sci Rep 16, 6718 (2026). https://doi.org/10.1038/s41598-026-37647-z
关键词: APOL1, 肾脏疾病, 蛋白质降解, 质膜, 蛋白酶体