Clear Sky Science · zh
体外表征人类组蛋白去乙酰化酶5催化结构域
为什么我们DNA包装上的微小开关很重要
在每个细胞内,我们的DNA缠绕在类似轴线的蛋白质上,帮助将米级的遗传物质塞入微观空间。基因是否被开启通常取决于这些轴线蛋白上的小型化学标记。本研究聚焦于一种名为HDAC5的蛋白“开关”,它与心脏病、脑部疾病、癌症等多种疾病相关。通过在分子水平上理解HDAC5的工作机制,研究人员希望为更精确、副作用更少的药物开发铺平道路。
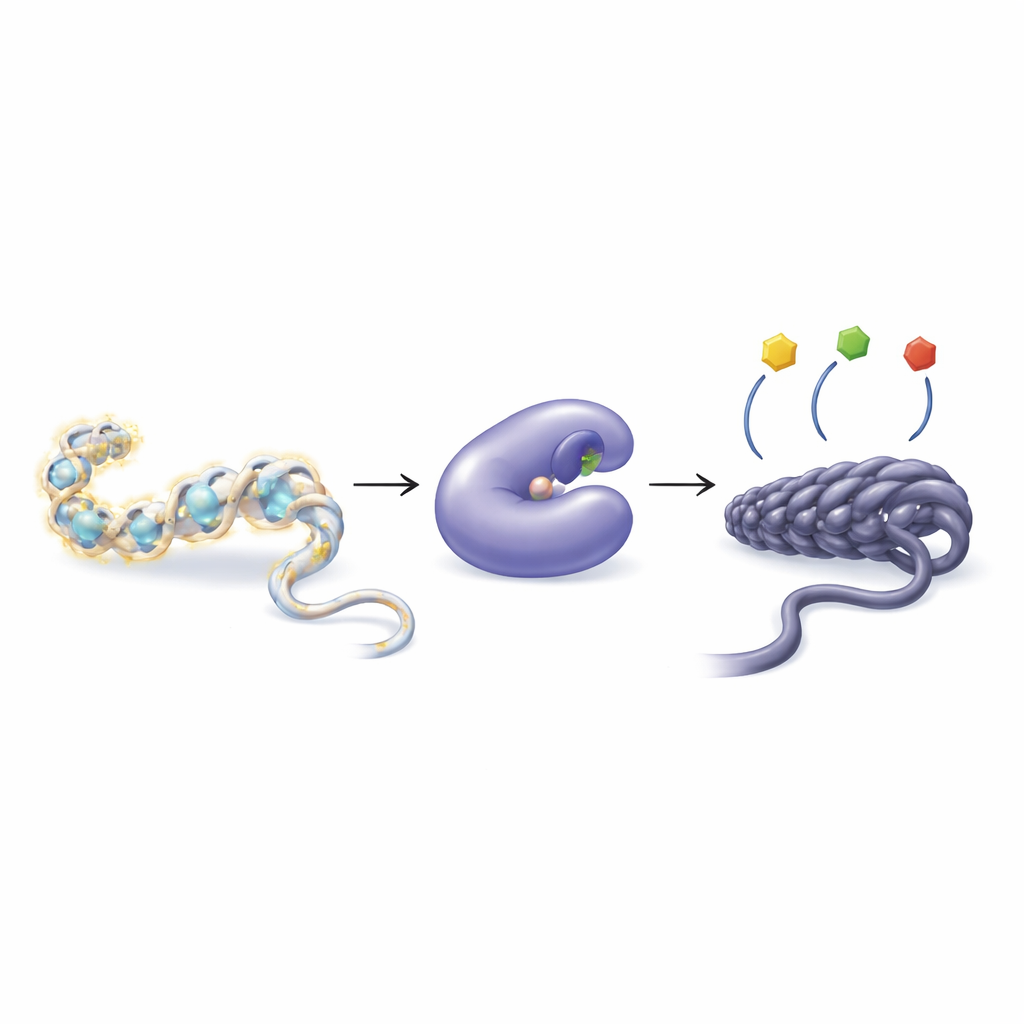
细胞如何用微小化学标记调节基因
我们的DNA不是自由漂浮的,而是缠绕在称为组蛋白的蛋白质上,形成称为染色质的结构。细胞可以在组蛋白尾部添加或去除小的化学基团,例如乙酰基,从而使染色质松散或紧密。较松散的包装通常有利于基因被读取;较紧密的包装则倾向于沉默基因。两类酶共同管理这一平衡:组蛋白乙酰转移酶添加乙酰基,而组蛋白去乙酰化酶(HDAC)则将其移除。当该平衡被打破时,可能导致包括癌症、心脏疾病、肌肉萎缩和免疫疾病在内的多种病症。
为何HDAC5是有前景但复杂的药物靶点
HDAC构成了一个庞大的相关酶家族,分为多个亚类。许多临床使用的药物会同时阻断多种HDAC,这可能抑制重要的正常功能并导致严重副作用。IIa类HDAC(包括HDAC5)特别引人注目,因为它们在大脑、心脏和骨骼肌等特定组织中富集,并与其他蛋白合作调控关键基因网络。HDAC5常充当桥梁,把活性很高的伴侣酶(如HDAC3)带到某些基因处,从而使染色质收缩并沉默那些基因。由于这些相对集中的作用,HDAC5被视为更具选择性的药物设计的有吸引力的目标,但过去缺乏详细的生化数据且其活性核心没有高分辨率结构,这使得基于结构的药物设计变得困难。
在试管中重建HDAC5
为了解决这一空白,研究人员仅在细菌中表达了人HDAC5的催化核心——执行化学反应的那一部分,进行了纯化,并确认该片段在溶液中形成稳定的单体蛋白。随后他们测试了在不同盐浓度和酸碱度下的活性。HDAC5在宽范围的盐浓度下保持稳健活性,并在弱碱性条件下达到峰值,这与许多细胞内环境相似。使用特殊的荧光底物,他们发现天然形式的HDAC5只识别一类常用于检测IIa类酶的底物。借鉴先前关于相关HDAC的工作,他们在一个关键位点将单个氨基酸(组氨酸)替换为酪氨酸。令人惊讶的是,这一微小改变使得突变体HDAC5能有效处理两种类型的检测试剂,揭示了活性位点中单个残基如何决定酶的化学偏好。
测试并比较两种新药候选物
团队接着检查了两种实验性HDAC5抑制分子,称为NT160和FFK24。这些化合物使用了一种更新的锌结合基团,避免了旧有羟肟酸类药物的一些毒性和选择性差的问题。通过在严控反应条件下测量每种抑制剂对HDAC5的抑制,作者确定了处于纳摩尔范围的极低抑制常数,说明两种化合物都能紧密结合该酶。NT160始终比FFK24结合力强约十倍。为理解原因,研究人员使用基于AlphaFold预测的HDAC5核心结构进行计算对接。两种抑制剂都有一个共同的头部深入活性袋并接触金属离子,但NT160的尾部与口袋中特定氨基酸形成了额外的稳定接触。这些额外相互作用很可能解释了其更高的效力。
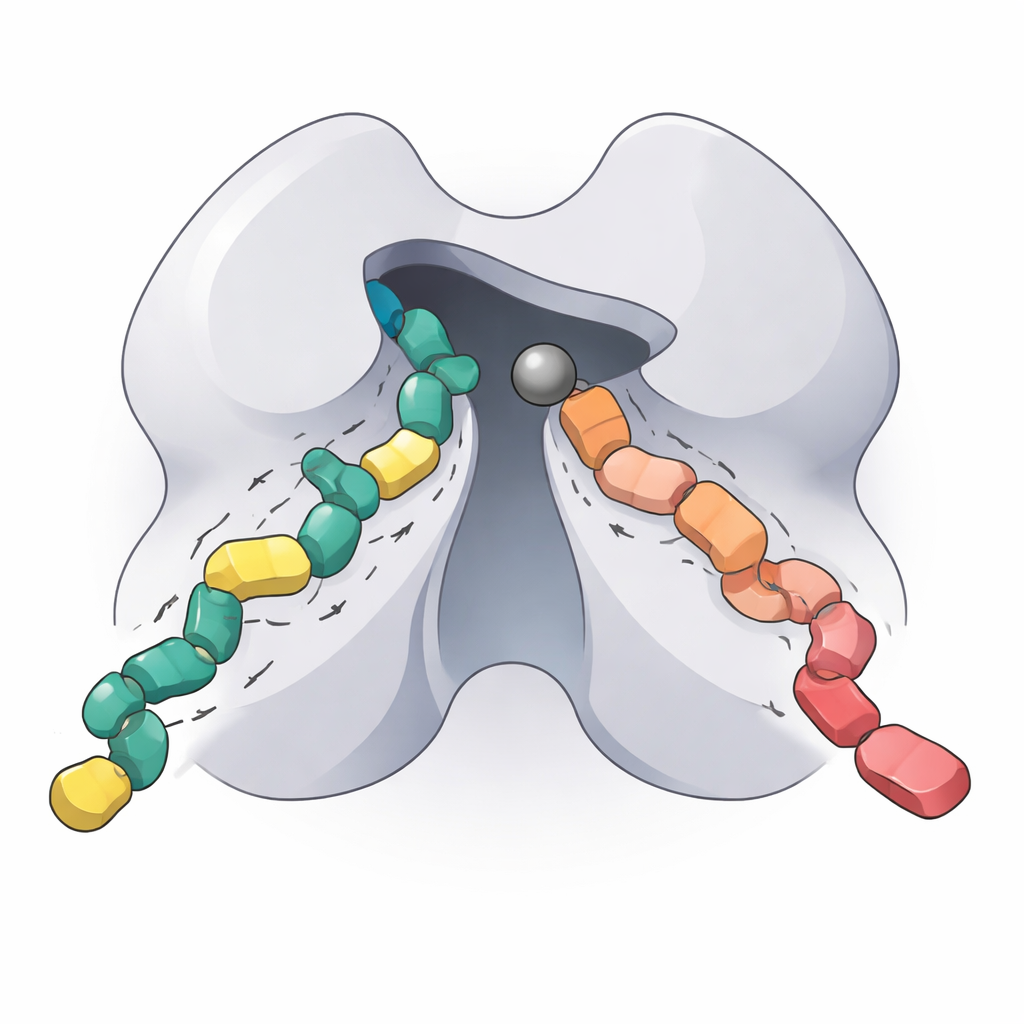
这对未来靶向疗法意味着什么
通过重建HDAC5的工作核心、绘制其最佳工作条件、解析单个氨基酸变化如何改变其行为,并量化两种新一代抑制剂的结合特性,本研究提供了对这一重要但此前表征不足的酶的详细生化“指纹”。对于非专业读者,关键结论是HDAC5有助于控制某些基因的开启或关闭,精确调节这一开关可能对治疗心脏病、神经退行性疾病、癌症和免疫疾病具有价值。这里提供的新见解和工具应能帮助研究者设计在所需组织发挥作用、同时将体内其他部位的副作用降至最低的HDAC5及IIa类选择性药物。
引用: Mammen, C., Hornung, F.M., Anzenhofer, C. et al. In vitro characterization of the catalytic domain of human histone deacetylase 5. Sci Rep 16, 7935 (2026). https://doi.org/10.1038/s41598-026-37633-5
关键词: 组蛋白去乙酰化酶5, 表观遗传调控, HDAC 抑制剂, 靶向癌症疗法, 染色质结构