Clear Sky Science · zh
H19通过削弱miR-29c-5p对ATF2/ECM1的抑制作用,增强胰腺癌的增殖与侵袭
为何这种“隐秘”细胞信息很重要
胰腺癌是死亡率极高的癌症之一,部分原因在于常常晚期才被发现且对现有治疗耐受性强。这项研究超越了编码蛋白质的基因,转而关注那些“沉默”的遗传信息——长链和小型RNA分子——它们帮助胰腺肿瘤生长、转移并逃避免疫或治疗。通过揭示一种名为H19的长链RNA与其微小搭档miR-29c-5p如何协同重塑肿瘤周围环境,作者勾勒出一条新的分子回路,这可能为更早的诊断和更精准的治疗提供线索。
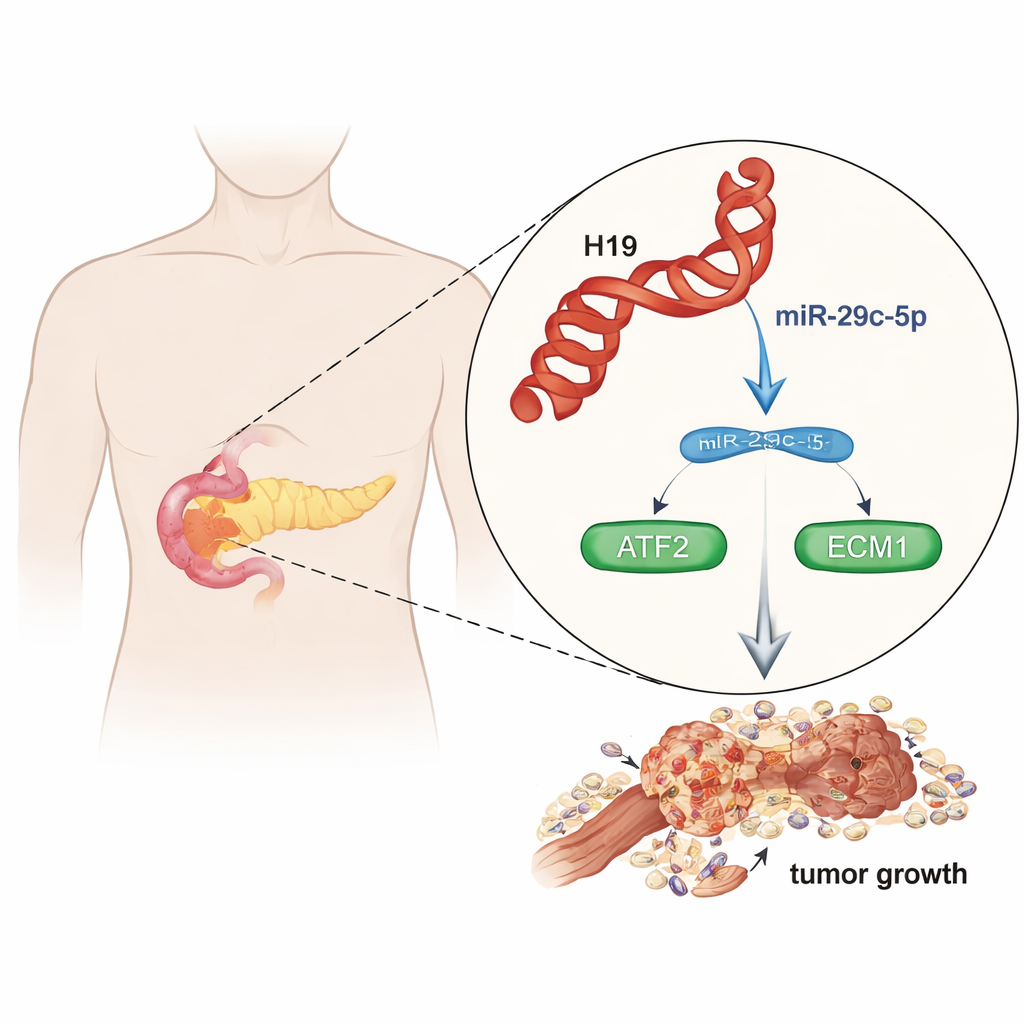
一个危险且选择有限的癌症
胰腺导管腺癌(PDAC)五年生存率低于10%,主要因为其早期转移且对化疗反应差。研究者越来越认识到,非编码RNA——不翻译成蛋白质的遗传信息——是控制肿瘤行为的重要开关。本研究通过分析大型公共数据库与患者样本,发现一种长链非编码RNA H19在胰腺肿瘤中持续升高,相较正常胰腺组织表达更高。肿瘤H19水平较高的患者存活更短,提示H19并非旁观者,而是驱动侵袭性疾病的因子之一。
H19如何在肿瘤细胞内部扭转平衡
在细胞内,H19主要位于水样的细胞质中,因此更倾向于与其他RNA相互作用,而不是直接修改DNA。作者发现H19像一个分子海绵:它结合并俘获一种名为miR-29c-5p的小型RNA,而该小RNA本可抑制肿瘤生长并发挥监督作用。当H19水平升高时,可用的游离miR-29c-5p减少。细胞与体外实验显示,增加H19使胰腺癌细胞增殖加快并更容易穿过人工膜,抑制H19则减缓其生长与侵袭。相反,恢复miR-29c-5p可逆转许多这些有害效应,表明两者之间存在拉锯战。
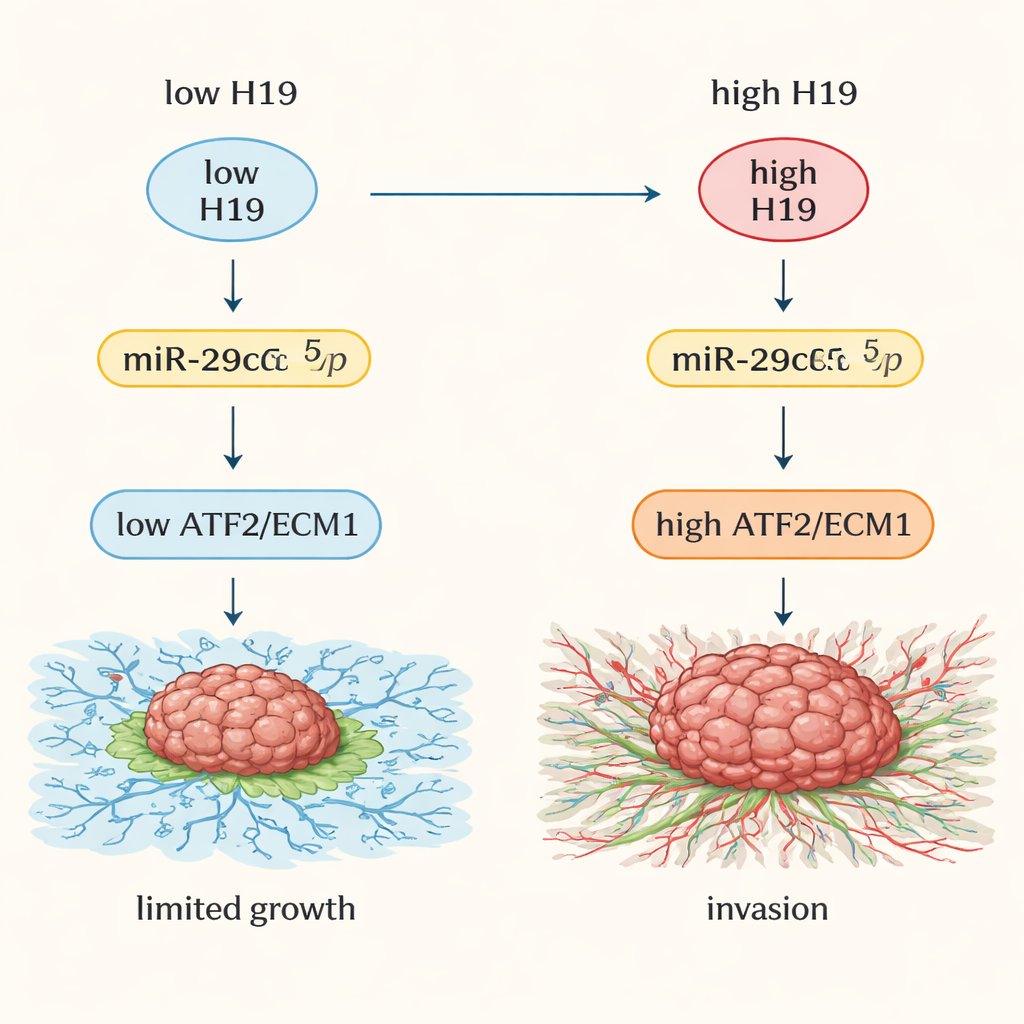
下游靶点:解除对肿瘤生长的制动
小RNA miR-29c-5p通常抑制两种重要蛋白:核内的基因调控因子ATF2,以及塑造细胞外基质的蛋白ECM1。当miR-29c-5p被H19“吸走”时,ATF2和ECM1的水平上升。在肿瘤样本和公共癌症数据库中,ATF2与ECM1在胰腺癌中的表达明显高于正常组织。两者的高表达与疾病更晚期和更差的生存相关。在细胞与小鼠实验中,降低H19或增加miR-29c-5p会减少ATF2和ECM1、缩小肿瘤并削弱其侵袭行为。证据指向一条级联反应:H19结合miR-29c-5p,释放ATF2,继而上调ECM1,促使组织变得僵硬和纤维化,利于肿瘤扩散。
从机制到潜在的标志物与疗法
除了描绘这条信号链外,研究者还评估这些分子是否能帮助临床诊断或分型胰腺癌。利用患者数据,他们发现ECM1和ATF2的水平能较高准确度地区分癌组织与正常胰腺,在某些分析中表现优于常用的血液标志物CA19-9。肿瘤ECM1表达较低的患者往往生存期更长,提示其可能作为预示侵袭性疾病的信号。尽管该医院的临床样本量有限,但在独立数据库与动物实验中观察到的一致性增强了该轴在PDAC生物学中关键作用的论据。
对患者与未来研究的意义
通俗地说,这项研究表明,一种长链“沉默”RNA H19通过中和保护性小RNA miR-29c-5p并释放两种促生长蛋白ATF2与ECM1,帮助胰腺肿瘤生长与侵袭。这个四元链条——H19/miR-29c-5p/ATF2/ECM1——助力肿瘤改造其周围环境,使之成为支持性巢穴,并与更差的预后紧密相关。尽管需要更多、更大规模的临床研究,这项工作提示测量该通路的成分或可用于识别高危患者,而设计针对H19或ECM1的药物,或恢复miR-29c-5p活性的策略,未来或能为这一难治性癌症提供新的治疗选择。
引用: Rui, M., Xiuping, L., Yu, C. et al. H19 enhances pancreatic cancer proliferation and invasion by reducing miR-29c-5p’s inhibitory effects on ATF2/ECM1. Sci Rep 16, 7623 (2026). https://doi.org/10.1038/s41598-026-37632-6
关键词: 胰腺癌, 非编码RNA, H19, 肿瘤微环境, 生物标志物