Clear Sky Science · zh
强度依赖的 tACS 在皮质微电路中的相位锁定效应:一项计算研究
为何“轻柔”脑电刺激重要
科学家正在探索通过头皮施加极弱电流来微调大脑的自然节律,这种技术称为经颅交变电流刺激(tACS)。这些有节律的“脑电刺激”正在被尝试用于缓解抑郁、精神分裂症和帕金森病的症状,以及提升记忆和注意力。然而在人群中的实验结果喜忧参半:有时 tACS 有效,有时几乎没有作用。本研究提出了一个既简单又关键的问题:在单个神经元和微小局部回路的层面,当我们调高 tACS 强度时,究竟会发生什么?
计算机中的一小片皮层模型
作者没有直接在动物或人身上实验,而是构建了一个详细的计算机模型,模拟一小块类人的皮层。他们的虚拟回路包含五个经过精确重构的神经元,跨越皮层的浅层到深层。三类是高大、树状的锥体细胞,承担大部分兴奋性传递;另外两个是较小的抑制性中间神经元,帮助维持活动平衡。模型不仅捕捉了这些细胞的位置,还包含它们的分支形态、电学特性,以及它们之间兴奋性和抑制性连接的网络。研究团队随后用随机时序的突触输入驱动该回路,以模拟大脑自身在 alpha(约 10 Hz)和 theta(约 5 Hz)频段的节律活动。 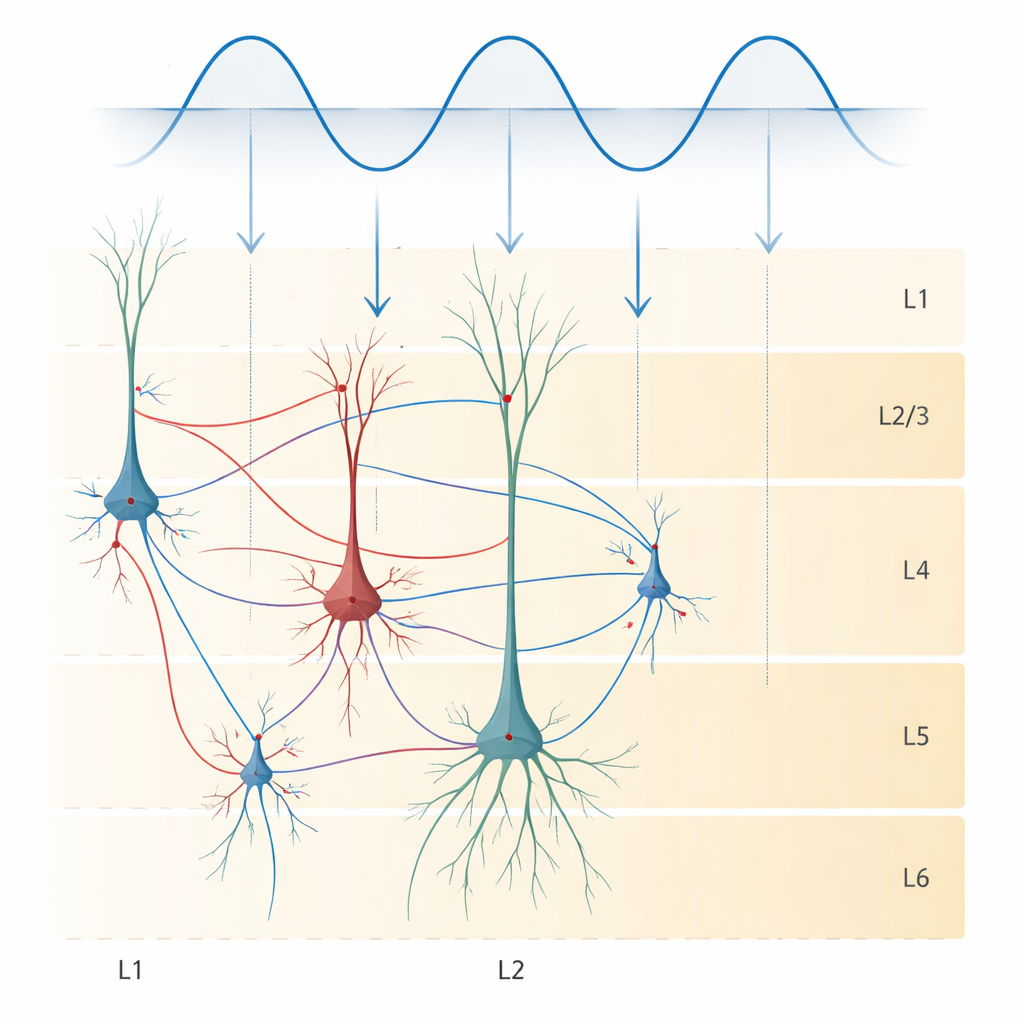
微弱电流改变时机,而非强度
接着,研究者施加了模拟的 tACS:一个以正在进行的脑节律相同频率振荡的弱且均匀的电场,强度从非常低到 2 毫安。他们同时监测“局部场电位”(作为电极记录的代理)和每个神经元的精确放电时序。结果出现了清晰的模式。即便刺激增强,神经元的总体发放率几乎没有变化——变化幅度低于约 1%。显著改变的,是神经元发放的时间。随着强度增加,脉冲越来越集中在刺激波形的一个优先相位附近,锥体细胞尤为明显。换言之,tACS 更像节拍器而非音量旋钮:悄然重塑活动的时序,而不是让神经元更大声地放电。
何时微弱刺激会先扰乱再同步
通过检查脉冲与 tACS 周期的对齐方式,研究者发现了一个“强度依赖”的故事。在非常低的强度下,当大脑自身节律与外加驱动不同步时,tACS 实际上可能会降低同步性,短暂地扰乱正在进行的模式。随着电流增大至临床常用水平(约 1–2 毫安),外部刺激开始占主导:脉冲更紧密地锁定在波形上升相,模型中衡量相位锁定的指标在锥体神经元上大致呈线性上升。这种先弱扰乱后强锁定的进程,有助于解释为何在某些设置下 tACS 会破坏不健康的节律,而在另一类设置下又能强化有益的节律。 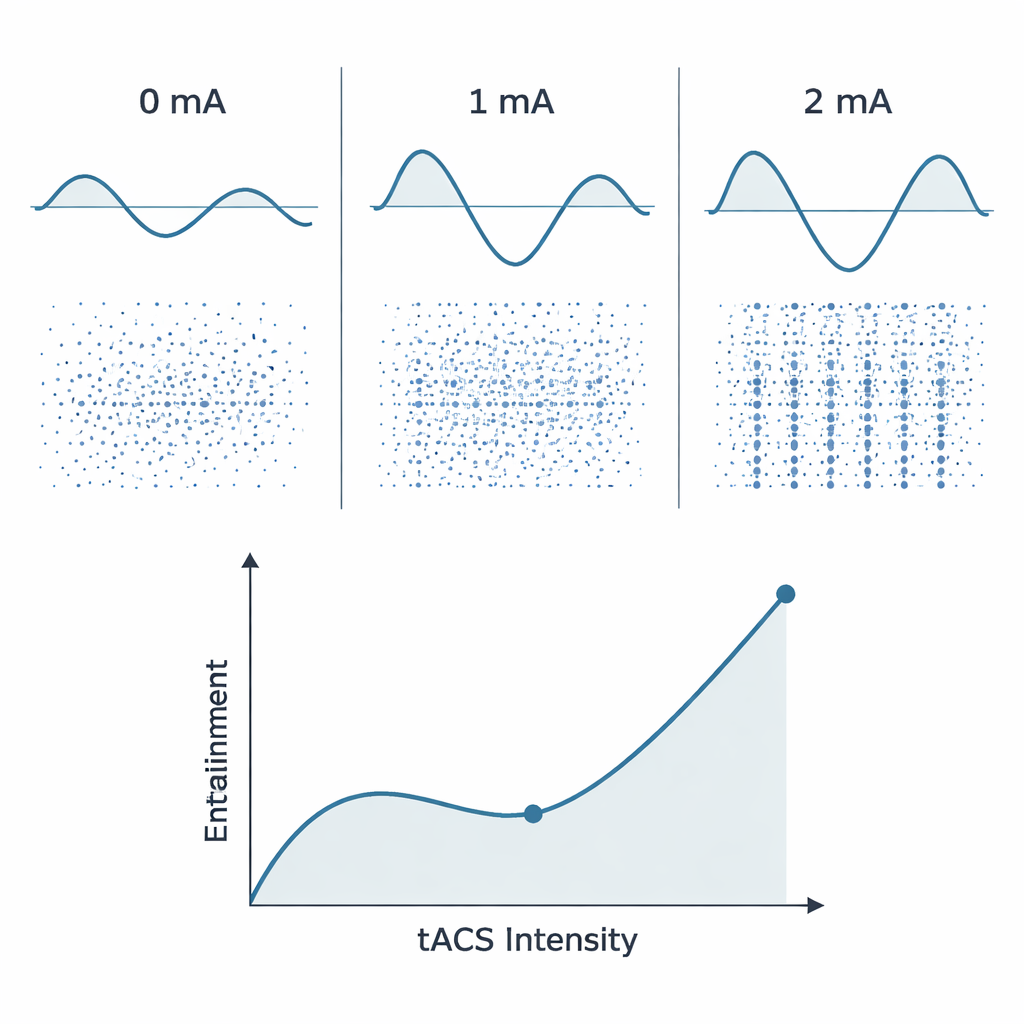
为何细胞形态与连接决定结果
并非所有神经元的反应都相同。具有长而垂直定向树突的锥体细胞对电场要比形态更紧凑的中间神经元敏感得多。随着强度增加,它们的放电时机与刺激相位整齐对齐,而中间神经元则更为散乱、锁相较弱。当研究者在模型中“切断”突触连接时,锥体细胞仍能相当好地被调相,但中间神经元几乎失去了相位锁定。再次引入连接后,这些抑制性细胞的相位锁定部分恢复,表明 tACS 作用它们主要是间接的——通过重塑送入它们的锥体细胞的活动。微电路中兴奋与抑制的平衡,以及已有的放电模式,和刺激本身一样重要。
对未来脑刺激的启示
对非专业读者和临床医生而言,结论是:tACS 的效应微妙且高度依赖细胞形态与网络语境。相同的电流能温和同步某一类神经元,却对另一类影响甚微,而微弱刺激既可能暂时去同步,也可能在更高强度下强力锁定节律。由于锥体神经元尤为敏感,其分支结构或许应成为规划电极放置、选择刺激强度与频率时的重要考量。尽管这项工作仅限于小规模模型和短时程模拟,但它提示,要在患者中优化 tACS,需将刺激调校到与大脑现有节律和微电路结构相匹配,目标可以是削弱有害的同步或强化支持健康认知的时序模式。
引用: Park, K., Chung, H., Seo, H. et al. Intensity-dependent tACS entrainment effects in a cortical microcircuit: a computational study. Sci Rep 16, 6825 (2026). https://doi.org/10.1038/s41598-026-37594-9
关键词: 经颅交变电流刺激, 神经相位锁定, 皮质微电路, 锥体神经元, 脑振荡