Clear Sky Science · zh
在CRISPR/Cas9编辑EGF结合域后EGFR活性变化
为何重新接线癌症信号至关重要
宫颈癌常依赖一种强大的生长开关——表皮生长因子受体(EGFR)。许多肿瘤细胞表面有大量此类受体,然而旨在封锁它们的药物只帮助了部分患者。本研究提出了一个根本性且具有重要治疗意义的问题:如果去掉EGFR抓取其首选生长信号表皮生长因子(EGF)的能力,但不移除受体本身,会发生什么?
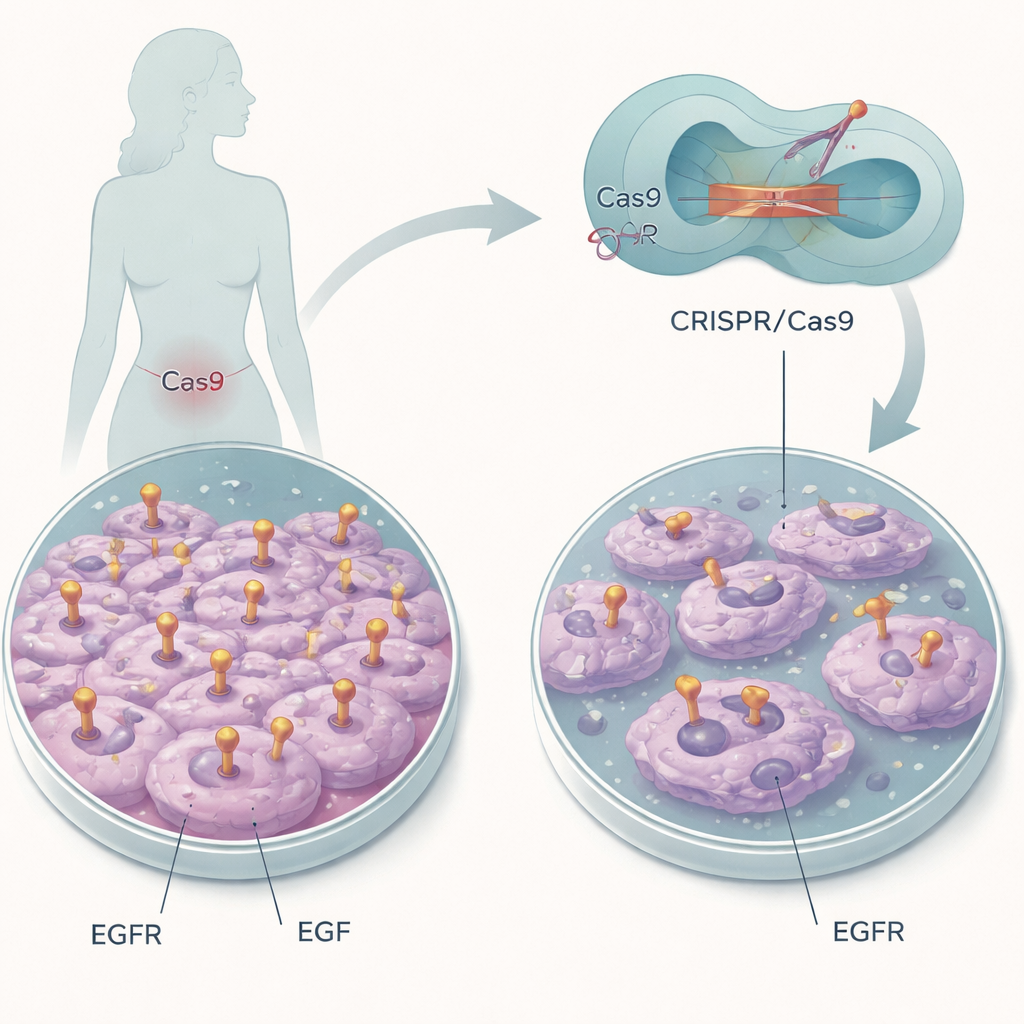
关闭分子“开启开关”
研究人员聚焦于一株携带大量正常EGFR的宫颈癌细胞系。他们没有拆除基因,而是将CRISPR/Cas9基因组编辑作为分子手术刀,仅改变EGFR EGF结合口袋中的少数氨基酸。两个特定位置,称为L14和Y45,帮助EGF与受体对接。通过将这些构件替换为其他氨基酸,研究组旨在保持EGFR存在但对EGF失明,从而能够独立分离这一单一相互作用在癌细胞行为中的作用。
构建“定制”癌细胞系
在第一步中,团队在细胞中使用瞬时表达正常或突变EGFR的质粒测试这些突变。带荧光标记的EGF显示,所有突变体结合配体的能力远低于正常受体,尤其是在L14和Y45同时改变时。随后研究人员使用CRISPR/Cas9将这些改变直接引入癌细胞基因组,生成了多个新克隆。有些携带单一突变,有些在一份EGFR拷贝上携带双突变而另一份拷贝则为失活改变。对所得蛋白构象的计算机建模显示,这些变化足以扭曲结合位点,削弱或消除EGF的对接,这与结合测试结果一致。
受体改变位置但细胞仍然存活
详细成像显示,编辑后的受体在细胞内表现出截然不同的行为。在未编辑的癌细胞中,EGFR位于细胞表面,捕获EGF后向内转运,同时通过磷酸化被化学激活。在带有双突变的克隆中,EGF结合基本消失,EGFR不再出现在膜上;相反,少量残留的受体在细胞内部积累。即便仅有Y45的单一改变,也显著降低了结合并降低了整体EGFR水平。然而,尽管教科书式的EGF–EGFR信号通路遭到破坏,癌细胞仍能存活并在培养中继续生长,细胞周期模式仅出现温和改变。
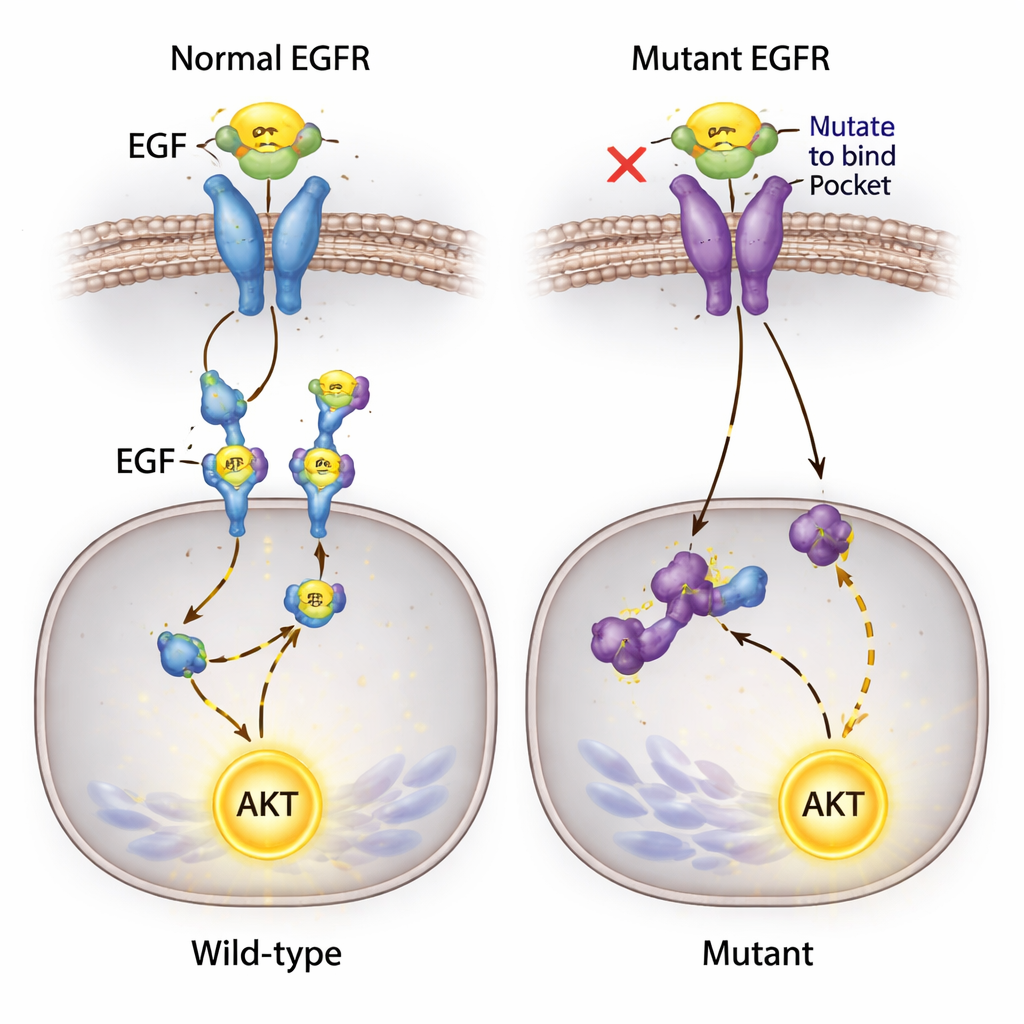
一个出乎意料却不肯停止的信号
最令人惊讶的发现之一涉及AKT——一种促进细胞存活的关键蛋白,通常在EGFR下游被激活。研究人员原以为阻断EGF–EGFR结合会让这一通路沉默。相反,当他们向培养基添加EGF时,AKT在所有细胞系中都被强烈激活——即便是在EGF已无法结合EGFR且受体磷酸化无法检测到的细胞中。鉴于这些细胞携带另一条信号基因PIK3CA的已知突变,团队怀疑可能存在替代途径使EGF能够激活AKT,或通过其他表面蛋白或背景突变绕过被编辑的EGFR。
隐藏的基因变化与未来疗法
为了确定CRISPR没有引起大范围的非目标编辑,科学家对新细胞系做了全基因组测序。他们确认了所需的EGFR突变存在,并未发现CRISPR引导RNA预测的脱靶切割证据。然而,他们确实检测到基因组中散布的许多自发突变,其中一些可能影响细胞行为。这强调出即便CRISPR命中目标地址,癌细胞固有的不稳定DNA也会复杂化我们对实验结果的解读以及精确基因疗法的设计。
这对患者意味着什么
对非专业读者来说,核心结论是:仅仅阻断EGF与EGFR之间的“握手”——即便是在原子水平上非常精确地阻断——并不必然阻止癌细胞接收“生长与存活”的指令。该研究表明,癌细胞可以将像AKT激活这样的关键信号绕开被阻断的受体进行重路由,而且必须在这种不稳定的基因组背景下仔细评估CRISPR编辑本身。这些工程化的细胞系现在为在实验室中寻找维持EGFR依赖性肿瘤的备用通路提供了强有力的模型,相关信息最终可能促成同时针对EGFR及其隐藏同谋的联合治疗策略。
引用: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
关键词: EGFR, 宫颈癌, CRISPR, EGF信号, AKT通路