Clear Sky Science · zh
拷贝数扩增驱动 IFI30 过表达并协调免疫激活,揭示胃腺癌中新型诊断与治疗靶点
为何胃内一种蛋白很重要
胃癌是全球致死性最高的癌症之一,这在很大程度上源于它常常被晚期发现且难以治疗。本研究聚焦于一种鲜为人知的蛋白 IFI30,它存在于帮助免疫系统识别威胁的细胞中。通过追踪 IFI30 在胃肿瘤中的改变及其如何塑造机体防御反应,研究者提出它有望成为用于更早诊断和选择更有效个体化治疗的有力工具。
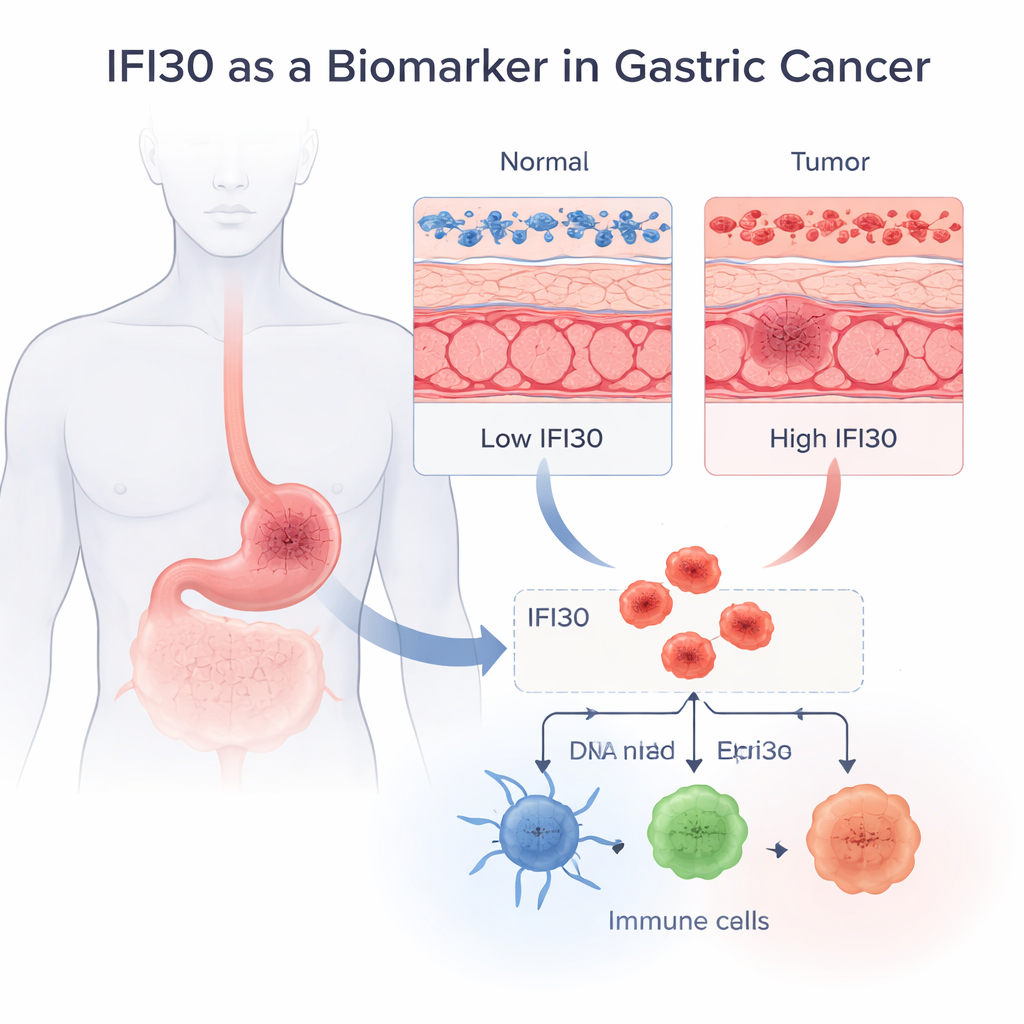
胃肿瘤中的隐匿信号
研究团队首先提出一个基础问题:IFI30 在健康与癌变胃组织中的表达是否不同?利用整合数千个样本的公开大数据集,他们发现 IFI30 在胃腺癌——最常见的胃癌类型——中的表达持续显著高于正常胃黏膜。这一结论在多个独立患者群体以及 RNA 和蛋白水平上均成立。当作者检验 IFI30 单独用于区分肿瘤和健康组织的效果时,其诊断性能令人瞩目:AUC 为 0.92,对于单一标志物而言属于优秀水平。显微图像还将 IFI30 定位于细胞内部的回收系统(即抗原处理用于免疫识别的场所)。
驱动 IFI30 上调的 DNA 改变
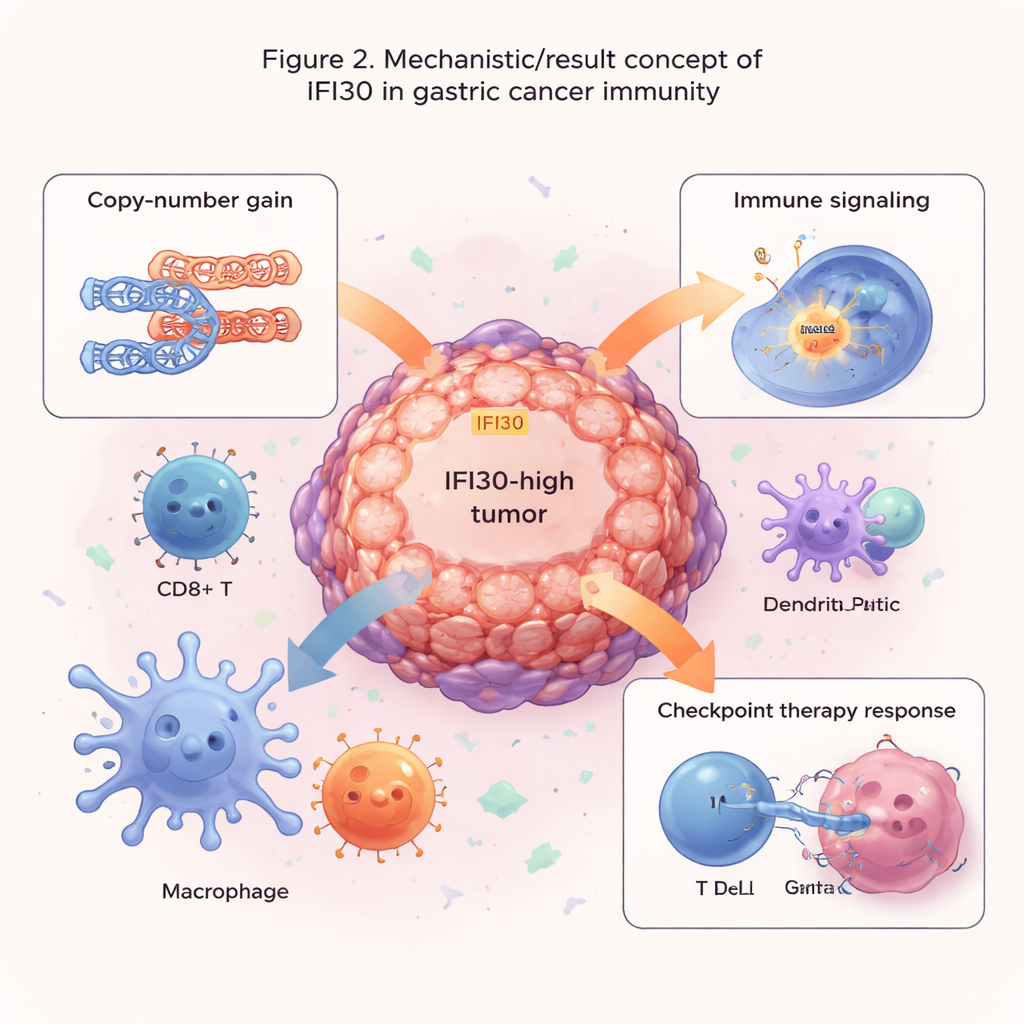
接着,研究者探究了为何 IFI30 在这些肿瘤中显著升高。在扫描癌症基因组(来自癌症基因图谱)时,他们发现 IFI30 基因的拷贝数增加——称为拷贝数扩增——是其过表达的主要驱动因素。具有 IFI30 扩增的肿瘤往往显示更强的整体基因组不稳定性,并常伴随已知的癌症突变,如 TP53 和 PIK3CA。随着 IFI30 拷贝数的升高,其 RNA 水平也随之上升,暗示结构性 DNA 改变与该蛋白产量提高之间存在直接联系。这表明 IFI30 并非被动旁观者,而是更大范围侵袭性肿瘤生物学模式的一部分。
肿瘤周围的免疫对话
鉴于 IFI30 参与处理呈递给 T 细胞的“通缉令”样抗原,团队进一步探索其在肿瘤微环境中的确切位置。单细胞测序显示 IFI30 在树突状细胞、巨噬细胞和 CD8 T 细胞中特别富集——这些细胞是启动和维持抗肿瘤免疫的关键角色。网络分析揭示 IFI30 丰富的免疫细胞与周围肿瘤细胞和基质细胞之间存在密集的通信。高 IFI30 的肿瘤表现出与抗原呈递、炎症信号和吸引、组织免疫细胞的通讯分子相关的强烈通路激活。同时,这些肿瘤也显示出侵袭和应激的特征,如细胞周期加速、组织重塑和低氧适应,突显出 IFI30 在肿瘤内攻守交汇处的角色。
为用药选择与免疫治疗提供线索
作者随后探讨 IFI30 是否能帮助预测肿瘤对治疗的反应。将 IFI30 水平与大型药物反应数据库配对分析后,他们发现 IFI30 高表达的肿瘤往往对某些靶向细胞分裂或常见生长通路(MAPK)的药物具有抵抗性,但对阻断 EGFR 和 PI3K/AKT 信号通路的药物似乎更为敏感。值得注意的是,IFI30 水平与 PD-L1(T 细胞主要的制动因子,当前检查点抑制剂的靶点)紧密相关。在多项免疫治疗研究中,肿瘤中 IFI30 表达较高的患者比低表达者更可能对检查点阻断产生反应。基于 IFI30 的评分优于肿瘤突变负荷和单独 PD-L1 等既有指标,且在微卫星不稳定性高(MSI-H)的肿瘤中尤为富集——该亚组已知更易对免疫治疗产生良好反应。
从实验室到潜在新靶点
为检验 IFI30 是标志物还是也助长癌症生长,团队在胃癌细胞系中使用遗传工具降低其表达。IFI30 被敲低后,癌细胞增殖放缓,表明其在维持肿瘤增殖中具有直接作用。综合来看,数据表明 IFI30 既是免疫活性的一种读出,也助力恶性行为。对患者而言,这意味着对 IFI30 的简单检测未来可能帮助医生更可靠地发现胃癌、预测谁可能从特定靶向药物或免疫治疗中受益,并可能指导开发直接或间接阻断 IFI30 促肿瘤作用的新疗法。
引用: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
关键词: 胃癌, IFI30, 生物标志物, 肿瘤免疫, 免疫治疗