Clear Sky Science · zh
一种分裂生物素连接酶方法揭示寡聚α‑突触核蛋白在聚集过程中相关的蛋白质
为什么大脑中蛋白质的凝聚重要
在帕金森病及相关疾病中,一种通常有益的脑蛋白α‑突触核蛋白可能会凝聚形成称为路易体的粘性沉积物。这些沉积物在症状出现前数十年就可出现,并且在尸检中是一项决定性特征,但我们仍然不清楚哪些其他蛋白质促使α‑突触核蛋白从无害状态转变为有害的聚集体。本研究使用一种巧妙的分子“邻近标签”来绘制α‑突触核蛋白从单体向小簇转变时周围哪些蛋白靠得近,提供了关于疾病如何起始以及哪些通路可能被用于减缓或预防的新线索。
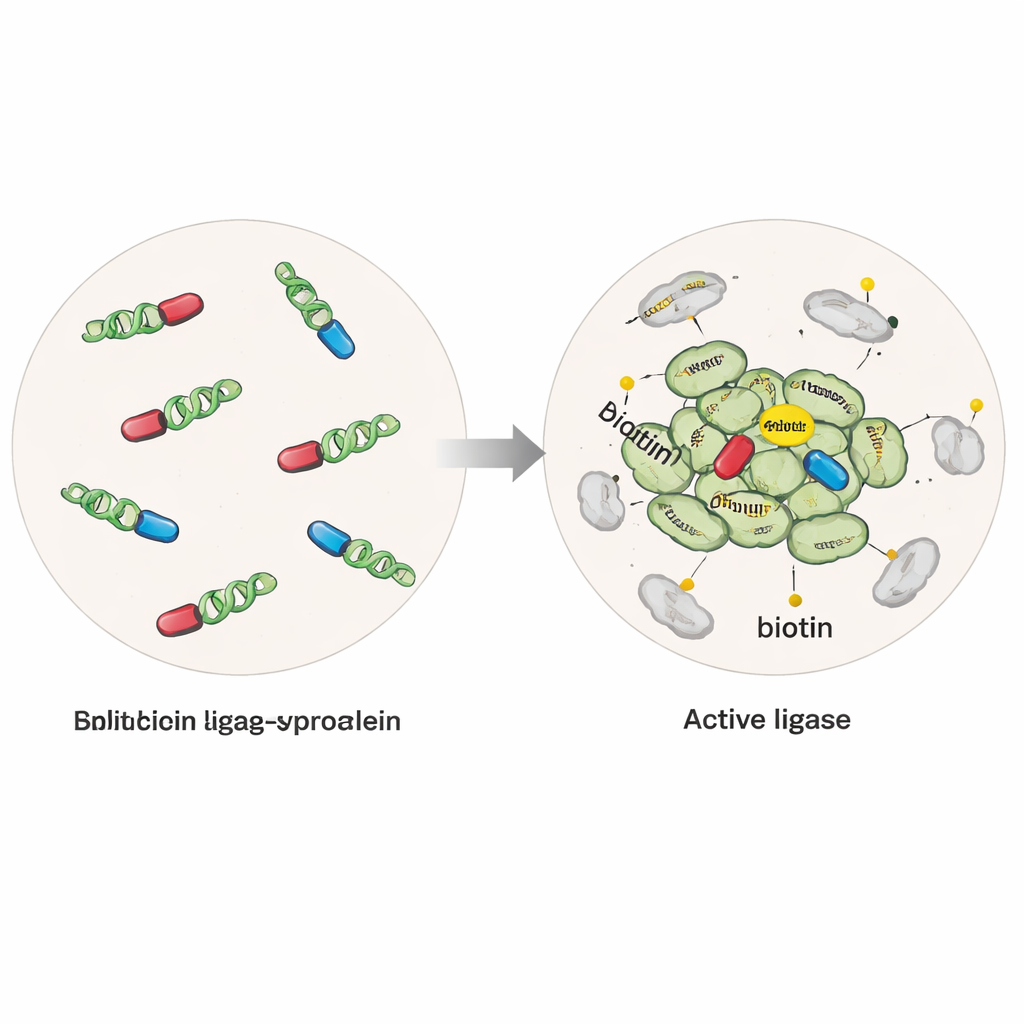
一种能点亮邻居的分子“标签”
研究者在人体细胞中构建了将α‑突触核蛋白与一种改造过的酶融合的系统,该酶能在数十亿分之一米范围内将小的生物素标签连接到任何蛋白上。在一种版本中,酶是完整并在α‑突触核蛋白存在时始终活跃,能捕获靠近单体以及聚集体的蛋白。在第二种更具选择性的“分裂”版本中,酶被切成两个不活跃的半片,分别连接到不同的α‑突触核蛋白分子上。只有当α‑突触核蛋白分子聚集成多聚体或寡聚体时,这两半才会重组为活性酶,从而专门在这些早期聚集体周围启动标记。通过向细胞中加入纯化的α‑突触核蛋白纤维,团队还能够诱导类似疾病的聚集并比较正常与病理状态。
构建附近蛋白的地图
在允许标记发生一段时间后,团队富集了所有带生物素标记的蛋白并用质谱鉴定这些蛋白——这是一种高精度称重并计数蛋白的技术。在所有条件下他们发现了1,277种不同蛋白,并在仔细过滤后缩小到581种可能真正靠近α‑突触核蛋白的蛋白。比较完整酶与分裂酶系统,他们能够区分主要与单体相关的蛋白与偏好多聚体的蛋白。他们还比较了有无加入纤维的细胞,以观察一旦触发聚集α‑突触核蛋白的局部蛋白环境如何变化。
被卷入聚集体的关键细胞通路
得到的相互作用组草图指向若干主要生物学主题。在正常条件下,多聚的α‑突触核蛋白靠近许多膜运输蛋白和蛋白修饰酶——与其被提议在帮助神经细胞管理突触囊泡和维持蛋白质质量控制方面的角色一致。若干添加磷酸基的酶,包括激酶PAK4、RIPK2和MAP4K4,在健康多聚体附近富集,但一旦形成聚集体便似乎失去接触,这提示这些关系的破坏可能促成疾病相关形式的出现。团队还检测到与类胰岛素生长因子信号有关的蛋白,支持胰岛素抵抗与帕金森病之间的临床关联,并发现聚集体招募了参与清除受损蛋白的成分,例如14‑3‑3伴侣家族和细胞降解通路中的特定组成部分。
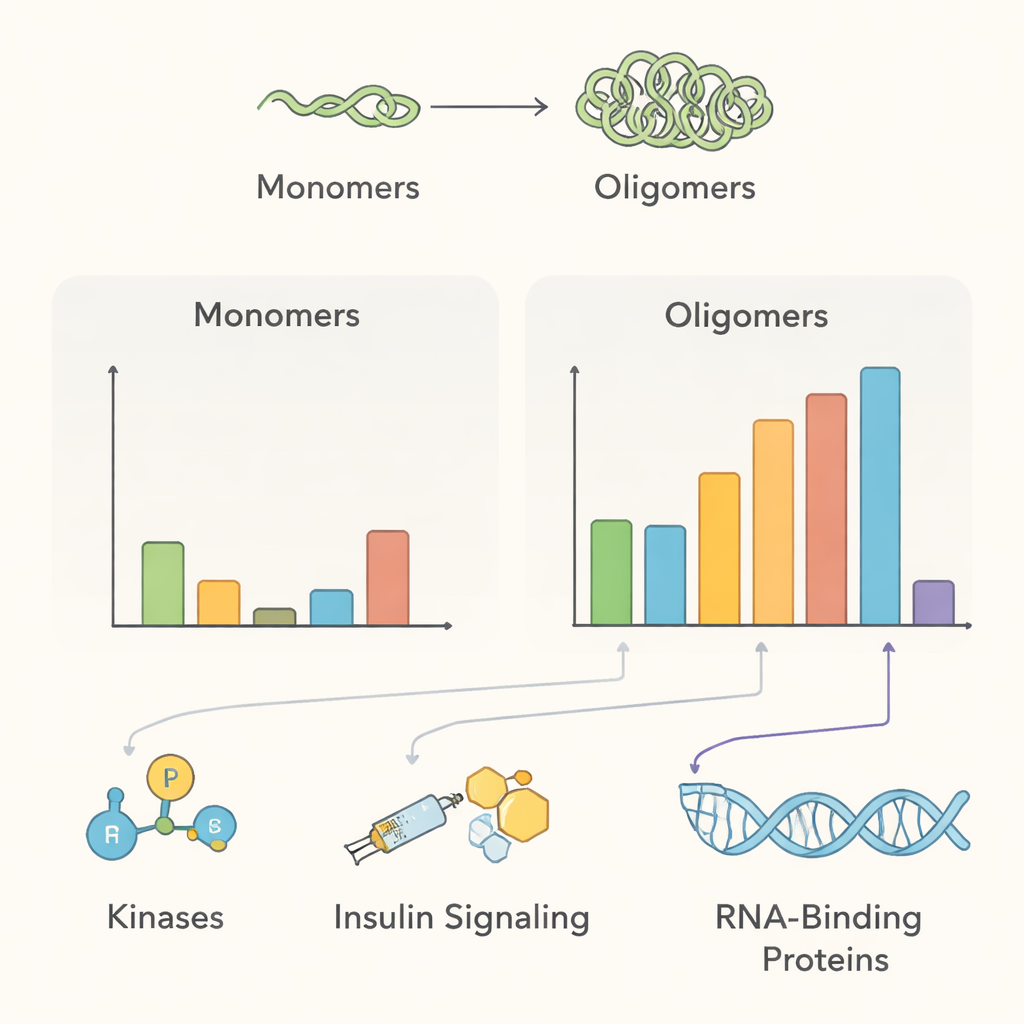
与其他脑疾病的意外联系
除了帕金森病外,数据还强调了与肌萎缩性侧索硬化(ALS)和额颞叶痴呆(FTD)之间令人意外的联系。一种名为FUS的RNA结合蛋白在这些疾病中会发生错误定位和聚集,在正常和诱导聚集的条件下都出现在多聚α‑突触核蛋白的近邻。其他与RNA相关的蛋白在α‑突触核蛋白聚集时也改变了它们的邻近关系。这些发现提出了这样一种可能性:小的α‑突触核蛋白组装体可能会将处理RNA的蛋白困在细胞内错误的部位,从而将路易体疾病的生物学与ALS和FTD联系起来,尽管直接的物理相互作用仍需进一步验证。
这对理解疾病意味着什么
对非专业读者而言,主要结论是,这项工作提供了一份早期“接触名单”,列出随α‑突触核蛋白从正常帮助者转变为有害凝聚体时随行的蛋白。研究表明,失去某些保护性关系——例如与特定激酶或质量控制酶的关联——可能与获得新的有毒伙伴同样重要。尽管实验是在简化的细胞模型中进行,尚未证明因果关系,但它们突出了未来在神经元和脑组织中检验的具体候选分子和通路。长期来看,绘制这些不断变化的蛋白邻域可能有助于指导恢复保护性相互作用、支持胰岛素相关信号或防止RNA结合蛋白被捕获的策略,从而可能减缓从微妙分子变化到全面路易体疾病的进展。
引用: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
关键词: α‑突触核蛋白, 路易体病, 蛋白质聚集, 邻近组学, 帕金森病