Clear Sky Science · zh
脉冲低频电磁场(PEMF)与线粒体的相互作用
温和场与细胞的动力工厂
脉冲电磁场(PEMF)治疗已在临床用于促进骨折愈合、缓解关节疼痛并加速术后恢复。然而,我们仍未完全弄清这些温和的低频场在体内如何发挥作用。本研究提出了一个基础但重要的问题:PEMF 信号是否直接影响线粒体——细胞内产生大部分能量的小型动力工厂——如果影响,机制为何?
为何线粒体对日常健康至关重要
线粒体将食物和氧气转化为 ATP,这是一种细胞通用的“能量货币”。当线粒体功能受损时,组织愈合变慢、肌肉更易疲劳,代谢相关疾病可能加重。既往研究提示 PEMF 治疗可改善能量代谢并支持组织修复,因而作者关注特定 PEMF 设备是否能微调线粒体活性。他们使用了明确的磁信号:毫秒级的 30 kHz 正弦波短脉冲,输入能量低,施用于培养的肌肉细胞、大鼠组织和纯化的线粒体。
在活细胞内更细致地观察
在体外培养的人肌肉细胞中,研究团队在 PEMF 暴露后测量了三个关键指标:线粒体内膜跨膜电位(一种微小电池)、活性氧水平(过高会有损害)和一氧化氮——一种可暂时阻断线粒体呼吸的气体。处理约 90 分钟后,线粒体膜电位轻度下降,而一氧化氮水平降低;活性氧并未增加。膜电位的小幅下降既可能表示损伤,也可能意味着 ATP 生成更活跃。由于细胞未表现出应激迹象,作者推测线粒体可能只是运转略快,耗用了内膜上储存的电压。
检测线粒体的“呼吸”方式
为更直接检验这一想法,研究者轻微穿孔细胞外膜,以便精确地向线粒体提供不同燃料并测量耗氧率。他们持续观察到在 PEMF 作用后,与 ATP 生成相关的呼吸趋于增加,尤其在谷氨酸(一种常见的线粒体燃料)存在时更明显。跨多个样本的统计分析表明,PEMF 暴露与燃料种类的组合显著影响线粒体消耗氧气的速度。重要的是,没有迹象表明 PEMF 损害了细胞或其线粒体。相反,这些场似乎选择性地刺激了“耦联”呼吸模式——即氧气消耗与 ATP 合成紧密相连的模式,而不是提高那种浪费性、非耦联的燃料氧化。
炎症、一氧化氮与来自蓝光的意外发现
鉴于一氧化氮在炎症过程中可能积累并阻断线粒体呼吸的关键步骤,团队探究 PEMF 是否能帮助线粒体从这种抑制中恢复。他们向肌肉与肝组织匀浆以及分离的肝线粒体中加入化学一氧化氮供体,使呼吸显著减慢。在这些条件下,PEMF 并未恢复线粒体功能,即便在线粒体高度集中的情况下亦如此。为判断该阻断是否可逆,他们用已知可使一氧化氮从结合位点释放的方法对受抑的线粒体照射蓝光。蓝光部分恢复了呼吸,证明系统可以恢复,但 PEMF 并未带来额外好处。这表明 PEMF 的正面效应并非通过在类似炎症条件下去除一氧化氮来实现。
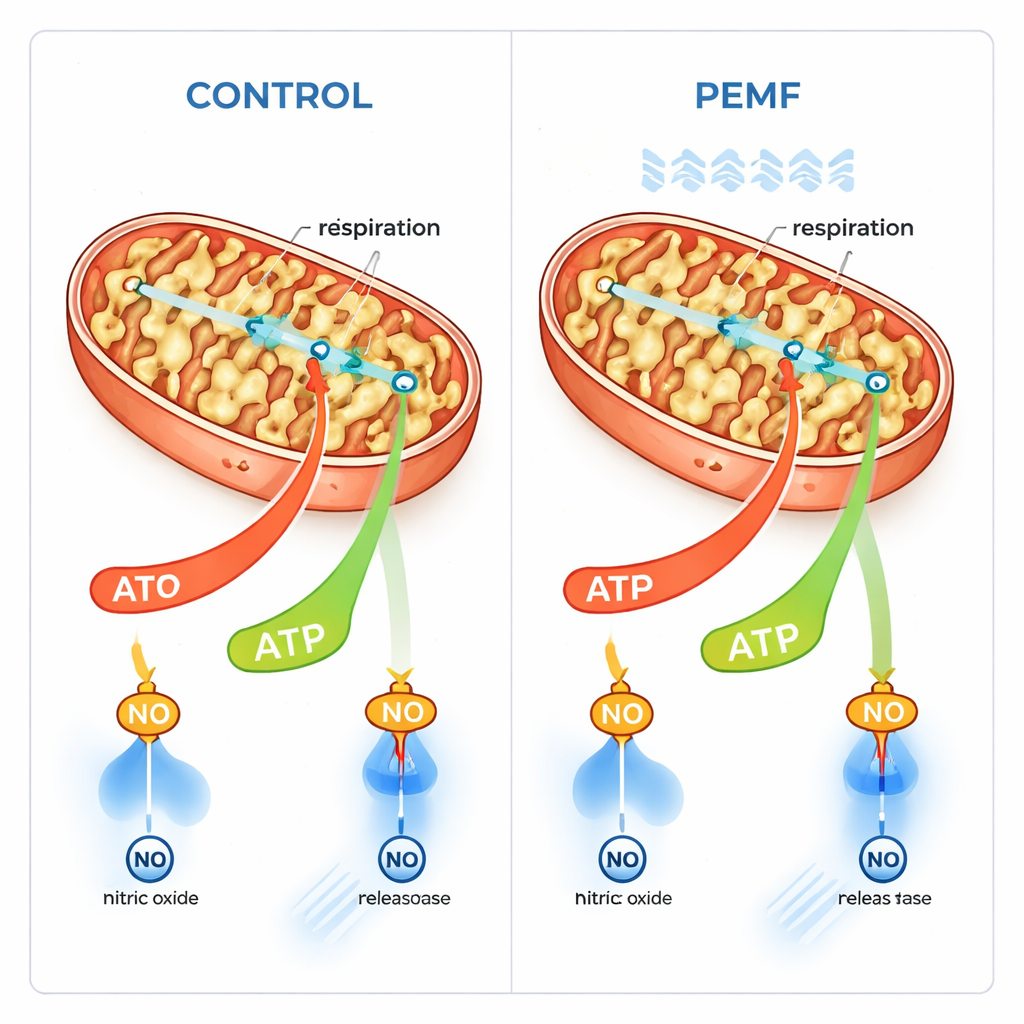
膜通道与能量流动
作者以细胞与电路类比,提出 PEMF 可能主要作用于生物膜。线粒体被一层外膜包裹,外膜包含一个关键的通道蛋白 VDAC,允许与能量相关的分子出入。与内膜的高电压不同,外膜的电位较小,更容易受影响。作者提出 PEMF 可能微妙地改变外膜电位,进而改变 VDAC 门控开启的频率,从而促进燃料与已消耗 ATP 在膜间的流动。这自然会提升耦联的、产生 ATP 的呼吸模式,而不改变电子传递体系本身的最大能力。
对未来治疗的意义
总体而言,研究未发现此类 PEMF 对线粒体有害的证据。相反,PEMF 轻柔地增强了产生 ATP 的那部分线粒体呼吸,同时不改变最大呼吸能力和氧化应激。然而,它并不能挽救被高一氧化氮阻断的线粒体,表明其在发炎组织中的益处必须通过其他途径实现。对于患者和临床医生而言,这些结果支持这样一种观点:精心调谐的电磁场可以将细胞的动力工厂略微推向更高效的能量产出状态——为一些在骨修复、伤口护理和术后恢复中报道的愈合效应提供了一个合理的机制性解释。
引用: Zavadskis, S., Gasser, A.S., Karas, M. et al. Interaction of pulsed low frequency electromagnetic field (PEMF) with mitochondria. Sci Rep 16, 6681 (2026). https://doi.org/10.1038/s41598-026-37527-6
关键词: 脉冲电磁场治疗, 线粒体, 细胞能量, 一氧化氮, ATP 生成