Clear Sky Science · zh
用于在小鼠和猕猴中靶向中脑多巴胺能神经元的MiniPromoters Ple384(TH)和Ple388(PITX3)
为何这项研究对大脑健康重要
大脑中产生多巴胺的细胞帮助我们运动、从奖赏中学习并保持动机。这些细胞也是在帕金森病中死亡的细胞。科学家和临床医生希望将有益的基因或分子工具专门递送到这些易受损的神经元中,无论是在实验动物还是未来的人类中。但如何引导基因疗法仅在正确的细胞中开启,而不在大脑各处广泛表达,一直是一个主要障碍。本研究描述了两个新的、紧凑的DNA“开关”,它们可以可靠地几乎只在小鼠和猕猴的中脑多巴胺神经元中启动基因,从而为更精确且潜在更安全的治疗打开了道路。
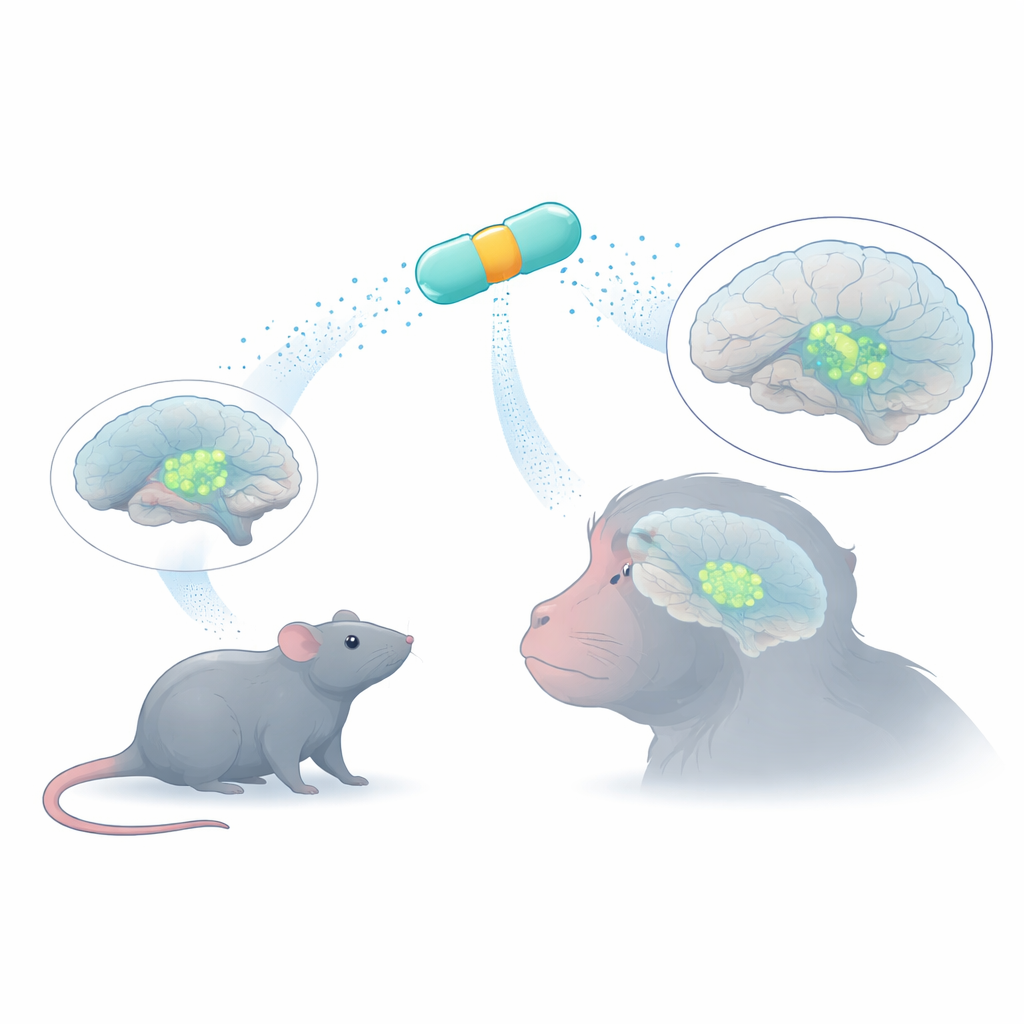
体积小但任务重的遗传开关
为了将治疗性基因送入脑细胞,研究人员常使用腺相关病毒(AAV)——这是一种无害的载体,但只能携带有限量的DNA。在每个病毒内部,短的启动子序列就像一个开关,决定该基因将在何处被激活。许多天然启动子体积太大或选择性太低,会在过多细胞类型中开启基因。研究团队利用生物信息学从人类DNA中设计了八个非常紧凑的“MiniPromoters”——由已知标记多巴胺产生神经元的基因中的调控元件短片段组合而成。他们的目标是获得一组既能装入AAV又能驱动强烈、细胞类型聚焦表达的开关。
在小鼠脑中寻找合适的靶点
这八个候选MiniPromoters首先在小鼠中进行测试。每个启动子被置入携带绿色荧光蛋白的AAV中,使科学家能够观察开关的激活位置。他们将病毒通过血液或直接注入脑的充液空间递送。大多数MiniPromoters未能表现出选择性:有些在许多非多巴胺细胞中被激活,有些几乎不起作用。其中两个表现突出。一个称为Ple384,是从酪氨酸羟化酶(tyrosine hydroxylase,TH)基因的调控区构建而来,该酶是所有儿茶酚胺产生神经元使用的关键酶。另一个Ple388来自PITX3基因,PITX3对中脑某一亚群多巴胺神经元至关重要。Ple384和Ple388在黑质致密部和腹侧被盖区——中脑多巴胺神经元的枢纽——产生明亮且高度受限的信号,超过90%的标记细胞同时携带多巴胺的标志性分子。
从小鼠到猴子:无需深部钻孔注射
任何面向人类疾病的基因疗法最终都必须在灵长类动物中发挥作用,其大脑更大且更复杂。直接注射黑质技术上要求高,且可能损伤这一小而深的结构。相反,研究人员测试了是否可以通过一次向侧脑室注射,将相同的MiniPromoters递送到恒河猴的脑脊液中。使用一种已知能从脑脊液空间广泛扩散的AAV衣壳变体,他们发现Ple384和Ple388都能在黑质和腹侧被盖区的中脑多巴胺神经元中驱动强烈表达,同时在下丘脑和蓝斑等其他多巴胺富集区基本被回避。目标区域中大多数被标记的细胞都是多巴胺神经元,证明这些开关在不同物种间保持了选择性。
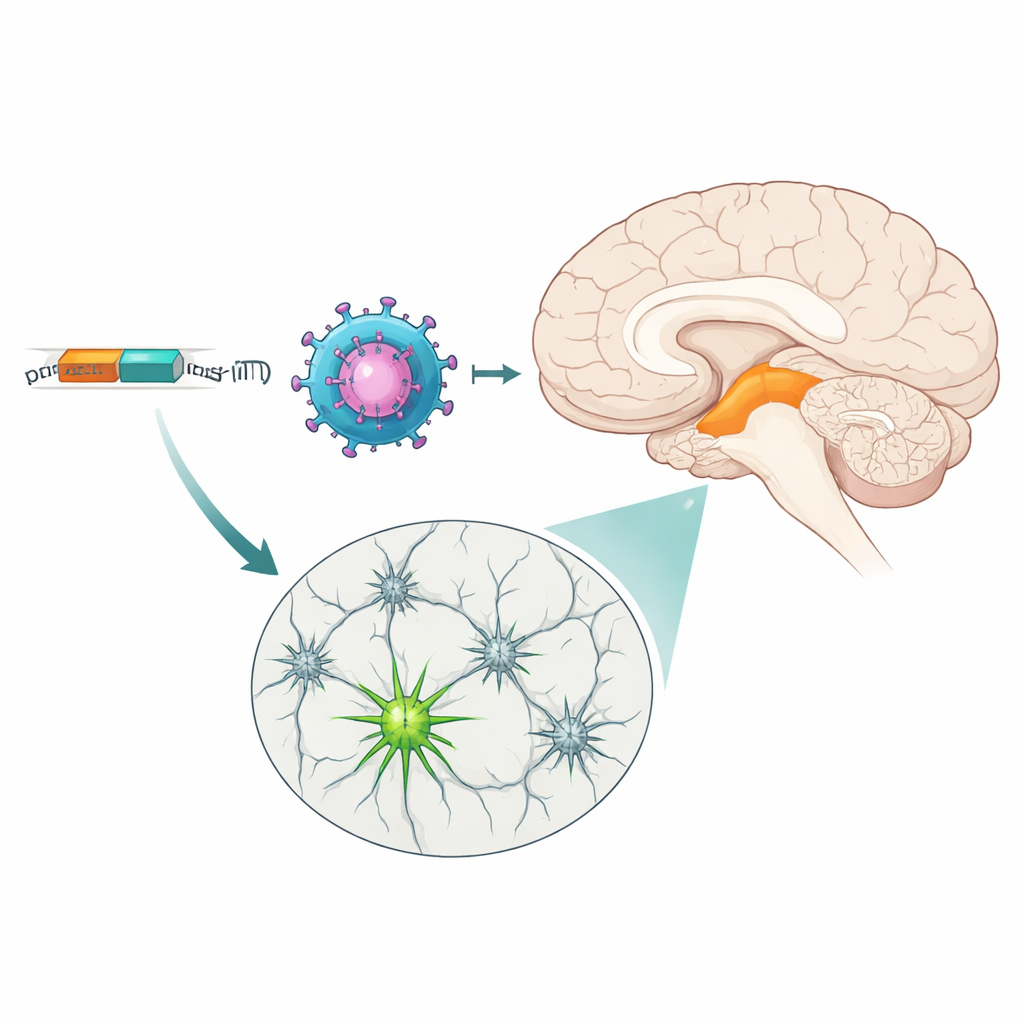
两个工具各有优势
尽管两种MiniPromoters都命中目标,但它们的表达模式不同。基于更广泛表达的酪氨酸羟化酶基因的Ple384在总体上标记了更多神经元,覆盖了黑质的腹层和背层以及更大范围的腹侧被盖区。反映更受限的PITX3基因的Ple388主要标记了腹层亚群神经元,并产生较弱的荧光。非目标表达主要出现在注射点附近以及经血液递送后的一些外周器官,但对照实验表明病毒载体本身能到达许多脑区;限制表达主要由MiniPromoters自身决定,主要局限于中脑多巴胺神经元。这种可调的强度——一种更强且更广,一种更选择性且温和——意味着研究者可以根据需要在温和调控与大范围干预之间选择最合适的开关。
对未来疗法的意义
对非专业读者而言,关键信息是作者创造了两个紧凑的遗传开关,能像精确可编程的电灯开关一样控制小鼠和猕猴的多巴胺神经元。Ple384提供对这些细胞的强烈且广泛的访问,而Ple388则聚焦于更狭窄、特别易受损的亚群。由于这些开关足够小,能够轻松装入常用的病毒载体,它们为治疗基因留下空间,并可能通过避免不必要的大脑区域来减少副作用。随着针对帕金森病及相关疾病的基因疗法发展,这类靶向控制元件将成为既强大又精确的治疗所必需的组成部分。
引用: Galvan, A., Choi, D., Korecki, A.J. et al. MiniPromoters Ple384 (TH) and Ple388 (PITX3) for targeting midbrain dopaminergic neurons in mice and monkeys. Sci Rep 16, 9277 (2026). https://doi.org/10.1038/s41598-026-37466-2
关键词: 多巴胺神经元, 基因疗法, 帕金森病, AAV 载体, 细胞特异性启动子